Geen producten in de winkelwagen.
Eierstokkanker

Per jaar krijgen ongeveer 1200 vrouwen te horen dat ze eierstokkanker of ovariumcarcinoom hebben. De meesten van hen zijn jonger dan zeventig jaar. De diagnose zet hun leven op zijn kop. Na de diagnose belanden ze in een stortvloed van nadere onderzoeken en behandelingen. Eierstokkanker en nu? beschrijft wat er allemaal op je pad komt en welke keuzemogelijkheden er zijn. Ook de verschillende behandelingen komen aan de orde, de bijwerkingen ervan, wat ze betekenen in je dagelijks leven en wat je eraan kunt doen. Al deze informatie helpt je het overzicht te behouden en maakt dat je de regie houdt over je leven.
Bestel ons boek over Eierstokkanker
Wat is eierstokkanker?
Er zijn verschillende soorten eierstokkanker. De epitheliale vorm, en dan met name het hooggradig sereus type, komt het meeste voor. Aan de hand van Anna Verhoog kom je meer te weten over dit type kanker. Helaas geeft eierstokkanker pas laat klachten, waardoor ontdekking vaak plaatsvindt als de ziekte al in een vergevorderd stadium is.
Vormen van eierstokkanker
Het hooggradig sereus type ovariumcarcinoom ontstaat aan het oppervlak van de eierstokken en is het meest voorkomende subtype van de epitheliale vorm van eierstokkanker. Bij 80 procent van de vrouwen bij wie eierstokkanker wordt vastgesteld, betreft het deze vorm.
Andere subtypen van de epitheliale vorm zijn:
- laaggradig sereus carcinoom
- heldercellig carcinoom
- endometroïd carcinoom
- mucineus carcinoom
- carcinosarcoom
- ongedifferentieerd carcinoom
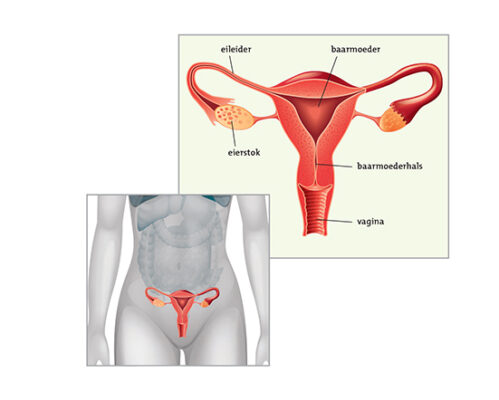
Figuur 1. Anatomie van de vrouwelijke geslachtsorganen.
Hoe eierstokkanker ontstaat
De oorzaak van eierstokkanker is niet bekend. Het vermoeden bestaat dat de epitheliale vorm niet ontstaat in de eierstokken, maar in de eileiders. Dat zou verklaren waarom er soms alleen afwijkingen in het buikvlies te vinden zijn en niet in de eierstokken. De uiteinden van de eileiders hangen namelijk als een soort paraplu over de eierstokken heen (zie figuur 1). Als kwaadaardige cellen uit de eileiders zich verspreiden dan komen ze op het oppervlak van de eierstok of soms op het buikvlies terecht en zien ze kans verder te groeien (zie figuur 2).
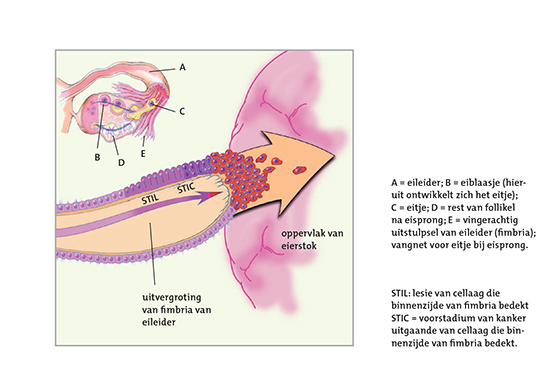
Figuur 2. Hypothese over het ontstaan de de eierstokkanker.
Deze gedachtegang is niet bewezen. Evenmin is bekend of de verschillende subtypen van de epitheliale vorm van eierstokkanker mogelijk verschillende oorzaken hebben. Dat lijkt wel logisch omdat iedere vorm verschillende onderliggende genetische veranderingen (mutaties) kan hebben en anders kan reageren op chemotherapie. Maar veel is ook nog niet bekend over het ontstaan van eierstokkanker en het reageren op de behandeling.
Acht alarmsymptomen
- Gezwollen buik
- Opgeblazen gevoel
- Vol gevoel en/of moeite met eten
- Misselijkheid
- Obstipatie
- Vaker plassen dan normaal
- Bekken- of buikpijn
- Vermoeidheid
Risicofactoren
Naarmate vrouwen ouder worden, is hun kans op eierstokkanker groter. Kinderloze vrouwen hebben iets meer (1 à 2 procent) kans op eierstokkanker dan vrouwen met kinderen.
Als eierstokkanker in de familie voorkomt kan er sprake zijn van familiaire belasting. Hetzelfde geldt voor borstkanker. Bij 10-15 procent van de vrouwen met eierstokkanker komt verandering in een gen voor, de zogenoemde BRCA1- of BRCA2-genmutatie. Vrouwen die drager zijn van de mutatie in het BRCA1-gen lopen 40 procent risico om gedurende hun leven eierstokkanker te krijgen. Voor de BRCA2- genmutatie is dit risico 20 procent.
De verschillende stadia
Als eierstokkanker is vastgesteld, wordt gekeken in welk stadium de ziekte is volgens de systematiek van de International Federation of Gynaecology and Obstetrics (Internationale Federatie van Gynaecologie en Verloskunde, afgekort FIGO). Er kan sprake zijn van FIGO-stadium I, II, III of IV. Een laag stadium van de ziekte (stadium I en IIA) wordt vrijwel alleen ontdekt als de buik of geslachtsorganen om een andere reden worden onderzocht of als de eierstokken uit voorzorg worden verwijderd vanwege een erfelijke belasting.
Eierstokkanker geeft pas laat in de ontwikkeling klachten.
Daarom is bij meer dan twee derde van de patiënten sprake van een hoog stadiumziekte, dus vanaf stadium IIB. Meestal is al sprake van ziekte in stadium III of IV. De kans om dan met de behandeling (chemotherapie en operatie) de ziekte te genezen, is niet groot. Om deze reden wordt eierstokkanker ook wel een silent killer genoemd. Het belang van de behandeling is daarom ook om de ziektevrije periode zo lang mogelijk te laten duren.
Te onderscheiden stadia bij eierstokkanker
- Laag stadium
- Stadium I: beperkt tot de eierstokken (of tot de eileider, als daar de ziekte is begonnen).
- Stadium IIA: uitbreiding naar baarmoeder of eileider als de ziekte in een eierstok is begonnen.
- Hoog stadium
- Stadium IIB: uitbreiding op het buikvlies in het kleine bekken, maar geen doorgroei in blaas of darm.
- Stadium III: uitbreiding in de buikholte buiten het kleine bekken of uitzaaiingen in regionale lymfklieren (figuur 3).
- Stadium IV: uitzaaiingen buiten de buikholte (long, lymfklieren in bijvoorbeeld de lies of hals) of uitzaaiing naar de lever of kwaadaardige cellen in het vocht achter de longen.
Overlevingskans
Voor de overleving van kanker wordt vaak gekeken naar hoeveel mensen vijf jaar na de behandeling nog in leven zijn. Dit wordt de ‘vijfjaarsoverleving’ genoemd. De vijfjaarsoverleving van eierstokkanker in stadium I is ongeveer 90 procent (dat wil zeggen dat van elke honderd vrouwen er nog negentig leven na vijf jaar) en voor stadium II ongeveer 75 procent. De vijfjaarsoverleving voor eierstokkanker in stadium III is 34 procent en voor stadium IV slechts 18 procent. De vijfjaarsoverleving zegt niet dat de ziekte niet weer aanwezig is. Evenmin kan na vijf jaar worden gezegd dat iemand genezen is, want ook daarna nog kan de ziekte opnieuw de kop opsteken, al is die kans een stuk kleiner dan in de eerste jaren na de behandeling.
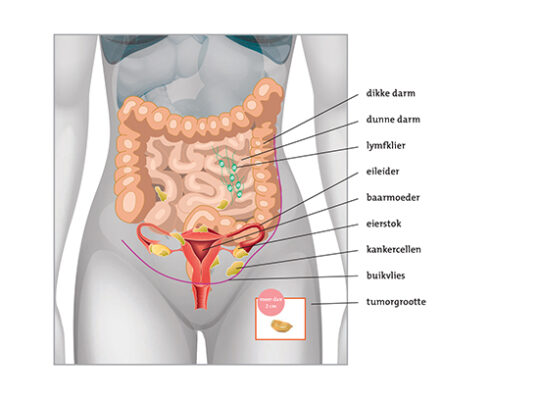
Figuur 3. Eierstokkanker stadium IIIC.
Multidisciplinair team
De behandeling van eierstokkanker is in handen van een multidisciplinair team. De gynaecoloog-oncoloog is verantwoordelijk voor de operatie en de internist-oncoloog voor de behandeling met chemotherapie. De oncologieverpleegkundige coördineert het zorgproces en begeleidt de patiënte en haar naasten gedurende het gehele traject.
Samenvatting
Er bestaan verschillende vormen van eierstokkanker. Het hooggradig sereus type van de epitheliale vorm komt het meest voor. De diagnose eierstokkanker wordt vaak pas laat vastgesteld, omdat er niet snel klachten zijn. De ziekte is dan al in een hoger stadium en heeft zich verspreid in de buikholte (stadium III) of zelfs al buiten de buikholte (stadium IV). De behandeling bestaat in dat geval uit een combinatie van operatie en chemotherapie. De kans op langdurige genezing is helaas niet groot bij eierstokkanker in een hoog stadium.
Soms is eierstokkanker het gevolg van een erfelijke aanleg, waarbij er een mutatie is in het BRCA1- of BRCA2-gen.
Erfelijkheid
Steeds vaker wordt erfelijkheidsonderzoek aangeboden. Er kan namelijk sprake zijn van een erfelijke vorm van eierstokkanker. Als dit het geval is, dan heeft dat op verschillende manieren effect op de patiënte en haar familie.
Reden voor erfelijksheidsonderzoek
Er zijn verschillende redenen voor erfelijkheidsonderzoek. Een erfelijke aanleg voor eierstokkanker kan gepaard gaan met een verhoogd risico op borstkanker of andere tumoren. Deze aanleg kan worden doorgegeven aan de kinderen, voor wie het consequenties kan hebben. Ook kan het aantonen van een erfelijke aanleg bij eierstokkanker gevolgen hebben voor de behandeling als sprake is van terugkeer van eierstokkanker.
Klinisch genetici en genetisch consulenten zijn artsen/paramedici die aan de hand van informatie over het voorkomen van kanker bij een patiënte, bij haar familieleden en aan de hand van de familiesamenstelling nagaan en beoordelen of erfelijkheidsonderzoek zinvol is. Zij lichten hierover voor en zetten indien relevant en gewenst genetisch onderzoek in. Ook communiceren zij over de uitslag met de patiënte en familieleden voor wie dit relevant is en die dit wensen. Alle acht academische ziekenhuizen (AMC, VUMC, UMCG, Radboud UMC, UMCM, UMCU, LUMC en Erasmus MC) en het Antoni van Leeuwenhoek hebben een afdeling Klinische Genetica.
De kern van iedere lichaamscel bevat chromosomen die opgebouwd zijn uit genen, die bestaan uit DNA-moleculen (figuur 4b). Een gen is een afgebakend stukje DNA dat de erfelijke informatie bevat voor bepaalde kenmerken, bijvoorbeeld eiwittten voor de kleur van onze ogen. Een gen kan schematisch gezien worden als een dubbel kralensnoer van DNA-moleculen, die met elkaar vervlochten zijn (figuur 4a). Een verandering in het gen (mutatie) kan in een van de vele kralen (DNA-molecuul) ontstaan. Gedurende het leven vinden steeds mutaties plaats die niet erfelijk zijn omdat ze alleen in enkele lichaamscellen voorkomen (somatische mutaties). Als een mutatie in de geslachtscellen plaatsvindt dan is het wel erfelijk. Dit wordt een ‘kiembaanmutatie’ genoemd. De plaats van het veranderde DNA- molecuul in het gen is dan binnen een familie hetzelfde. Op grond van een en dezelfde verandering kan duidelijk worden dat mensen familie van elkaar zijn, wat wil zeggen dat ze een verre voorouder delen bij wie de kiembaanmutatie als eerste voorkwam. Gelukkig geven de meeste veranderingen van een gen in een familie geen verhoogd risico op kanker, maar een enkele wel.
Figuur 4a. Schematische weergave DNA-streng: een vervlochten dubbel kralensnoer.
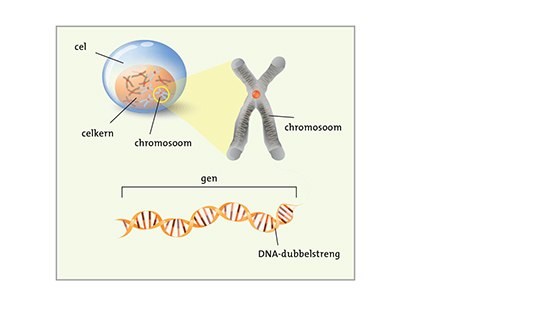
Figuur 4b. Van cel tot DNA. Een cel bevat 46 chromosomen (23 chromosomenparen) die zijn opgebouwd uit DNA.
Mutaties in het DNA
Bij ongeveer 15 op de 100 vrouwen met eierstokkanker (inclusief tubacarcinoom en primair peritoneaal carcinoom) gaat het om een erfelijke vorm. Er is dan sprake van een verandering (mutatie) in het erfelijke materiaal, wat al vanaf de geboorte is meegekregen, een zogenaamde kiembaanmutatie. Zo’n mutatie is aanwezig in álle lichaamscellen. Niet alle vrouwen met een erfelijke aanleg krijgen ook eierstokkanker. Wel lopen ze meer risico op eierstokkanker dan vrouwen zonder een erfelijke aanleg. Erfelijke eierstokkanker kan worden veroorzaakt door verschillende veranderingen in het erfelijk materiaal. Het risico op eierstokkanker verschilt tussen de verschillende erfelijke vormen.
BRCA-genmutatie
De meest relevante erfelijke factor als oorzaak van eierstokkanker is een mutatie in het BRCA1- of het BRCA2-gen (breast cancer gene 1 en 2). Een vrouw die draagster is van een BRCA-genmutatie heeft een sterk verhoogd risico om borstkanker en/of eierstokkanker te krijgen, juist als ze jonger is dan vijftig jaar.
Vrouwen met eierstokkanker die jonger zijn dan zestig jaar of die een Joodse achtergrond hebben lopen meer kans dat ze draagster zijn van een BRCA1- of BRCA2-genmutatie. Hetzelfde geldt voor vrouwen die eerder borstkanker hebben gehad, of bij wie borst- en eierstokkanker in de familie voorkomt.
Bij een BRCA1-genmutatie is het risico om gedurende het leven borstkanker te krijgen 60-80 procent (10 procent bij niet- mutatiedraagsters) en 30-60 procent voor eierstokkanker (1 procent bij niet-mutatiedraagsters). Het risico op eierstokkanker is overigens meestal pas vanaf het veertigste jaar duidelijk verhoogd.
Bij een BRCA2-genmutatie is het risico om gedurende het leven borstkanker te krijgen 60-80 procent en voor eierstokkanker 5-20 procent. De leeftijden waarop de kanker zich manifesteert is gemiddeld iets hoger dan bij een BRCA1-genmutatiedraagster.
Lynch-syndroom
Ook vrouwen met een mutatie in een van de DNA mismatch repair genen (DNA herstelgenen MLH1, MSH2, MSH6 en PMS2) passend bij het Lynch-syndroom hebben een erfelijke vorm van eierstokkanker. Het Lynch-syndroom is een clustering van maag-darmtumoren, gynaecologische tumoren (met name baarmoederkanker), en eventuele andere tumoren. Het wordt ook wel Hereditair Non-polyposis Colorectal Cancer (HNPCC) genoemd. Vrouwen met het Lynch-syndroom hebben een risico van 9 tot 12 procent om gedurende hun leven eierstokkanker te krijgen. Voor hen geldt ook een kans van 15 tot 55 procent op het krijgen van baarmoederkanker en een kans van 80 procent op dikkedarmkanker. Ook hebben ze een verhoogd risico op kanker van de maag, dunne darm, alvleesklier en/of borstkanker. Er bestaan nog meer erfelijke tumorsyndromen waarbij eierstokkanker vaker voorkomt, zoals het Peutz-Jeghers syndroom. Die komen echter zelden voor.
Onderzoek naar een BRCA-genmutatie
Als de chemokuren van Anna er bijna opzitten, komt ze bij de internist- oncoloog terug op het erfelijkheidsonderzoek. Ze wil er graag meer over weten, want ze wil niets liever dan haar dochters deze ziekte besparen.
Anna hoort dat het genetische onderzoek in haar geval belangrijk is en ze krijgt een verwijzing naar de afdeling Klinische Genetica.
Bij de eerste afspraak met de genetisch consulent nemen Anna en Jeroen de hele familie van Anna door aan de hand van de stamboom. Daaruit blijkt dat een zus van haar opa, aan vaderskant, vrij jong is overleden aan borstkanker. Opa had verder geen zussen en heeft zelf alleen zonen gekregen, waaronder de vader van Anna. Verder is er nog een nicht aan vaderskant, die nu 55 jaar is en op haar vijftigste borstkanker kreeg. Anna heeft ook nog een oudere broer met een volwassen dochter.
Ze bespreken de voor- en nadelen van erfelijkheidsonderzoek, zowel voor Anna als voor haar gezonde familieleden. De uitkomst van het erfelijkheidsonderzoek kan gevolgen hebben als haar dochters of nicht levens- of arbeidsongeschiktheidsverzekeringen willen afsluiten. Verzekeraars vragen dan altijd om een gezondheidsverklaring.
Bovendien heeft de verzekeraar het recht om vragen te stellen over erfelijke aandoeningen in de familie als de gevraagde dekking boven een bepaalde grens uitkomt.
Ook de eventuele psychische gevolgen van erfelijkheidsonderzoek komen aan de orde. De consulent beschrijft de consequenties. De wetenschap van een erfelijke aanleg voor een ziekte kan spanning en angst oproepen. Het kan zelfs de familierelaties aantasten. Sommige familieleden willen helemaal niet weten dat er erfelijkheidsonderzoek plaatsvindt, laat staan de uitkomsten ervan. Het gebeurt ook weleens dat de boodschapper van het slechte nieuws verantwoordelijk wordt gesteld voor dit nieuws. Anna en Jeroen realiseerden zich niet dat er zoveel bij komt kijken. Anna denkt goed na over alles wat ze te horen heeft gekregen en besluit om erfelijkheidsonderzoek te laten doen.
Als bij Anna een BRCA-genmutatie wordt aangetoond, dan heeft zij een verhoogd risico op borstkanker. Er kan hiervoor controle worden afgesproken om eventuele borstkanker vroegtijdig te ontdekken. De internist-oncoloog legde Anna eerder al wel uit dat haar levensverwachting nu allereerst bepaald wordt door de eierstokkanker die ze heeft en op dit moment niet door het verhoogde risico op borstkanker. De kans is helaas aanwezig dat de eierstokkanker na verloop van tijd terugkomt. Gelukkig kan het ook zijn dat de eierstokkanker niet terugkomt en in de toekomst periodiek onderzoek naar borstkanker wel een rol gaat spelen.
Als een erfelijke aanleg is aangetoond, is het ook mogelijk om andere familieleden (dochters en nichten) te informeren over de erfelijke aanleg. Zij krijgen jaarlijks borstonderzoek aangeboden en zij komen voor de keuze te staan of zij in aanmerking willen komen voor mutatieonderzoek en op welk moment in hun leven ze deze test willen laten uitvoeren. Daarmee komen ze te weten of ze een verhoogd risico hebben om borst- of eierstokkanker te krijgen.
Gezonde vrouwen met erfelijke aanleg
Gezonde BRCA1- of BRCA2-genmutatiedraagsters (of zij met 50 procent kans op deze mutatie) komen in aanmerking voor borstkankercontrole vanaf 25 jaar met als doel opsporing van borstkanker in een laag stadium, waardoor de kans op genezing groot is. Ook preventieve verwijdering van de borsten is mogelijk. Het risico op borstkanker wordt dan weliswaar kleiner, maar de impact van deze ingreep is groot op het gebied van uiterlijk, zelfbeleving en seksualiteit. Screening op eierstokkanker wordt niet meer geadviseerd, omdat het niet effectief is gebleken bij vrouwen met een BRCA1- of BRCA2- genmutatie. Preventieve verwijdering van de eierstokken en eileiders is bespreekbaar na het 35-40ste jaar (of vijf jaar onder de leeftijd van het jongste aangedane familielid) als er geen kinderwens meer is.
Vrouwen met Lynch-syndroom krijgen een jaarlijkse screening op baarmoederkanker aangeboden, en dan worden ook de eierstokken onderzocht.
Preventieve verwijdering eierstokken
Als een preventieve verwijdering van de eierstokken/eileiders wordt overwogen, worden vrouwen verwezen naar een gynaecoloog met aandacht voor erfelijke tumoren. Deze informeert de vrouw over de ingreep en de gevolgen daarvan. Het is belangrijk je te realiseren dat het verwijderen van de eierstokken leidt tot een vervroegde menopauze en verhoogd risico geeft op hart- en vaatziekten op latere leeftijd. Vrouwen jonger dan 45 jaar die niet eerder borstkanker hebben gehad, krijgen vaak hormoonvervangende behandeling om het gebrek aan vrouwelijk hormoon (oestrogenen) op te vangen. Vrouwen die wel eerder borstkanker hebben gehad, en vrouwen ouder dan vijftig jaar wordt geadviseerd geen hormoonvervangende behandeling te gebruiken. Het is ook belangrijk om je te realiseren dat de ingreep geen absolute bescherming geeft tegen eierstokkanker (inclusief eileiderkanker en extraovarieel kanker). Het risico wordt wel met ruim 95 procent verlaagd, maar een klein risico om toch nog buikvlieskanker (primair peritoneaal carcinoom) te krijgen, blijft bestaan.
Vrouwen met een BRCA2-genmutatie kunnen de operatie uitstellen tot ze iets ouder zijn, omdat eierstok/eileiderkanker bij hen gemiddeld op latere leeftijd voorkomt dan bij BRCA1- genmutatiedraagsters. In het algemeen wordt bij BRCA1- genmutatiedraagsters aanbevolen de operatie uit te voeren tussen 35 en 40 jaar, en bij BRCA2-genmutatiedraagsters tussen 40 en 45 jaar.
Bij vrouwen met Lynch-syndroom wordt geen duidelijk leeftijdsadvies gegeven, vanwege de grote spreiding in leeftijd van optreden van eierstokkanker. Lynch-syndroom geeft vooral risico op baarmoederkanker bij een MSH6-mutatie. Bij een MSH6-mutatie is het advies preventief de baarmoeder te verwijderen.
Voor BRCA-genmutatiedraagsters die al eerder voor kanker zijn behandeld (borst- of eierstokkanker) geldt een geïndividualiseerde advisering waarbij verschillende specialisten betrokken zijn. Dit kan het meest optimaal plaatsvinden door vrouwelijke patiënten na het bekend worden van een BRCA-genmutatie te verwijzen naar een polikliniek Familiaire tumoren. Daar vindt multidisciplinair overleg plaats om te komen tot een optimaal advies als het gaat om vroegdiagnostiek en eventuele preventieve chirurgische ingrepen.
Nog meer redenen voor erfelijkheidsonderzoek
Bij patiënten met eierstokkanker is er naast dit alles nog een reden om erfelijkheidsonderzoek te laten doen. Er kunnen consequenties zijn voor de behandeling in de toekomst als de kanker onverhoopt terugkomt. Vrouwen met BRCA1- of BRCA2-geassocieerde eierstokkanker, die is teruggekomen, kunnen in bepaalde situaties behandeld worden met nieuwe medicijnen (zie hoofdstuk 5).
Omdat de keuze voor de therapie afhankelijk kan zijn van de aanwezigheid van een BRCA1- of BRCA2-genmutatie is het belangrijk deze uitslag tijdig te weten. Ook daarom wordt nu aan iedere vrouw die eierstokkanker heeft of heeft gehad erfelijkheidsonderzoek aangeboden.
Ontwikkelingen in erfelijkheidsonderzoek
Bij erfelijkheidsonderzoek zal er niet altijd een veroorzakende erfelijke aanleg gevonden worden, omdat nog niet alle mutaties bekend zijn.
Het is de verwachting dat in de toekomst meer genmutaties bekend worden.
Voor erfelijkheidsonderzoek is een bloedmonster nodig. Aangezien bij een erfelijke aanleg de mutatie in de kern van iedere lichaamscel aanwezig is (kiembaanmutatie), komt deze ook voor in de kern van de witte bloedcellen (rode bloedcellen en bloedplaatjes hebben geen kern). Via de afname van een bloedmonster is erfelijk materiaal dus eenvoudig te verkrijgen. De vooropgezette kans om een genmutatie te vinden is het grootst bij degene die kanker heeft (gehad). Bij deze persoon wordt namelijk aangenomen dat de ziekte is veroorzaakt door een genmutatie (zie figuur 5). Deze persoon wordt gevraagd om bloed af te staan voor het erfelijkheidsonderzoek. Het is tegenwoordig ook steeds vaker mogelijk om een mutatieanalyse te verrichten op DNA dat is geïsoleerd uit tumormateriaal, maar deze technieken zijn nog in ontwikkeling. Als in de tumor een mutatie wordt gevonden, betekent dat echter niet dat er ook sprake is van een kiembaanmutatie. Het kan zijn dat de mutatie alleen in het tumorweefsel zit en dat er dan dus
sprake is van een somatische mutatie. Om te weten of er toch sprake is van een kiembaanmutatie, moet het gebruikelijke erfelijkheidsonderzoek worden ingezet. Het toekomstige voordeel van eerst een mutatieanalyse in de tumor lijkt te zijn dat alleen de vrouwen bij wie de mutatie in de tumor is gevonden, verwezen hoeven te worden voor erfelijkheidsonderzoek.
Samenvatting
Een erfelijke aanleg voor eierstokkanker kan gepaard gaan met een verhoogd risico op borstkanker of andere tumoren. Deze aanleg kan worden doorgegeven aan de kinderen, voor wie het consequenties kan hebben. Daarnaast kan het aantonen van een erfelijke aanleg bij eierstokkanker soms gevolgen hebben voor de behandeling van eierstokkanker. De meest relevante erfelijke factor als oorzaak van eierstokkanker is een mutatie in het BRCA1- of het BRCA2-gen (breast cancer gene 1 en 2). Een vrouw die draagster is van een BRCA- genmutatie heeft een sterk verhoogd risico om borstkanker en/of eierstokkanker te krijgen. Een andere vorm van een erfelijke aanleg voor eierstokkanker is het Lynch-syndroom. Onderzoek naar erfelijke aanleg wordt veelal verricht door klinisch genetici en genetisch consulenten. Daarnaast vindt steeds vaker onderzoek plaats naar (somatische) mutaties op DNA dat is geïsoleerd uit de tumor.
Onderzoek en diagnose
Om de diagnose eierstokkanker te kunnen stellen zijn verschillende onderzoeken nodig. De beeldvorming en de bepaling van het gehalte CA-125 spelen daarin een belangrijke rol.
Klachten passend bij eierstokkanker
Anna ging vanwege vermoeidheid, een opgezette buik en verminderde eetlust naar de huisarts. Eierstokkanker is een ziekte die pas laat klachten geeft en is daardoor bij 70 procent van de patiënten in een gevorderd stadium op het moment dat ze naar de dokter gaan.
Vandaar de al eerder genoemde term silent killer. Klachten zoals vermoeidheid, problemen bij de ontlasting en/of plassen, een opgezette buik, snel een vol gevoel en verminderde eetlust kunnen aanwijzingen zijn dat er sprake is van eierstokkanker. Zulke klachten zijn echter niet specifiek voor deze ziekte en kunnen ook bij andere aandoeningen voorkomen of het gevolg zijn van de overgang en het ouder worden.
Lichamelijk en gynaecologisch onderzoek en echografie
Anna ging naar haar huisarts vanwege haar klachten. Haar buik was zo opgezet en gespannen door vocht (ascites) dat de huisarts bij lichamelijk onderzoek meteen verdenking koesterde op eierstokkanker. Het kan ook zijn dat als je met klachten naar de huisarts gaat, er nog geen vocht in je buik zit, maar dat de huisarts of gynaecoloog bij inwendig onderzoek een vergrote eierstok voelt. Ook dat is reden voor aanvullend onderzoek door middel van een echo. De huisarts kan ervoor kiezen om een echo in een diagnostisch centrum te laten maken of dat door de gynaecoloog te laten doen (figuur 6). Op de echo is dan een zogenoemde simpele cyste (die goedaardige kenmerken heeft) of een cyste met kwaadaardige kenmerken te zien.
Bloedonderzoek
Anna is 55 jaar en heeft haar laatste menstruatie langer dan een jaar geleden gehad. Dit betekent dat zij postmenopauzaal is. Als een eierstok bij een postmenopauzale vrouw een cyste bevat, wordt het CA-125, een eiwit dat gemaakt kan worden door eierstokkankercellen, in het bloed bepaald. Het gehalte CA-125 in het bloed is bij 80 procent van de vrouwen met een hoog stadium eierstokkanker verhoogd en wordt daarom een tumormarker genoemd. Bij vrouwen met eierstokkanker in een laag stadium is het CA-125 slechts in 45 procent van de gevallen verhoogd. Het CA-125 kan overigens ook verhoogd zijn bij goedaardige aandoeningen zoals een eileiderontsteking of endometriose (dan is baarmoederslijmvlies buiten de baarmoederholte aanwezig) en vlak voor of tijdens de menstruatie. Omdat het CA-125 ook normaal kan zijn bij eierstokkanker is het dus een aspecifieke tumormarker.
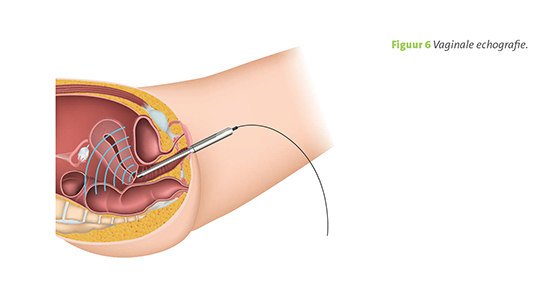
Figuur 6. Vaginale echografie.
CT-scan
Als de klachten, het lichamelijk onderzoek, het echobeeld en/of het
CA-125 in de richting van de diagnose eierstokkanker wijzen, dan vindt er nog een CT-scan plaats van de longen en buik. Op de CT-scan zijn eventuele afwijkingen te zien in de eierstokken, op het buikvlies (peritoneum), in het vetschort (een grote plooi van het buikvlies die van de maag af naar beneden hangt en die een verbinding heeft met het dwarse deel van de dikke darm, figuur 7, wordt ook omentum genoemd), in de lymfeklieren, milt, lever en longen. Ook wordt gekeken of de tumor is doorgegroeid naar de darmen of blaas.
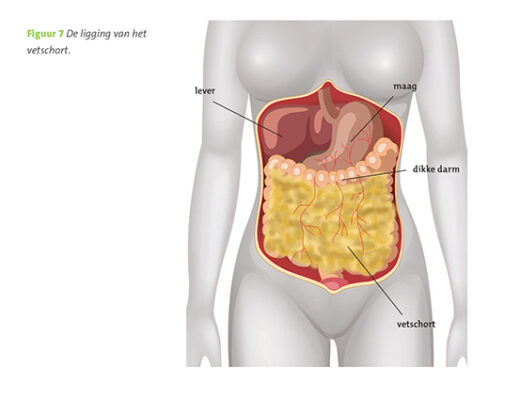
Figuur 7. De ligging van het vetschort.
Punctie en weefselonderzoek
Als de buik veel vocht (ascites) bevat, wordt een cytologische punctie genomen van dat vocht. Het vocht wordt onderzocht onder de microscoop om de diagnose eierstokkanker te kunnen bevestigen. Als de CT-scan tumoren zichtbaar maakt op het peritoneum en/of omentum, dan wordt dit weefsel aangeprikt (histologische punctie) en onderzocht onder de microscoop.
Onderzoek en diagnostiek samengevat
Als uit het onderzoek tot nu toe niet duidelijk is of er sprake is van eierstokkanker dan kan besloten worden om een eierstok te verwijderen. Dat kan met een kijkoperatie, maar het kan ook zijn dat de buik wordt geopend. Soms is de ziekte zo ver gevorderd dat het niet mogelijk is om een eierstok te verwijderen. De eierstokken zijn dan niet meer herkenbaar door tumorweefsel in het gehele bekken. In dat geval wordt een stuk tumorweefsel uit bijvoorbeeld het vetschort gehaald voor verder onderzoek.
- Lichamelijk en gynaecologisch onderzoek: palperen massa in het bekken en bovenbuik. Klieren palperen in hals en liezen
- Laboratoriumonderzoek: tumormarker CA-125, niet tumor-specifiek
- Beeldvorming: vaginale echo en zo nodig CT-scan
- Punctie: indien nodig cytologische punctie van buikvocht en/of histologische punctie van een tumorlokalisatie
- Als de diagnose eierstokkanker eenmaal is gesteld
Anna heeft vocht in haar buik wat bij eierstokkanker meestal betekent dat er sprake is van een hoog stadium ziekte. Eierstokkanker in stadium III en IV wordt anders behandeld dan eierstokkanker in een laag stadium (I en IIA), namelijk met chemotherapie meestal gecombineerd met een operatie in plaats van alleen een operatie. Zie hoofdstuk 1 voor de indeling in stadia volgens de FIGO-stadiumclassificatie en hoofdstuk 4 voor informatie over de behandeling van eierstokkanker.
Diagnose tijdens operatie
Bij een (verdenking op) laag stadium eierstokkanker wordt vooraf meestal geen weefsel onderzocht. Er wordt een risico-inschatting gemaakt op basis van de leeftijd, het echobeeld en het gehalte CA-125 in het bloed. Afhankelijk van die risico-inschatting vindt een operatie plaats. Tijdens de operatie wordt de verdachte eierstok naar de patholoog gebracht voor een vriescoupe. Een vriescoupe is een versnelde techniek, waarbij het ingestuurde weefsel (gedeeltelijk) wordt bevroren, waardoor het snel mogelijk is dunne coupes (plakjes) te snijden die onder de microscoop kunnen worden beoordeeld. De uitslag van de vriescoupe kan afwijken van de latere definitieve uitslag. Als de patholoog zeker weet dat het beeld van de vriescoupe past bij eierstokkanker, zal de operateur doorgaan met een uitgebreidere operatie. Soms wordt de diagnose eierstokkanker pas gesteld nadat een eierstok is verwijderd. In dat geval vindt een tweede operatie plaats. Tijdens deze tweede operatie wordt een stadiëring verricht. Deze wordt in hoofdstuk 4 beschreven.
Samenvatting
Eierstokkanker is een ziekte die pas laat klachten geeft en is daardoor bij 70 procent van de patiënten in een gevorderd stadium op het moment dat ze naar de dokter gaan. Om de diagnose eierstokkanker te kunnen stellen zijn verschillende onderzoeken nodig. Als de bevindingen niet duidelijk zijn, kan besloten worden om een eierstok te verwijderen. Uiteindelijk is het van belang het stadium van de ziekte te bepalen en daarmee het behandelplan. Dat kan bestaan uit alleen operatie of uit een operatie en behandeling met chemotherapie.
Behandeling
De behandeling van eierstokkanker bestaat over het algemeen uit een operatie en chemotherapie bij een hoog stadium en uit een operatie bij een laag stadium eierstokkanker.
De behandeling van eierstokkanker bestaat meestal uit een operatie en chemotherapie en is afhankelijk van het stadium van de ziekte. Een multidisciplinair team van artsen en verpleegkundigen beoordeelt wat de beste behandeling voor iedere patiënte is. Dit gebeurt tijdens een regulier overleg tussen verschillende specialisten, een zogenaamd multidisciplinair overleg (vaak afgekort als MDO) of een tumorwerkgroep. De klachten en de bevindingen bij het aanvullende onderzoek, zoals echo’s, scans en biopten, worden nogmaals bekeken en besproken en op grond daarvan worden het juiste stadium en de behandeling vastgesteld.
- Eierstokkanker wordt voor het vaststellen van de behandeling in grofweg twee groepen ingedeeld: (zie voor FIGO-stadium hoofdstuk 1)
- het lage stadium (FIGO-stadium I-IIA): de tumor beperkt zich tot de eierstokken, de eileiders en de baarmoeder;
- het hoge stadium (FIGO stadium IIB-IV): de tumor heeft zich uitgebreid in het bekken, de buikholte, de lymfeklieren, of buiten de buikholte.
- Eierstokkanker in een laag stadium
Als de ziekte in een vroeg stadium is ontdekt, dan is een operatie over het algemeen toereikend en is nabehandeling met chemotherapie niet nodig. Deze operatie wordt een stadiëring genoemd (waarbij de hele buik schematisch is beoordeeld en onderzocht). Een stadiëringsoperatie moet wel volledig zijn uitgevoerd om het stadium heel betrouwbaar te kunnen vaststellen. Wat een volledige (complete) stadiëringslaparotomie precies inhoudt, wordt later in dit hoofdstuk beschreven. Als de stadiëringsoperatie niet volledig is uitgevoerd, dan bestaat de kans dat er ergens ziekte in de buik aanwezig is zonder dat dit bekend is. Dat betekent dat de ziekte al wat uitgebreider kan zijn en mogelijk een hoger stadium heeft bereikt. In geval van een incomplete stadiëring wordt vanwege de kans op de aanwezigheid van ziekte elders in de buik chemotherapie aanbevolen als nabehandeling. De kans op overleving is dan even groot als bij een volledige stadiëring.
Bij laag stadium eierstokkanker kan de tumor wel bepaalde kenmerken hebben (hoge graad en bepaalde subtypes) die meer kans geven op terugkeer van de ziekte. Bij deze risicogroepen wordt daarom een aanvullende behandeling met chemotherapie overwogen.
Eierstokkanker in een hoog stadium
Bij veel vrouwen wordt eierstokkanker vaak laat, dat wil zeggen in een hoog stadium van de ziekte ontdekt. Dan is de tumor al uitgebreid tot bijvoorbeeld in de bovenbuik (in het vetschort). De behandeling bestaat dan eerst uit een operatie (primaire debulking) met als doel het tumorweefsel zo veel mogelijk, liefst compleet, te verwijderen. De zes kuren chemotherapie die daarop volgen, moeten de resterende kankercellen doden.
Steeds vaker wordt bij eierstokkanker in FIGO-stadium IIIC en IV begonnen met drie kuren chemotherapie. De bedoeling daarvan is de tumor te verkleinen en de operatie nadien beter te kunnen uitvoeren. Na deze kuren wordt een CT-scan gemaakt. Als op de CT-scan te zien is dat de tumor kleiner is geworden, dan vindt een operatie plaats om de tumor maximaal te verwijderen (intervaldebulking). Daarna volgen opnieuw drie chemokuren. Deze behandeling met chemotherapie om de operatie heen wordt ook wel sandwichtherapie genoemd.
Anna ondergaat haar eerste chemotherapie
De sandwichtherapie is ook de behandeling die Anna krijgt. Zij begint al snel nadat ze de definitieve diagnose te horen heeft gekregen en het behandelplan is vastgesteld met de eerste chemokuur. Ook al wordt ze overdonderd door alle berichten, ze vindt het toch een fijn idee om snel te starten en eindelijk iets te doen. Voor de eerste kuur bespreken Anna en Jeroen met de oncologieverpleegkundige alle mogelijke bijwerkingen en krijgen ze praktische adviezen. Omdat ze twee toiletten hebben, besluiten ze dat het toilet boven voor Anna is en dat de rest van de familie het toilet beneden gebruikt. De eerste dag na de kuur valt tot haar grote opluchting erg mee, ze heeft nagenoeg geen last van misselijkheid. Ze heeft meer energie dan in de weken ervoor, en besluit zelfs de hond eens lekker lang uit te laten. Hoe anders zijn de paar dagen erna. Ze is nu wat misselijk en al haar botten en spieren doen zeer. Zodra ze uit bed is, wil ze eigenlijk alleen maar terug. Haar man en dochters zijn extra lief voor haar en willen het liefst alles overnemen, en dat benauwt haar een beetje. Gelukkig knapt ze in de tweede week snel op en in de derde week voelt ze zich prima. Dan begint de tweede kuur, maar nu weet ze een beetje wat haar te wachten staat.
De meeste patiënten (70 procent) reageren goed op de behandeling. De ziekte is aan het einde van de behandeling niet of nauwelijks meer aanwezig. Helaas komt bij een groot deel van deze patiënten de ziekte later toch terug.
Operatie
Om beter te kunnen begrijpen wat er gebeurt tijdens een operatie, is het handig meer te weten van de anatomie en de manier waarop de ziekte zich uitbreidt. Eierstokkanker begint in (of beter gezegd op) de eierstok (ovarium), in de eileider (tuba) of op het buikvlies (peritoneum). De ziekte kan zich daarna over het gehele buikvlies verspreiden en in het vetschort (omentum) terechtkomen (figuur 8). De ziekte kan doorgroeien in baarmoeder (uterus), blaas of darmen (figuur 9). Uitzaaiingen via de lymfevaten (figuur 10) zijn niet ongewoon en ook kunnen uitzaaiingen voorkomen via het bloed naar de lever of longen.
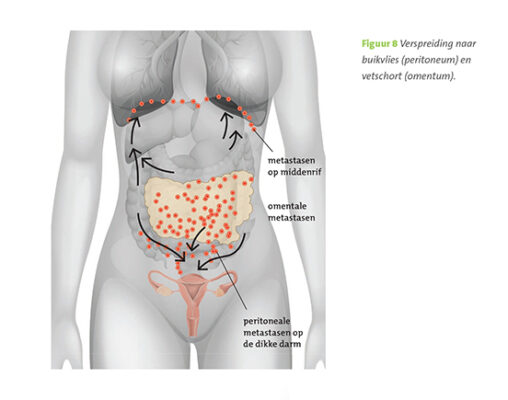
Figuur 8. Verspreiding naar buikvlies (peritoneum) en vetschort (omentum).
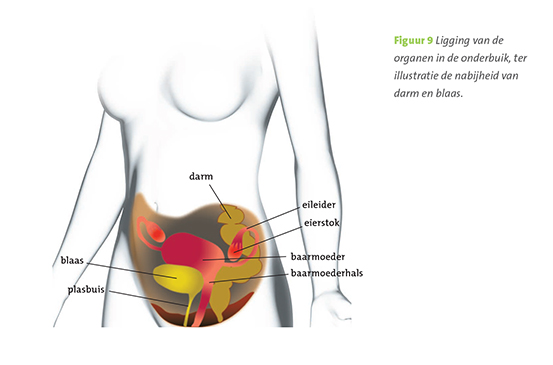
Figuur 9. Ligging van de organen in de onderbuik, ter illustratie de nabijheid van darm en blaas.
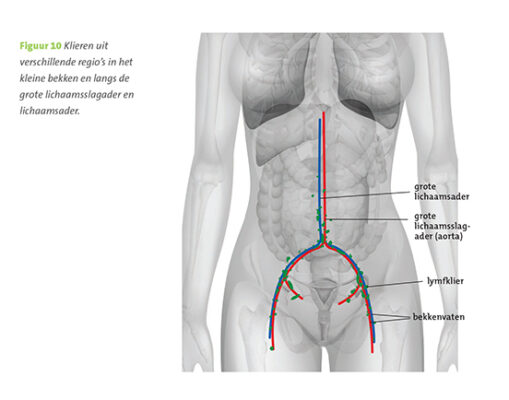
Figuur 10. Klieren uit verschillende regio’s in het kleine bekken en langs de grote lichaamsslagader en lichaamsader.
Stadiëringsoperatie bij eierstokkanker in een laag stadium
Een stadiëringsoperatie is heel belangrijk om vast te stellen waar de tumoren zich bevinden. De volledigheid van de stadiëring is de belangrijkste voorspellende waarde voor overleving. Hoe vollediger het resultaat, hoe kleiner de kans is dat de ziekte terugkomt als sprake is van eierstokkanker in een laag stadium.
De stadiëringsoperatie verloopt in Nederland via een vast protocol, dat is vastgelegd in de richtlijn Epitheliaal Ovariumcarcinoom (www.oncoline.nl).
Dat betekent dat de chirurg eerst een verticale snee maakt in de buik. Dat heet in vaktaal een mediane onder- en bovenbuiklaparotomie (figuur 11). Vervolgens wordt buikvocht (ascites) afgenomen voor onderzoek. Daarna inspecteert de chirurg de hele buikholte en verwijdert hij de baarmoeder, de eileiders, de eierstokken en het vetschort. Vervolgens neemt hij stukjes weefsel weg (stadiëringsbiopten) van alle plaatsen waarmee de tumor verkleefd was en van de plaatsen die er verdacht uitzien. De richtlijn schrijft voor dat er ook van verschillende plaatsen op het buikvlies biopten moeten worden genomen. Om te kunnen beoordelen of de lymfklieren zijn aangetast, worden minimaal tien klieren uit het bekken en langs de grote lichaamsslagader weggenomen en onderzocht. Dit heet lymfkliersampling.
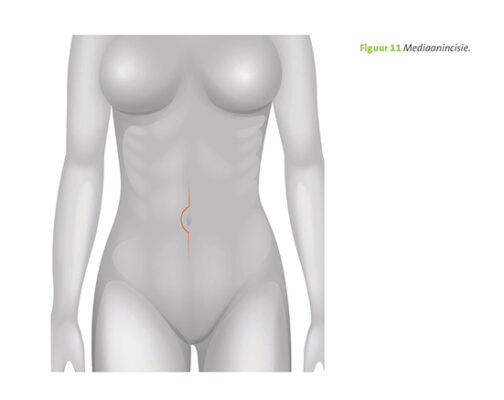
Figuur 11. Mediaanincisie.
Onderzoek van het weefsel
De patholoog onderzoekt al het weefsel dat is afgenomen tijdens de stadiëringsoperatie onder de microscoop. Hij stelt vast hoe sterk de kankercellen afwijken van de gezonde cellen. De differentiatiegraad van de tumor geeft aan hoe sterk de kankercellen afwijken van de gezonde cellen. Deze differentiatiegraad is net zo belangrijk als de volledigheid van de stadiëringsoperatie, want het geeft een indicatie van de prognose.
De vijfjaarsoverleving bij laag stadium eierstokkanker is bij:
- laaggradige tumor en volledige stadiëring: 90-100 procent
- hooggradige tumor en volledige stadiëring: 78-85 procent.
De gynaecologisch oncoloog, de internist-oncoloog, de oncologieverpleegkundige en de patholoog bespreken de uitslag van het weefselonderzoek in het multidisciplinaire overleg. De belangrijkste vraag die op tafel ligt is of aanvullende chemotherapie nodig is. Als de stadiëringsoperatie volledig is uitgevoerd, worden hierdoor bij 20 tot 25 procent van de vrouwen uitzaaiingen van de ziekte ontdekt. Als dat zo is, zal aanvullende chemotherapie nodig zijn. Er is dan namelijk geen sprake meer van eierstokkanker in een laag stadium, maar van een hoger stadium.
Als de stadiëringsoperatie niet volledig is uitgevoerd, dan zal een complete herstadiëringsoperatie het advies zijn. Als dat niet mogelijk is, vanwege bijvoorbeeld een verhoogd risico op complicaties door aanwezigheid van een chronische ziekte of obesitas, is de kans op verspreiding van de ziekte groot. Daarom is in dat geval aanvullende chemotherapie nodig.
Operatie bij eierstokkanker in een hoog stadium (debulking)
Bij het hoge stadium, FIGO-stadium IIB, IIC, III, IV (zie hoofdstuk 1), zijn de volgende factoren belangrijk om te kunnen voorspellen hoe de ziekte verloopt en hoe groot de kans is dat de ziekte terugkomt.
- De differentiatiegraad van de tumor, die aangeeft hoe sterk de kankercellen afwijken van de gezonde cellen.
- De lichamelijke conditie (performance-score, volgens WHO of Karnofsky, en bijkomende onderliggende aandoeningen geven informatie over de conditie en het functioneren van een vrouw)
- De grootte van de tumorrest na de operatie.
Anna wordt geopereerd
Na de drie kuren wacht Anna op de operatie. Het is een spannende periode. Na haar derde kuur wordt de reactie van de tumor (tumorrespons) op de chemotherapie bepaald. Om duidelijk te krijgen wat de tumorrespons is, krijgt Anna een gynaecologisch onderzoek, een vaginale echografie, wordt er bij haar bloed geprikt en een CT-scan gemaakt. Het wachten op de uitslag is voor haar slopend. Samen met Jeroen en haar zus komt ze op de polikliniek voor de uitslag. Anna krijgt een goed bericht. Ze heeft respons, de afwijkingen zijn kleiner geworden. Het klopt dus dat haar klachten minder zijn; ook de ascites is verdwenen.
Ter voorbereiding op de operatie gaat Anna naar de anesthesist voor een screening en informatie over de narcose en over de pijnstilling na de operatie die de eerste dagen via een ruggenprik (epiduraal katheter) wordt toegediend.
Een paar dagen later wordt Anna geopereerd. De gynaecoloog voert een complete intervaldebulking uit en verwijdert beide eierstokken met eileiders, de baarmoeder en het vetschort (omentum) en alle zichtbare tumorlokalisaties op het buikvlies en darmen. Als Anna terug is op de afdeling is ze nog erg slaperig. Ze heeft in haar arm een infuus waar ze vocht door krijgt en zo nodig medicijnen tegen de misselijkheid. In haar rug zit het dunne slangetje (epiduraal katheter) waardoor ze pijnstilling krijgt. Omdat het gevoel in haar onderlichaam daardoor verminderd is, heeft zij een urinekatheter in haar blaas. Op haar buik heeft zij een grote pleister zitten. De wond loopt vanaf haar schaambeen tot boven haar navel.
De grootte van de tumorrest na debulking is bepalend voor de overleving. De gynaecologisch oncoloog schat daarom vooraf zo goed mogelijk de operabiliteit van de ziekte in. Dit is onder andere afhankelijk van de lokalisaties, de uitgebreidheid, doorgroei in andere organen en of er uitzaaiingen zijn in longen of lever. Als in eerste instantie een complete/optimale debulking (primaire debulking) niet haalbaar lijkt, dan komt dat in het multidisciplinair overleg aan de orde. In samenspraak met de internist-oncoloog en radioloog wordt dan besloten of het verstandig is eerst chemotherapie te geven. Als de chemotherapie ervoor zorgt dat het aantal tumoren afneemt en ze bovendien kleiner worden, dan stijgt daarmee de kans op een complete of optimale debulking.
De resultaten van grote internationale studies waarin opereren gevolgd door zes kuren chemotherapie vergeleken worden met de behandeling door drie kuren chemotherapie, opereren en nog eens drie kuren chemotherapie bij vrouwen met stadium IIIC/IV, laten geen verschil zien in overleving. Wel blijkt dat de operatie korter duurt en er minder complicaties voorkomen na de operatie van vrouwen die chemotherapie kregen voorafgaand aan een operatie. Het nadeel is dat de operatie wordt uitgesteld. Als ingeschat wordt dat een complete primaire debulking vooraf goed mogelijk is, dan heeft dat toch de voorkeur.
Bij een complete debulking worden de baarmoeder, beide eierstokken, het vetschort en alle zichtbare tumorlokalisaties verwijderd. Is dat niet mogelijk, dan streeft de chirurg een optimale debulking na. Dat betekent dat alle tumorlokalisaties worden teruggebracht tot 1 cm of minder. Als dat niet haalbaar blijkt, dan verwijdert de chirurg zo veel mogelijk tumorweefsel.
Debulking kan dus kort samengevat drie resultaten hebben:
- complete debulking = macroscopisch (met het blote oog) geen zichtbare tumorrest
- optimale debulking = alle tumorresten ≤ 1cm
- incomplete debulking = tumorrest(en) > 1 cm.
Complicaties bij en gevolgen van debulking
Als de ziekte zich uitbreidt in de buik, dan is er kans op een stoma van de darm om tot een optimale/complete debulking te komen. Ook kunnen darmlissen aan de tumor vastzitten, waardoor een stuk darm moet worden verwijderd of een stoma moet worden aangelegd.
Andere problemen die kunnen voorkomen, zijn:
- infecties van de wond, blaas of longen
- bloedingen tijdens of na de operatie
- darmproblemen, geen peristaltiek (ileus)
- letsels aan de blaas, urinewegen of darm.
De risico’s zijn niet groot. Ze worden wel groter als iemand overgewicht heeft, in slechte conditie is (lage performance score) of lijdt aan diabetes. Ook het gebruik van bloedverdunners en verklevingen tussen de darmen leveren nog weleens problemen op. Die verklevingen kunnen zijn ontstaan door de uitgebreidheid van de ziekte, na eerdere buikoperaties of vroegere infecties in de buik.
Goed nieuws na de operatie
De gynaecoloog vertelt na de operatie dat deze goed is gelukt; er bleken nog kleine nestjes met kankercellen tegen haar middenrif aan te zitten, maar ook deze zijn allemaal verwijderd. Dat is voorlopig het beste nieuws waar ze op hoopte. De definitieve uitslag krijgen ze een week later, na het weefselonderzoek door de patholoog en de multidisciplinaire bespreking. Alle zichtbare kanker is verwijderd en de chemotherapie heeft duidelijk effecten laten zien op de tumoren in de buik. Anna zal enkele weken na de operatie opnieuw beginnen met chemotherapie. Daar ziet ze erg tegen op. Ze is nu nog zo moe van de operatie en het eten valt niet altijd even goed. Haar pruik kriebelt vreselijk nu het warmer weer is geworden. Daarom besluit ze vaker een sjaaltje te dragen. Gelukkig maakt het goede nieuws van de operatie veel goed.
Chemotherapie
De medicijnen die gebruikt worden voor de behandeling van kanker worden chemotherapie of cytostatica genoemd. De cytostatica worden via de bloedbaan door het gehele lichaam verspreid en bereiken de kankercellen overal. De werking van deze medicijnen is meestal gebaseerd op het ingrijpen op de processen die in een lichaamscel nodig zijn voor de celdeling en celontwikkeling. Hierbij worden vooral snelgroeiende cellen zoals kankercellen beschadigd maar er zijn ook
effecten op gezonde lichaamscellen. Aangezien de tumorcellen gekenmerkt worden door een versnelde celdeling, vaak in combinatie met een beschadigd celreparatie-mechanisme, zijn ze een stuk gevoeliger voor de cytostatica dan gezonde cellen. De dode kankercellen worden afgebroken waarna het lichaam ze verwijdert.
Er zijn verschillende soorten cytostatica en kankercellen kunnen verschillen in de gevoeligheid voor de diverse cytostatica. Om een optimaal resultaat te bereiken, wordt er voor een combinatie van verschillende medicijnen gekozen. Deze medicijnen kunnen elkaar aanvullen en versterken. Na een bepaalde tijd (meestal drie weken) wordt de chemokuur herhaald.
De standaardchemotherapie bij eierstokkanker bestaat uit een combinatie van twee soorten cytostatica, meestal paclitaxel en carboplatin, eens per drie weken toegediend. Andere platinum bevattende combinaties of doseringsschema’s zoals wekelijkse kuren met paclitaxel en carboplatin zijn ook mogelijk. De chemotherapie wordt via een infuus gegeven en de behandeling is meestal poliklinisch. Het is belangrijk dat een verpleegkundige of arts je voor het begin van de kuur goed informeert over de toediening en de bijwerkingen van de chemotherapie en allerlei praktische zaken daaromheen.
Voordat het infuus wordt aangelegd krijg je premedicatie (extra medicijnen zoals granisetron en dexamethason) om allergische reacties te voorkomen en om misselijkheid en braken tegen te gaan. Vlak voor elke volgende chemokuur wordt bloed afgenomen, om te bekijken of het bloedbeeld goed hersteld is na de laatste kuur. Als de hoeveelheid witte bloedcellen (leukocyten en granulocyten) en/of de hoeveelheid bloedplaatjes (trombocyten) te laag zijn, wordt de kuur uitgesteld of de dosering aangepast.
Aan het eind van de behandeling wordt de reactie van de tumor op de totale behandeling bepaald. Dit gebeurt door gynaecologisch onderzoek, een vaginale echografie, bloedonderzoek en soms een CT- scan.
Platinum
De ontdekking van cytostatica op basis van platina begint in 1961. De biofysicus Rosenberg is gefascineerd door de patronen van chromosomen in delende zoogdiercellen, ze doen denken aan een magnetisch veld. Hij besluit de invloed van een elektromagnetisch veld op de celgroei van bacteriën na te gaan, hiervoor gebruikt hij platinumelektroden. Wat er dan gebeurt, is erg verrassend. Zodra de stroom aan staat houden de bacteriën op zich te vermenigvuldigen; wel groeien ze door tot heel grote cellen. Zodra de elektromagneet uit staat, vermenigvuldigden de bacteriën zich weer. De celdeling stopte door bepaalde platinaverbindingen (cis-dichlorodiamineplatinum), die ontstonden onder invloed van elektrische stroom uit de platina-elektroden in de ammoniumchloride (NH4Cl)-oplossing of onder invloed van fotosynthese uit zonlicht. De eerste klinische studies bij kankerpatiënten werden in 1972 gedaan. Hoewel zeker in de beginjaren
de bijwerkingen van cisplatin aanzienlijk waren, was het effect op kanker ook zodanig baanbrekend dat cisplatin een zeer belangrijk middel is voor de behandeling van diverse vormen van kanker. Vooral tumoren aan hoofd en hals en die aan de geslachtsorganen blijken zeer gevoelig voor cisplatin. In later jaren werd het aan cisplatin verwante carboplatin ontwikkeld, dat veel minder bijwerkingen heeft en bij eierstokkanker hetzelfde effect geeft als cisplatin.
Bijwerkingen van de chemotherapie
Chemotherapie zorgt voor een verminderde aanmaak van rode bloedcellen (dit geeft bloedarmoede en vermoeidheid), verminderde aanmaak van witte bloedcellen (verhoogde vatbaarheid voor infecties) en een verminderde aanmaak van bloedplaatjes (verhoogde kans op bloedingen). Het is daarom belangrijk dat je alert bent op verschijnselen als koorts, koude rillingen, bloedingen enzovoorts.
- Misselijkheid en braken zijn goed te voorkomen door of worden behandeld met medicijnen tegen misselijkheid en braken.
- De medicijnen tegen misselijkheid en braken kunnen obstipatie veroorzaken, waardoor na enkele dagen juist misselijkheid kan ontstaan. Het is belangrijk zo nodig laxeermiddelen te gebruiken.
- Door de chemotherapie kan de smaak veranderen, waardoor je sommige voedingsmiddelen opeens heel vies vindt.
- Chemotherapie kan irritatie veroorzaken van de slijmvliezen, wat kan leiden tot een pijnlijke mond en soms diarree. Meestal is dit van korte duur. Goede mondhygiëne en regelmatig drinken kan de beschadiging van de mondslijmvliezen (gedeeltelijk) voorkomen. Vaak helpt het, als u uw mond 4 tot 6 maal per dag spoelt met zout water (9 gram zout op 1 liter gekookt water), met afgekoelde kamillethee of met gewoon water.
- Gebruik een zachte tandenborstel en vet regelmatig je lippen in met witte vaseline, dan ontstaan er minder snel kloofjes.
- Beschadiging van de zenuwbanen kan zich uiten in prikkelingen en/of een doof en stijf gevoel in handen en voeten (neuropathie).
- Soms heb je last van pijn of spierkrampen. Over het algemeen worden de klachten enige tijd na het stoppen van de behandeling minder en soms verdwijnen ze. Een deel van de klachten kan echter blijvend van aard zijn.
- Allergische reacties tijdens de inloop van de chemotherapie kunnen zich op verschillende manieren uiten. Niesbuien, neusverstopping, benauwdheid, bloeddrukschommelingen, heftige pijn in de rug of op de borst, misselijkheid, braken, buikklachten of aandrang tot ontlasting, jeuk of roodheid van de huid kunnen zich plotseling voordoen. Waarschuw direct de verpleegkundige van de dagbehandeling.
- Haaruitval ontstaat door paclitaxel en begint meestal de tweede week na de eerste kuur. Soms gaat dat gepaard met een soort haarpijn. Die is van voorbijgaande aard.
- Spierpijn en gewrichtspijn komen vaak een paar dagen na de kuur voor, met name door paclitaxel.
Follow-up
Als de behandeling is afgerond volgt er een controletraject. De frequentie van controleafspraken ziet er meestal als volgt uit:
- In het eerste en tweede jaar elke drie maanden een controleafspraak
- In het derde jaar elke vier maanden
- In het vierde en vijfde jaar elke zes maanden
- Na het vijfde jaar eenmaal per jaar.
Bij de controle wordt lichamelijk en gynaecologisch onderzoek gedaan. Het onderzoek kan aangevuld worden met een vaginale (en/of abdominale) echografie. Als je klachten hebt, kan de specialist besluiten het gehalte CA-125 in je bloed te bepalen. Dat gebeurt ook bij verdenking op een recidief (de ziekte is teruggekomen). Afhankelijk van de bevindingen kan er een reden zijn om het onderzoek verder uit te breiden met een CT-scan.
Er is in een onderzoek aangetoond dat het standaard vervolgen van de tumormarker CA-125 geen effect heeft op de overleving. Wel bleek dat de kwaliteit van leven van patiënten bij wie het CA-125 bekend was slechter was, omdat ze eerder dan de andere groep er weet van hadden dat de ziekte actief was, zonder dat de CT-scan dat dan al aantoonde. Alleen bij bewezen ziekteactiviteit op een CT-scan is er een indicatie om te behandelen. De bevindingen van dit onderzoek hebben ertoe geleid dat alleen op indicatie (klachten of afwijkende bevindingen bij lichamelijk en gynaecologisch onderzoek) een CA-125 wordt bepaald.
Behalve het opsporen van een mogelijk recidief heeft de controle nog andere doeleinden. Je kunt last hebben van bijwerkingen van de behandeling. De behandeling van eierstokkanker heeft ook psychosociale gevolgen en kan verandering geven op het gebied van seksualiteit. Het is belangrijk om hierover te praten met je behandelend arts, zodat die je kan helpen of je kan doorverwijzen naar andere zorgverleners. Je kunt hiervoor ook terecht bij de oncologieverpleegkundige die deel uitmaakt van het nazorgteam.
Ontwikkelingen in chemotherapie
Soms wordt een derde middel toegevoegd met een ander werkingsmechanisme. In een grote studie met 1500 patiënten is echter gebleken dat zo’n schema de overlevingskansen niet vergroot. Er zijn ook onderzoeken met andere, meer gerichte middelen, zoals bevacizumab (Avastin). Dat werkt tegen de ontwikkeling van nieuwe bloedvaten die kankercellen maken om aan zuurstof en voeding te komen en wordt daarom een angiogeneseremmer genoemd.
Angiogeneseremmers zijn antilichamen die binden aan de vasculaire endotheliale groeifactor (VEGF). Deze groeifactor wordt in grote hoeveelheden door eierstokkankercellen gemaakt en stimuleert de
vorming van nieuwe bloedvaten in en rondom de tumor. Bevacizumab als toevoeging aan de chemotherapie is geregistreerd voor eierstokkanker stadium III met een resterende tumor van meer dan 1 cm na operatie en voor eierstokkanker stadium IV. Het nadeel van dit middel is dat patiënten het langdurig (één jaar) moeten krijgen omdat het geen zin heeft het slechts een korte periode te gebruiken.
Bovendien geeft bevacizumab extra bijwerkingen. Het lijkt erop dat slechts een klein deel van de patiënten er overlevingsvoordeel bij kan hebben. Mede daardoor wordt het in Europa lang niet overal gebruikt.
Ander toedieningsschema
Soms worden de chemokuren met paclitaxel en carboplatin wekelijks gegeven in aangepaste dosis. In een Japanse studie pakte deze wekelijkse toediening van paclitaxel beter uit dan de gebruikelijke driewekelijkse toediening. De vrouwen die deze therapie kregen, leefden gemiddeld enkele maanden langer. Deze resultaten konden in de Europese en Amerikaanse studies niet worden bevestigd.
Intraperitoneale chemotherapie
Intraperitoneale chemotherapie betekent dat een of meer cytostatica via een chirurgisch ingebracht flexibel buisje (katheter) in de buikholte wordt gebracht, naast de chemotherapie via het infuus. Het idee is dat er maximaal aanbod is van chemotherapie op de plaats van ziekte. Uit wetenschappelijk onderzoek bleek dat fitte patiënten bij wie weinig tot geen overblijfselen van de ziekte te vinden zijn na de operatie, overlevingswinst kunnen halen uit deze behandeling. Toch is het een onderwerp van discussie gebleven en geen wijdverbreide standaardtherapie in Europa omdat er ook veel kanttekeningen bij te plaatsen zijn. De behandeling geeft extra bijwerkingen, een deel van de patiënten ondervond problemen met de katheter en meer dan de helft van de patiënten kon de behandeling met intraperitoneale chemotherapie niet afmaken, onder andere vanwege complicaties. De kwaliteit van leven was tijdens deze behandeling bovendien slechter.
Ten slotte komt de chemotherapie via deze methode niet overal in de buik. Toch zijn de eerste resultaten veelbelovend. Het wachten is op de resultaten van meer onderzoek naar deze therapie.
Hypertherme intraperitoneale chemotherapie (HIPEC)
Hypertherme intraperitoneale chemotherapie is een andere manier om chemotherapie via de buik toe te dienen. Dit gebeurt eenmalig tijdens de operatie. Met deze methode is ervaring opgedaan bij andere ziekten, met name darmkanker. Momenteel wordt in een wetenschappelijk onderzoek (OVHIPEC-studie) onderzocht of het zinvol is deze behandeling te gebruiken bij eierstokkanker.
Wetenschappelijk onderzoek
Steeds probeert men om de behandeling en overleving van eierstokkanker te verbeteren. De manier om erachter te komen of een nieuwe behandeling beter is dan de huidige standaardbehandeling is het doen van wetenschappelijk onderzoek. Bij vrouwen met eierstokkanker die vrijwillig deelnemen aan zo’n onderzoek wordt door loting bepaald of ze de nieuwe behandeling of de standaardbehandeling zullen krijgen. Aan het einde van de studie wordt vervolgens gekeken welke behandeling beter is geweest. Overigens zijn er verschillende vormen en fasen van wetenschappelijk onderzoek mogelijk.
Het kan dus zijn dat je de vraag krijgt om mee te doen aan vergelijkend onderzoek. Het onderzoek begint pas nadat je uitvoerige mondelinge en schriftelijke informatie hebt gekregen en je schriftelijk toestemming hebt gegeven voor deelname.
Samenvatting
De behandeling van laag stadium eierstokkanker begint met een operatie. De volledigheid van de stadiëring is de belangrijkste voorspellende waarde voor overleving en het terugkomen van de ziekte. De vijfjaarsoverleving bij laag stadium eierstokkanker is hoog.
Bij hoog stadium eierstokkanker is de grootte van de tumorrest na debulking bepalend voor de overleving. Of operatie mogelijk is, is onder andere afhankelijk van de lokalisaties, de uitgebreidheid, de doorgroei in andere organen en of er uitzaaiingen zijn in longen of lever. Als in eerste instantie een volledige debulking (primaire debulking) niet haalbaar lijkt, komt dat in het multidisciplinair overleg aan de orde. De gynaecoloog-oncoloog, internist-oncoloog en radioloog besluiten dan of het verstandig is eerst chemotherapie te geven. Als de chemotherapie ervoor zorgt dat de tumoren kleiner worden en ook hun aantal afneemt, dan stijgt daarmee de kans op een volledige debulking en daarmee de overleving. Bij de behandeling van hoog stadium eierstokkanker hoort ook een behandeling met chemotherapie. Die vindt plaats na de operatie, of als sandwichtherapie met drie chemokuren voor en drie chemokuren na de operatie. Als de behandeling is afgerond vinden elke drie maanden controles plaats.
Wat als de kanker terugkomt?
Het gebeurt dat de kanker na de succesvolle eerste behandeling toch terugkomt. Dit hoofdstuk gaat in op de behandelmogelijkheden en het perspectief. Vaak is genezing niet meer mogelijk en staat de kwaliteit van leven voorop.
Eierstokkanker kan terugkomen (recidief); hoe hoger het FIGO-stadium hoe groter de kans hierop. Genezing is dan niet meer mogelijk. Meestal wordt een recidief binnen twee jaar ontdekt. De uitgebreidheid van de ziekte en de compleetheid van de eerdere operatie zijn het meest bepalend voor het risico op terugkeer van de ziekte. Welke behandelingen vervolgens zinvol en mogelijk zijn, is afhankelijk van het type eierstokkanker, het tijdstip van terugkeer van de ziekte ten opzichte van het einde van de eerdere behandeling en de plekken waar het zit. Andere factoren die van belang zijn: is er sprake van BRCA1- of BRCA2-gendragerschap, welke eerdere chemotherapie heeft iemand gekregen en hoe was de eerdere reactie hierop? Ook de algemene gezondheidstoestand speelt mee, evenals de bijwerkingen die zijn overgebleven van de eerdere behandeling. Ten slotte staat bij de keuze voor behandeling de kwaliteit van leven voorop. Dat wil zeggen dat behandelingen met vervelende bijwerkingen beperkt moeten worden.
Het gaat er in dit stadium vooral om de symptomen van de ziekte te bestrijden.
Platinum-gevoelig recidief
De behandelmogelijkheden van een teruggekeerde eierstokkanker hangen onder andere af van de tijd die er is verstreken sinds de laatste chemokuur die platinum (carboplatin of cisplatin) bevatte
Eierstokkanker wordt als platinum-gevoelig (platinum-sensitief) beschouwd als het recidief optreedt vanaf zes maanden na de laatste kuur chemotherapie met carboplatin (of cisplatin). Deze patiënten zullen zeer waarschijnlijk opnieuw op platinum bevattende chemotherapie (carboplatin of cisplatin) reageren. Hoe later het recidief optreedt, hoe groter de kans is op een goede reactie op chemotherapie. De combinatie van carboplatin en paclitaxel (elke drie weken) heeft vaak de voorkeur. Andere combinaties zijn ook mogelijk, dat is afhankelijk van de nog bestaande en de verwachte bijwerkingen. De combinatie van carboplatin en gepegyleerde liposomale doxorubicine (Caelyx) veroorzaakt bijvoorbeeld minder neuropathie en is even effectief bij platinum-sensitieve eierstokkanker. De combinatie van carboplatin met gemcitabine is ook geschikt, maar geeft meer bijwerkingen op het beenmerg, waardoor kuren vaker uitgesteld moeten worden.
Soms wordt de chemotherapie gecombineerd met bevacizumab (Avastin). Door de chemotherapie te combineren met bevacizumab zou de kanker wat langer onderdrukt blijven, maar tot nu toe is niet aangetoond dat patiënten ook langer leven. Het nadeel van
bevacizumab is dat het ook na het einde van de chemokuren eens per drie weken als infuus in het ziekenhuis moet worden toegediend en het kan onder andere een hoge bloeddruk veroorzaken, waarvoor behandeling met bloeddrukmedicijnen nodig is.
De rol van chirurgie
Een belangrijke vraag van veel vrouwen met recidief ziekte is of opnieuw een operatie zinvol is. Er zijn onvoldoende gegevens of een tweede operatie gevolgd door chemotherapie bijdraagt aan de overleving. Wel of niet opnieuw opereren blijft een discussiepunt.
Opnieuw opereren is te overwegen als de ziekte na minimaal zes maanden of meer terugkomt als er na de eerste behandeling geen ziekte meer is aangetoond (complete remissie) en als bij het recidief een optimale en het liefst een complete debulking haalbaar is.
Andere voorwaarden voor opnieuw opereren zijn dat de vrouw in goede conditie is (performance status), bij de eerste behandeling een volledige debulking heeft ondergaan, weinig of geen vocht in haar buik heeft en het aantal tumoren beperkt is.
Mogelijkheden van chemotherapie als de ziekte snel terugkeert
De ziekte wordt beschouwd als platinum-ongevoelig (platinum refractair) als de tumor tijdens de chemotherapiebehandeling of binnen vier weken na de laatste dosis verder groeit. Er is dan geen verdere standaardbehandeling beschikbaar. Soms bestaat de mogelijkheid van studiebehandelingen met nieuwe medicijnen, waaraan patiënten kunnen deelnemen.
Als het recidief zich binnen een halfjaar na de laatste dosis voordoet, dan wordt de ziekte weinig platinum-gevoelig (platinum- resistent) genoemd. Ook nu is de situatie niet zo gunstig, maar er zijn nog wel mogelijkheden van behandeling met chemotherapie al is er internationaal geen eenduidige standaardbehandeling gedefinieerd. De keuze wordt meestal individueel bepaald. Meer nog dan in een eerder stadium van de ziekte en behandeling staat de kwaliteit van leven voorop en worden bijwerkingen van behandeling zoveel mogelijk vermeden. Er is veel aandacht voor behandeling van de klachten (symptoomverlichting).
Cytostatica die gebruikt kunnen worden zijn paclitaxel, topotecan, gepegyleerde liposomale doxorubicine (Caelyx) en gemcitabine. De kans dat dat korte tijd helpt (twee tot vier maanden) ligt tussen 10 en 30 procent. Er zijn ook gegevens beschikbaar van wekelijkse chemokuren met paclitaxel en carboplatin die in deze situatie nog effectief kunnen zijn. De responskans hiervan is 50 procent; de effectduur is gemiddeld zes tot acht maanden. De gedachte hierachter is dat door zo’n intensief schema kankercellen weer gevoeliger worden voor de chemotherapie. Deze wekelijkse kuren paclitaxel en carboplatin worden veel in Nederland, België, Groot-Brittannië en Spanje toegepast. Met het oog op de bijwerkingen is het belangrijk dat de patiënte en behandelend arts erover praten of ze deze behandeling nog de moeite waard vinden. Een andere tegenwoordig veelgebruikte combinatie van medicijnen is wekelijks toegediend paclitaxel met bevacizumab die één keer per drie weken wordt toegediend. Het is gebleken dat de toevoeging van bevacizumab aan de chemotherapie effectiever werkt tegen de kanker dan deze chemotherapie alleen en dat de bijwerkingen acceptabel zijn. Er zijn wel een paar voorwaarden verbonden aan deze combinatiebehandeling met bevacizumab. Alleen patiënten die maximaal twee series chemotherapie hebben ondergaan zonder bevacizumab komen ervoor in aanmerking.
Bij de behandeling van teruggekeerde eierstokkanker wordt soms lokale bestraling gebruikt om bijvoorbeeld pijnklachten te verminderen of bloedingen te stelpen.
Behandeling met hormonale therapie wordt alleen in bijzondere gevallen toegepast en heeft geen uitgesproken plaats bij de behandeling van eierstokkanker.
BRCA1- en BRCA2-dragerschap
Voor de behandeling van teruggekeerde eierstokkanker die gerelateerd is aan een BRCA1- of BRCA2-genmutatie, wordt olaparib (Lynparza) gebruikt. Dit medicijn hoort tot de groep van de zogenoemde PARP- remmers. PARP is een eiwit (enzym) in de lichaamscellen dat betrokken is bij de reparatie van DNA-schade. Door dit eiwit PARP te remmen, kan de lichaamscel DNA-beschadigingen niet goed repareren en kan de cel doodgaan. Dat is uiteraard gunstig als het om een kankercel gaat. Nu is het zo dat BRCA1- en BRCA2-gerelateerde eierstokkankercellen erg gevoelig kunnen zijn voor PARP-remmers. Uit klinisch onderzoek blijkt dat vrouwen met BRCA1- en BRCA2-gerelateerd recidief eierstokkanker bij gebruik van olaparib als onderhoudsbehandeling na behandeling met chemotherapie gemiddeld zeven maanden langer geen groei van de ziekte hadden. Er zijn tot nu toe wel strikte voorwaarden verbonden aan de registratie en toediening van olaparib (zie kader op blz. 66).
Momenteel zijn er diverse klinische studies met PARP-remmers gaande, dus de indicatie en registratie van deze en andere PARP-remmers zou kunnen veranderen. Nu wordt het nog met name als onderhoudsbehandeling na de chemotherapie gegeven, maar wellicht dat er combinaties van PARP-remmers met andere medicijnen, zoals de angiogeneseremmers, beschikbaar komen.
PARP is een enzym dat breuken in een DNA-streng repareert, via het base excision repair-systeem, zodat de cel verder kan groeien. Indien PARP wordt geremd, dan wordt de breuk niet gerepareerd. Indien ook een ander mechanisme, het homologe recombinatie reparatiemechanisme, om DNA-breuken te repareren ontbreekt, zoals in BRCA1- en BRCA2-kankercellen het geval is, dan kunnen DNA- breuken niet meer gerepareerd worden en gaat de (kanker)cel dood. Schematisch valt dit het beste uit te leggen aan de hand van figuur 13.

Figuur 13. Een tafel heeft vier poten waarbij elke poot een DNA-reparatiemechanisme voorstelt. Als een van deze poten wordt omgezaagd (remmer van enzym PARP, dus geen reparatie van DNA-breuken d.m.v. base excision repair) is er nog niets aan de hand. Als er twee poten ontbreken, valt de tafel om.
Andere subtypes eierstokkanker
Als de patholoog onder de microscoop de eierstokkankercellen bekijkt, dan is een aantal subtypes te onderscheiden. Die kenmerken zich ook verder doordat ze verschillende mutaties en andere veranderingen in hun DNA kunnen hebben.
Een van de subtypen is laaggradig sereus eierstokkanker. Voor deze groep vinden momenteel klinische studies plaats met een zogenoemde MEK-remmer. Daardoor wordt een eiwit (mitogen- activated protein kinase) in de kankercel geremd dat betrokken is bij de groei en vermenigvuldiging van deze kankercellen. Helaas laten de eerste resultaten nog geen meerwaarde of verbetering in behandeling zien. Ook andere middelen voor de verschillende subtypes van eierstokkanker worden nu of later in internationaal studieverband onderzocht in de hoop in de toekomst beter en/of langer effect op behandeling te krijgen.
Historisch perspectief en ontwikkelingen
De nieuwe ontwikkelingen op het gebied van de behandeling van eierstokkanker gaan helaas nooit snel genoeg, maar langzaamaan worden wel verbeteringen zichtbaar. Alle verbeteringen zijn tot nu toe mogelijk gemaakt door multidisciplinaire samenwerking in de ziekenhuizen, zowel regionaal, landelijk als internationaal. Alleen door deze samenwerking en de medewerking van patiënten kunnen goede klinische studies worden verricht. In dertig jaar hebben betere chirurgie, ontwikkelingen in de chemotherapie en gerichte therapie de prognose van de patiënten met eierstokkanker verbeterd naar een vijfjaarsoverleving van 35 procent. Door het vervangen van cisplatin door carboplatin is de kwaliteit van leven met het oog op bijwerkingen ook verbeterd.
Huidig en toekomstig onderzoek richt zich onder andere op geïndividualiseerde behandelingen, gericht tegen bepaalde mutaties en groeifactoren in de kankercel.
Een andere ontwikkeling is immunotherapie. Daarmee worden de eigen afweercellen sterker geactiveerd en richten zich op die manier meer tegen de kankercellen. Dit is bij enkele andere soorten kanker al effectief gebleken.
Bij platinum-resistent recidief eierstokkanker wordt ook steeds nog verder gekeken naar het voordeel van intensievere of wekelijkse behandelingen met chemotherapie, al of niet in combinatie met gerichte therapie zoals angiogeneseremmers.
Ten slotte gaat er ook veel aandacht uit naar het verminderen van bijwerkingen bij de behandeling van eierstokkanker en het verbeteren van de zorg voor ouderen met eierstokkanker.
Samenvatting
De meeste patiënten met hoog stadium eierstokkanker hebben een goed resultaat op de primaire behandeling, maar velen krijgen een recidief (70 procent). Bij het recidief staat kwaliteit van leven voorop.
Platinum-sensitief recidief dat na meer dan zes maanden optreedt, wordt standaard behandeld met (opnieuw) platinum bevattende chemotherapie.
Patiënten met een platinum-resistent recidief worden vaak behandeld met chemotherapie in combinatie met bevacizumab (Avastin) of met wekelijkse kuren paclitaxel en carboplatin. Een ander middel is onder andere gepegyleerde liposomale doxorubicine (Caelyx).
Bij een platinum-gevoelig recidief bij een vrouw met een BRCA1- of BRCA2-genmutatie is onder voorwaarden na behandeling met chemotherapie een onderhoudsbehandeling met olaparib (Lynparza) mogelijk.
Leven met eierstokkanker
Het hebben van eierstokkanker heeft invloed op veel aspecten van jezelf en van je leven. Als een wervelwind raast de ziekte door je bestaan. Het brengt je aan het wankelen en zet je tevens met beide benen op de grond.
Leven met kanker is niet vanzelfsprekend. De tijdlijn die in beeld is gebracht door Stichting Olijf (figuur 14) laat zien hoe vrouwen vanaf de diagnose tot aan de gevolgen op lange termijn worstelen met gynaecologische kanker en alles wat daarmee samenhangt. De tijdlijn maakt inzichtelijk hoe kanker je leven op zijn kop zet en hoe je er samen met anderen iets aan kunt doen.
Er is geen eenduidig antwoord te geven op de vraag hoe je met kanker moet omgaan. Ook al heb je hetzelfde type kanker, elke situatie is anders en iedere persoon is anders. De diagnose kanker brengt grote veranderingen met zich mee, zowel op fysiek, psychisch als sociaal gebied door onder andere fysieke klachten, ingrijpende behandelingen en onzekerheid over de toekomst.
Wat de tijdlijn ook laat zien, is dat tijdens de behandeling en in de eerste periode na de behandeling vooral de fysieke klachten centraal staan en pas daarna de psychische en sociale problemen op de voorgrond komen te staan. Veelal realiseer je je pas na de behandeling hoe de kanker je leven beïnvloedt.
Na een oncologische behandeling heeft meer dan 50 procent van de kankerpatiënten volgens de richtlijn Oncologische revalidatie langdurig fysieke, sociale of psychische problemen. Tot de fysieke problemen behoren lichamelijke klachten als pijn en vermoeidheid. Veel patiënten zijn ook beperkt in hun dagelijkse activiteiten en ondervinden problemen bij hun persoonlijke verzorging. Angst, depressie en een veranderd zelfbeeld zijn voorbeelden van problemen die op psychisch gebied voorkomen. Sociale problemen hebben onder andere betrekking op veranderingen in persoonlijke relaties. Vaak is het moeilijker om aan sociale activiteiten deel te nemen of om te werken.

Figuur 14. Tijdlijn ‘leven met kanker’ (bron: Stichting Olijf).
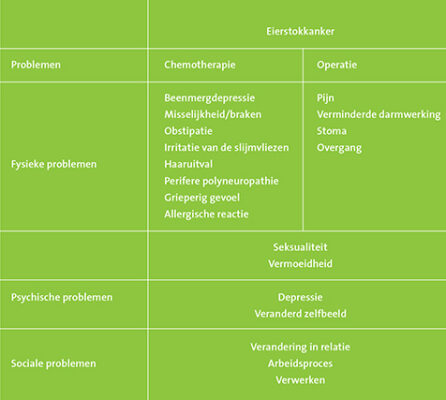
Tabel 1. Overzicht problemen voorkomend na behandeling voor eierstokkanker.
Fysieke problemen bij chemotherapie
Misselijk en moe
Anna is, omdat er sprake is van eierstokkanker FIGO-stadium IIIC, haar behandeling begonnen met drie kuren chemotherapie. Zij heeft de standaard combinatiechemotherapie gekregen met paclitaxel en carboplatin. De bijwerkingen die Anna ondervindt bij de kuren zijn wisselend. Na de eerste kuur gaat het de eerste dagen goed. Daarna is ze misselijk. Ze krijgt extra medicijnen voorgeschreven die de misselijkheid verlichten en laxeermiddelen, omdat de ontlasting kort na de kuur moeizaam verliep. Ook krijgt ze na een paar dagen last van spierpijn. Met het innemen van paracetamol is dat gelukkig snel onder controle. Anna is blij dat ze de eerste kuren zo goed doorstaan heeft. Om die reden twijfelt ze aan de werking ervan.
Na de derde kuur komt Anna samen met Jeroen op de polikliniek voor controle. Ze klaagt dat ze heel erg moe is. Uit bloedonderzoek blijkt dat haar hemoglobinegehalte (Hb) laag is. De internist-oncoloog legt uit dat de chemotherapie de aanmaak van de rode bloedcellen (erytrocyten) vermindert en dat daardoor de bloedarmoede (anemie) is ontstaan. Vermoeidheid is daar een symptoom van.
Na het bezoek aan de arts spreekt Anna de oncologieverpleegkundige uitgebreid. Samen nemen ze de periode van de behandeling met chemotherapie door. Anna vertelt hoe vreselijk ze het vindt dat ze haar haar kwijt is. Ze is blij dat ze zich al voor de eerste kuur chemotherapie een pruik heeft laten aanmeten. Toen de haaruitval in de tweede week van de eerste kuur begon, was ze hierop voorbereid.
Beenmergdepresssie
Door de chemotherapie kan de aanmaak van nieuwe bloedcellen (figuur15) in het beenmerg verminderen. Dat heet beenmergdepressie. Hierdoor kunnen anemie, leukopenie en trombocytopenie ontstaan. Leukopenie is een tekort aan witte bloedcellen (leukocyten). Deze cellen zorgen voor afweer tegen infecties. Door een tekort groeit het risico op infecties. Bacteriën en virussen die normaal weinig gevaar opleveren, kunnen nu heftige reacties veroorzaken met hoge koorts. Bij de combinatiechemotherapie met paclitaxel en carboplatin is er tussen de tiende en de vijftiende dag van de kuur sprake van een zogenaamde dipperiode. Dit is de periode waarin het aantal witte bloedlichaampjes lager is. Dan is het infectierisico het hoogst. Gelukkig gaat het meestal goed en treedt er geen infectie op.
Als er sprake is van een tekort aan bloedplaatjes (trombocyten) spreken we van trombocytopenie. De bloedplaatjes spelen een belangrijke rol bij de bloedstolling. Het gevolg van een daling van het aantal van deze cellen is dat het bloed minder snel stolt. Pas als de waarde van de bloedplaatjes heel erg laag is, wordt dit gevaarlijk en is
er reden voor toediening van bloedplaatjes. Dit komt weinig voor bij de kuren met paclitaxel en carboplatin.
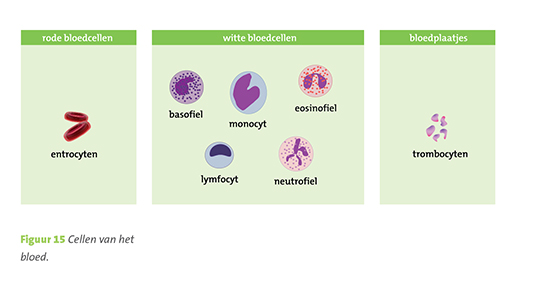
Figuur 15. Cellen van het bloed.
Misselijkheid en braken
Er zijn vrouwen die binnen 24 uur na een chemokuur last hebben van misselijkheid en/of braken. Bij anderen gebeurt dat soms later. Dat heeft te maken met de dosering van de middelen, maar ook leeftijd, gevoeligheid voor misselijkheid, obstipatie, angst, spanning en een slechte ervaring met chemotherapie kunnen een rol spelen.
Bij de start van de chemokuur krijg je medicijnen tegen misselijkheid en braken via het infuus toegediend. En voor de periode tussen de kuren in krijg je medicijnen mee in de vorm van een tablet of zetpil om zo nodig te gebruiken. Een andere tip om deze klachten te verminderen is over de dag kleine beetjes te eten en regelmatig iets te drinken. Zo blijft de maag steeds iets gevuld. Een lege maag kan soms de misselijkheid verergeren.
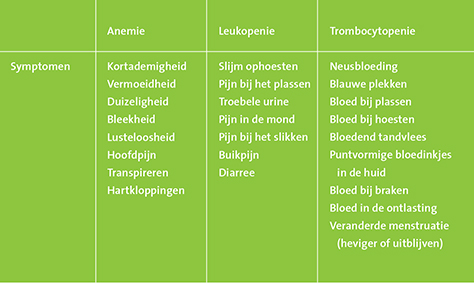
Tabel 2. Klachten als gevolg van beenmergdepressie.
Obstipatie
Het is van groot belang dat je zorgt voor een regelmatige stoelgang. Een van de medicijnen tegen misselijkheid die je voor toediening van de chemotherapie via het infuus krijgt (granisetron of ondansetron), kan obstipatie veroorzaken. Daarom is het advies om rond de chemotherapie zorg te dragen voor een makkelijke stoelgang, Dat doe je het liefst met vezelrijke voeding (bruin brood, groenten) en pruimen of, als het niet anders kan, met behulp van laxeermiddelen, zoals magnesium, macrogol of lactulose. Ook is het heel belangrijk om voldoende te blijven drinken (minimaal 1,5 liter per dag).
Irritatie van de slijmvliezen
Door de chemotherapie kan irritatie, beschadiging en ontsteking ontstaan van de slijmvliezen. Als dit in je mond gebeurt:
- heb je last van een droge mond
- kun je gevoelig zijn voor de temperatuur van voeding
- zijn zure of gekruide voedingsmiddelen niet echt lekker
- ontstaat bloedend tandvlees
- krijg je een slechte adem.
Daarom is goede mondverzorging heel belangrijk. Poets vaker dan normaal je tanden met een zachte tandenborstel. Spoel regelmatig de mond met zout water, koude kamillethee of een alcoholvrije chloorhexidinemondspoeling. Houd je lippen vet. Een gebitsprothese kun je ’s nachts het beste uitdoen.
De binnenkant van de darmen is ook bekleed met slijmvlies. Diarree ontstaat als bovenstaande problemen optreden in het darmslijmvlies. Diarree is waterige dunne ontlasting die meer dan vier keer per dag voorkomt. Symptomen zijn buikpijn, buikkrampen en frequente aandrang. Het gevolg van diarree is dat vocht en voedingsstoffen minder goed worden opgenomen. Daarom is het belangrijk om veel te blijven drinken en voedingsmiddelen die prikkelen (zoals citroen en sinaasappelsap) te vermijden.
Haaruitval
Door de behandeling met paclitaxel begint je haar na ongeveer twee weken uit te vallen. Dit kan samengaan met een gevoelige of pijnlijke hoofdhuid, ook wel haarpijn genoemd. Niet alleen het hoofdhaar kan uitvallen, maar ook je lichaamshaar, okselhaar, schaamhaar, wenkbrauwen en wimpers. Tegen het uitvallen van het haar is niet veel te doen. Als je je haar kort knipt, maak je het iets minder confronterend. Als de chemotherapie is gestopt, begint het haar na ongeveer een maand te groeien. Het duurt daarna nog een paar maanden voordat de haargroei goed hersteld is. Ter overbrugging kun je een pruik dragen of als afwisseling een pet, hoed, sjaal of muts.
Wanneer je haar weer aangroeit is het vaak anders van kleur en structuur (krullen). Meestal is dit tijdelijk.
In sommige ziekenhuizen wordt het haarverlies tegengegaan door tijdens de inloop van de chemotherapie de hoofdhuid te koelen (hoofdhuidkoeling). Dit werkt bij een deel van de vrouwen zodanig dat het haar wel dunner wordt, maar er voldoende haar overblijft om geen pruik te hoeven dragen.
TIP
Kijk eens voor ideeën op www.lookgoodfeelbetter.nl.
Via de website van Top Haarwerkers Gilde Nederland kun je zoeken naar betrouwbare haarwerkers en haarstylisten die je kunnen helpen met het kiezen van een goede pruik (www.thgn.nl).
Perifere polyneuropathie
Een andere bijwerking van paclitaxel is (tijdelijke) beschadiging aan de zenuwcellen, met name aan de zenuwuiteinden. Dit wordt perifere polyneuropathie genoemd. Klachten die hierbij optreden, zijn:
- minder gevoel in handen (vingers) en/of voeten
- (tenen) tintelend of verdoofd gevoel in vingertoppen en tenen
- gevoel op watten te lopen door gevoelloosheid in de voeten
- krachtverlies in armen en/of benen
- spier- en gewrichtspijnen
- verlies van de fijne motoriek.
In veel gevallen zijn deze klachten het ergst meteen na de chemokuur. Ook kunnen ze een paar dagen na de behandeling optreden. Als je heel veel last hebt, moet je dat vertellen. Dan wordt gekeken of de behandeling aangepast moet worden. De klachten verdwijnen meestal enige tijd na het stoppen van de behandeling, maar ze kunnen blijvend zijn.
Grieperig gevoel
Algehele malaise, hoofdpijn, koorts, spierpijn en verminderde eetlust kunnen je door de behandeling met chemotherapie een grieperig gevoel geven. Dit houdt meestal één of twee dagen aan en kan bestreden worden met paracetamol.
Allergische reactie
Een allergische reactie treedt op door overgevoeligheid. Zowel carboplatin als paclitaxel kan een allergische reactie geven tijdens de infusie, maar bij toediening van paclitaxel komt dat het meeste voor. De reactie kan direct bij de eerste kuur ontstaan, maar ook pas na een paar kuren. Reacties die optreden zijn vaak roodheid en huiduitslag. Dit kan gepaard gaan met jeuk over het hele lichaam. Ook kuchen en onrust komen vaak als eerste verschijnselen voor.
Verschijnselen die hierna kunnen optreden, zijn:
- beklemmend gevoel op de borst of erge pijn in de rug
- duizeligheid en bloeddrukdaling
- bleek zien
- gezwollen oogleden
- rillen
- misselijkheid en darmkrampen
- kortademigheid.
- aandrang voor ontlasting/urine.
Zodra je een verandering opmerkt is het belangrijk dit direct te melden en daarmee de ernst van de reactie te beperken. Om een allergische reactie te voorkomen, krijg je voor het starten met paclitaxel via het infuus een medicijn toegediend.
Fysieke problemen na operatie
Bij een chirurgische behandeling kun je meteen na de operatie fysieke problemen ervaren. Op langere termijn kun je ook klachten hebben en je moet leren leven met het feit dat je een groot litteken op je buik hebt.
Pijn
Pijn komt vaak voor bij kanker. Van de mensen die actief worden behandeld ervaart 30 procent pijnklachten. Als de ziekte is uitgezaaid loopt dat op tot meer dan 70 procent. Meer dan de helft van de kankerpatiënten wordt door pijn belemmerd in het dagelijks leven.
- Oorzaken van pijn bij kanker
- Pijn als direct gevolg van tumorgroei (die druk uitoefent of doordrukt op een zenuw).
- Pijn als indirect gevolg van tumorgroei (bijv. door afsluiting van bloedvaten).
- Pijn als gevolg van de behandeling van de tumor
- na chirurgische behandeling (litteken- of fantoompijn)
- na radiotherapie (beschadiging van de huid)
- na chemotherapie (polyneuropathie)
- Pijn zonder relatie tot de tumor.
Hoewel iedereen pijn op zijn eigen manier ervaart, zijn er wel algemene kenmerken die belangrijk zijn om te vertellen aan de arts:
- tijdsdimensie (hoe lang, constant of met tussenpozen, wanneer?)
- kwaliteit (prikkelend, drukkend, kloppend, zeurend?)
- intensiteit
- locatie.
Het ervaren van pijn is niet alleen lichamelijk, maar heeft ook te maken met de betekenis die je geeft aan de pijn. Ook emoties zoals angst kunnen de pijn versterken. De intensiteit (hevigheid) van pijn is subjectief. Om de intensiteit van pijn meetbaar te maken wordt gebruikgemaakt van de pijnscore.
Door de pijn een cijfer te geven, kun je de ernst van de pijn beter benoemen en is het mogelijk om het effect van de pijnbehandeling te beoordelen. Een score van 1 tot 4 wordt gezien als milde pijn, 5 en 6 als matige pijn en 7 tot 10 als ernstige pijn.
Een van de manieren om pijn te bestrijden is medicijnen toe te dienen. Hierbij is het belangrijk dat je de medicijnen inneemt zoals is voorgeschreven. Dit is in veel gevallen op vaste tijden, maar in sommige gevallen op het moment dat de pijn erger wordt. Soms krijg je voorschriften om het medicijn op een specifiek moment in te nemen, bijvoorbeeld tijdens het eten. Of om ze met een bepaalde vloeistof in te nemen. Het is belangrijk dat je de instructies opvolgt. Zo zorg je ervoor dat het medicijn zijn werk goed doet.
Een buikwond kan lang pijnlijk of gevoelig zijn, terwijl de huid rond het litteken juist lange tijd, en soms blijvend, ongevoelig is doordat de kleinere huidzenuwen bij de operatie doorgesneden zijn. Bij de operatie is ook door de buikspieren gesneden waardoor het aanvankelijk pijnlijk is om in beweging te komen en te blijven. Tijdens en na de operatie wordt pijnstilling toegediend via een epiduraal katheter om ervoor te zorgen dat de pijn aanvaardbaar is. Omdat pijn niet alleen wordt beïnvloed door lichamelijke oorzaken kunnen andere activiteiten de pijn soms verlichten. Denk aan een massage van handen en/of voeten of
- ademhalingsoefeningen ter ontspanning. Ook afleiding helpt de pijn even naar de achtergrond te brengen. Pijnstillers, met name opioïden, kunnen ook bijwerkingen hebben, zoals:
- obstipatie. Om deze bijwerking te verminderen wordt ook een laxeermiddel voorgeschreven om zo nodig te gebruiken. Vezelrijke voeding (zoals bruin brood, groenten) is ook belangrijk. En ook voldoende drinken (1,5-2 liter) is heel belangrijk;
- misselijkheid en braken. Er zijn medicijnen die deze bijwerking verminderen. Soms geeft ook het drinken van cola verlichting. Drink het bij voorkeur op kamertemperatuur. Als de misselijkheid wordt veroorzaakt door het gebruik van opioïden dan verdwijnt dit vaak na enkele dagen;
- sufheid
- droge mond en lippen: drink meer, neem kleine slokjes of zuig op een ijsklontje.
Door pijn kun je minder actief worden. In bed blijven liggen lijkt een oplossing, maar dat is niet verstandig. De kans op complicaties, zoals trombose en longontsteking wordt groter op die manier. Bovendien komen je darmen minder snel op gang. Obstipatie en misselijkheid zijn daarvan het gevolg. Om longontsteking te voorkomen is goed doorademen belangrijk. Dit kan pijnlijk zijn waardoor je ademhaling oppervlakkig wordt. Hoesten is eveneens pijnlijk, maar ook dit is belangrijk om een longontsteking te voorkomen. Om je ademhaling te bevorderen is het van belang dat je uit bed komt. Als dat niet goed lukt, dan is het belangrijk dat je in bed goed rechtop zit en regelmatig diep doorademt. Bij het hoesten helpt het als je je buik ondersteunt met een kussentje.
Lang aanhoudende pijn kan leiden tot somberheid en slapeloosheid. Goede pijnstilling helpt deze problemen te voorkomen.
Verminderde darmwerking
Na de operatie liggen de darmen meestal enige tijd stil. Meestal herstelt de werking van de darmen zich binnen drie dagen. Als dat niet zo is, krijg je meestal medicijnen die de darmwerking bevorderen. Soms blijft de doorgang van voedsel door de darmen een langere poos belemmerd. Dit komt doordat de spieren in de darmwand, die zorgen voor de voortstuwing van de inhoud van de darmen, niet goed samentrekken. Om die reden kan het voedsel het lichaam niet als ontlasting verlaten en ontstaat er een (gedeeltelijke) darmafsluiting , ook wel ileus genoemd. Klachten hiervan zijn:
- buikpijn
- een opgezette buik braken
- het wegblijven van winden en ontlasting
- geen darmbeweging en geen darmgeluiden (stille buik).
Om de werking van de darmen te bevorderen is het belangrijk dat je zo snel mogelijk na de operatie begint met eten. Bouw dit wel rustig op door te beginnen met licht verteerbare voedingsmiddelen (zoals brood, fruit, toetje) en geleidelijk aan zwaarder vallend voedsel toe te voegen. Voldoende drinken en uit bed komen is daarnaast heel belangrijk.
Stoma
Tijdens de operatie bekijkt de arts de organen in de buik, waaronder de darmen. Soms is er doorgroei van de tumor in de darmen. Dan kan het noodzakelijk zijn om een deel van de darmen weg te nemen. Daarbij moet dan soms een tijdelijk of blijvend stoma worden aangelegd. Een stoma is een kunstmatige uitgang. Hierbij komt de uitgang van de darm op de buik te liggen (figuur 16). Het verschil tussen een colostoma (dikke darm) en een ileostoma (dunne darm) is niet alleen het type darm waarvoor de stoma een kunstmatige uitgang is. Er is ook verschil in frequentie en dikte van de ontlasting en in de hoeveelheid vocht die via de stoma verloren gaat. Zo produceert de ileostoma continu brijige of dunne ontlasting waardoor de kans op vochttekort groter is. Ook kan zo een tekort aan zouten ontstaan. De colostoma produceert meestal een aantal keer per dag ontlasting via een herkenbaar patroon. De anus heeft een sluitspier, een stoma niet. Er kan dus voortdurend en vooral ongemerkt ontlasting uit de stoma komen. Om dit op te vangen, zijn er speciale stomazakjes. Via de anus verliest men soms nog wel slijm.
Als voor de operatie duidelijk is dat er een stoma aangelegd moet worden, komt de stomaverpleegkundige in beeld. Ze bespreekt met jou waar de stoma het beste geplaatst kan worden. Dit is afhankelijk van een aantal factoren, zoals de vorm en plooien van je buik, je postuur, het type kleding dat je draagt en het soort werk dat je doet, eventuele hobby’s en beperkingen die je hebt. De plaatsbepaling van de stoma is voor de arts een aanwijzing, maar hij kan hier om medische redenen van afwijken. De stomaverpleegkundige zal je informatie geven over het leven met een stoma en ook regelt zij de zorg rondom de stoma.
Het leven met een stoma kan aan de ene kant een nieuwe kans betekenen doordat je leven bedreigd is door de kwaadaardige aandoening. Maar aan de andere kant brengt het ook een grote verandering in je dagelijks leven. Je lichaam is anders, het werkt anders en ziet er anders uit. Verschillende emoties kunnen elkaar in razend tempo afwisselen.
Het volledig accepteren van een stoma is moeilijk, maar de ervaring leert dat de meeste vrouwen er goed mee leren omgaan (acceptatie). Als je dat moeilijk vindt, kun je terecht bij onder andere psycho-oncologische centra die hierin begeleiding bieden.
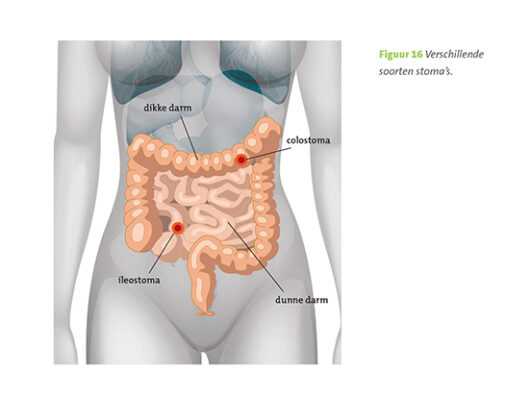
Figuur 16. Verschillende soorten stoma’s.
De overgang
Meestal ontstaat eierstokkanker na de overgang. Echter, een jonge vrouw komt, op het moment dat beide eierstokken worden verwijderd, in de overgang. Voor een vrouw die nog vruchtbaar was voor de operatie, betekent het dat zij vervroegd in de overgang komt. Net als bij de natuurlijke overgang kunnen hierdoor klachten ontstaan. Die kunnen hevig zijn, omdat de hormoonproductie van de eierstokken abrupt is gestopt. Voor het plotseling wegvallen van de hormoonproductie kunnen hormoonvervangende medicijnen worden gegeven.
Klachten waarvan je snel (soms al vijf dagen na de operatie) last kunt krijgen zijn opvliegers, overmatige transpiratie, het wisselend warm en koud hebben, slapeloosheid en stemmingswisselingen. Geen zin hebben in seks komt op langere termijn ook voor. Bij vrouwen die al in de overgang waren, kunnen deze klachten erger worden na de operatie. Als je door een behandeling vervroegd in de overgang bent gekomen, is de kans op botontkalking (osteoporose) en hart- en vaatziekten groter.
Een opvlieger is een plotselinge aanval van warmte en transpiratie die veroorzaakt wordt door verandering in de hormoonhuishouding. Een opvlieger herken je door een hevig gevoel van warmte op de borst die zich uitbreidt naar de hals en het hoofd en soms naar je hele lichaam. Doordat kleine bloedvaatjes open gaan staan wordt je huid rood. De transpiratie is hevig. De opvlieger zakt meestal na één tot drie minuten, waarna je het juist erg koud krijgt. Het overmatig transpireren is erg onplezierig en komt ook ’s nachts voor waardoor je slaap ernstig verstoord kan worden.
Enkele tips bij opvliegers
- Pas je kleding aan. Draag verschillende lagen kleding zodat je iets kunt uittrekken als je het warm hebt en kunt aantrekken als je het daarna weer koud hebt. Katoenen kleding neemt veel vocht op. Bij nachtelijke opvliegers is het dragen van katoenen nachtkleding en het gebruik van katoenen hoeslakens aan te raden.
- Zorg ervoor dat je voldoende drinkt (1,5 tot 2 liter per dag). Gekoelde dranken kunnen de opvlieger verminderen. Alcohol, koffie, thee en cola verhogen de kans op het krijgen van een opvlieger.
- Vermijd warme ruimtes. Een warme kamer of een warm bad kan een opvlieger uitlokken.
- Eet niet te veel kruiden. Sterk gekruide voeding kan opvliegers uitlokken.
Seksualiteit
Veranderde seksualiteit is een van de gevolgen van de behandeling (chemotherapie en chirurgie) van kanker. Kort na de operatie en rondom de behandeling zul je daar niet zo mee bezig zijn. Toch is het goed om erbij stil te staan, ook een jaar na de behandeling. Allereerst omdat je behalve een buikwond ook een wond aan de vaginatop hebt. De eerste zes weken na de operatie kun je beter geen gemeenschap hebben zodat de wond kan genezen. De meeste vrouwen hebben vlak na de operatie en ook later meer behoefte aan warmte en genegenheid dan aan gemeenschap. Ook als de wond genezen is kan het nog wel even duren voor je behoefte hebt aan seks. Dit kan onder andere te maken hebben met de veranderingen in je hormoonhuishouding. Je vagina kan daardoor minder vochtig zijn. Ook kun je een orgasme anders beleven dan voorheen. Dat komt doordat je baarmoeder is verwijderd; er zijn vrouwen die het samentrekken van hun baarmoeder missen. Gevoelens als angst en gespannenheid spelen een belangrijke rol bij verandering in de seksuele behoefte, zowel bij de vrouw als bij de partner. Het is belangrijk te praten over problemen op het gebied van seksualiteit als je daar last van hebt. Lotgenotencontact, de behandelend arts, de oncologieverpleegkundige en de medisch maatschappelijk werker kunnen jou en je partner helpen om te gaan met veranderingen. Als het nodig is kunnen zij jullie doorverwijzen naar een seksuoloog. Wacht niet tot een professional over seksualiteit begint. Begin er zelf over.
Vermoeidheid
Vermoeidheid is een veelgehoorde klacht van kankerpatiënten. Vermoeidheid na de diagnose is een complex probleem. Fysieke en psychische factoren dragen bij aan de vermoeidheid, maar vermoeidheid veroorzaakt op haar beurt fysieke en psychische klachten. Bovendien is vermoeidheid niet toe te schrijven aan één oorzaak. Er wordt daarom gesproken over uitlokkende factoren en in stand houdende factoren. De uitlokkende factoren zijn de kanker en de behandeling van kanker. Angst voor terugkeer van de ziekte, weinig sociale steun, te veel of te weinig activiteiten, verstoord slaappatroon, het gevoel weinig controle te hebben en een gebrek aan of ontoereikende verwerkingsstrategieën zijn onder andere factoren die de vermoeidheid in stand houden.
De vermoeidheid is anders dan ‘normale’ vermoeidheid. Het is er plotseling en vaak in volle hevigheid. Het is meestal niet het gevolg van inspanning of staat niet in verhouding tot de inspanning die geleverd is. De herstelperiode is langer en rust nemen of slapen lost niets op. Het is een probleem dat het leven behoorlijk beïnvloedt. Het werk kan te zwaar zijn, waardoor arbeidstijden moeten worden aangepast of gezocht moet worden naar andere werkzaamheden. Sociale contacten worden minder, omdat de energie die er is, opgaat aan zorg voor het gezin en andere verplichtingen. Ook in de thuissituatie veranderen er dingen. Het huishouden kan te veel zijn, waardoor er meer gevraagd wordt van andere gezinsleden. Door minder energie moet er gezocht worden naar een nieuw evenwicht in de relatie.
Hoe complex het probleem ook is, je kunt er wel zelf iets aan doen. Het is vooral belangrijk na de behandeling de draad van je gewone leven zo goed mogelijk op te pakken. Accepteer dat je niet alles kunt en blijf in beweging. Door te bewegen zorg je ervoor dat je conditie verbetert en het geeft afleiding zodat je je gedachten verzet. Verdeel andere activiteiten en houd je grenzen in het oog. Een vast slaappatroon is aan te bevelen, omdat langer in bed liggen de klachten niet vermindert. Goede voeding is ook van belang. Lukt het ondanks deze inspanningen niet om met de vermoeidheid om te gaan dan kun je professionele hulp inroepen. Een van de mogelijkheden is cognitieve gedragstherapie.
Psychische problemen
Spanning treedt vaak al op voordat de diagnose is gesteld. Vage klachten kunnen het vermoeden geven dat er iets aan hand is. De onrust die dan ontstaat, kan uiteindelijk overgaan in angst. Stress treedt vooral op de voorgrond als de diagnose weliswaar is gesteld, maar nog niet duidelijk is wat de gevolgen precies zijn. Dat is niet raar. Enerzijds moet je de diagnose verwerken, anderzijds moet je belangrijke beslissingen nemen over de behandeling. Angst en boosheid komen veel voor. Angst vanwege de onzekerheid over de ziekte en de behandeling. Boosheid komt met name tot uiting in waarom-vragen zoals: Waarom overkomt mij dit? en Waarom ben ik niet eerder serieus genomen? De spanning in deze periode leidt vaak tot slaapproblemen, vermoeidheid, geïrriteerdheid en nervositeit.
Tijdens de behandelperiode laaien verschillende emotionele spanningen op, afhankelijk van bijvoorbeeld de ernst van de bijwerkingen en persoonlijkheidskenmerken. Ondanks al die spanningen ervaren de meeste patiënten het vaak als positief dat de ziekte nu aangepakt wordt. Het overleven staat in deze periode voorop.
Opluchting kenmerkt vaak de periode ná de behandeling, omdat die heel belastend is. Toch steken dan ook angst voor terugkeer en onzekerheid de kop op. De regelmatige controles en de contacten met artsen vallen in deze periode weg, wat je als een gemis kunt ervaren.
Het is bovendien de periode waarin je alle narigheid kunt laten bezinken. Daardoor kunnen opeens allerlei emoties loskomen. De meeste mensen hervinden ongeveer een jaar na de behandeling hun evenwicht.
Depressie
Het is niet makkelijk om in een emotionele periode goed onderscheid te maken tussen wat een ‘normale’ reactie is op een levensbedreigende ziekte en wat toe te schrijven is aan een depressie. Ontroostbaar huilen, slecht slapen, vermoeid zijn en moeite hebben met concentreren kunnen door een depressie worden veroorzaakt. Ze kunnen ook een heel normale reactie zijn op de omstandigheden of veroorzaakt worden door de behandeling. Specifiekere klachten voor een depressie zijn: slecht voor jezelf zorgen en je uiterlijk verwaarlozen, vaak aan de dood denken en dit ook als een uitweg zien. Bij een depressie zijn negatieve gevoelens vaak continu aanwezig. Als je daar last van hebt en je herkent jezelf niet in de somberheid waarin je bent ondergedompeld, is het belangrijk dat je daarover praat. Een depressie vermindert je kwaliteit van leven en leidt vaak tot therapieontrouw. Het is daarom belangrijk dat je depressie wordt erkend en behandeld.
Veranderd zelfbeeld
Het zelfbeeld zegt iets over hoe je je persoonlijke eigenschappen, je lichaam en je uiterlijk ervaart. In de loop van je leven is dat zelfbeeld onderhevig aan veranderingen. Deze veranderingen vinden meestal geleidelijk plaats en leveren daardoor geen problemen op. Als je kanker krijgt heeft dat voor je uiterlijk plotselinge, dramatische gevolgen, die je flink uit je evenwicht kunnen brengen. Gezondheid en onafhankelijkheid blijken ineens niet zo vanzelfsprekend als je altijd aannam. Vrouwen kunnen door het verwijderen van hun baarmoeder het gevoel hebben dat ze minder vrouw zijn. De impact van haarverlies tijdens de chemotherapie is groot. Vervroegd in de overgang komen heeft heel veel consequenties. Dat maakt het allemaal niet gemakkelijk je zelfbeeld aan de veranderingen aan te passen. Dat proces komt eigenlijk pas op gang als alle behandelingen achter de rug zijn en dat gaat niet zonder slag of stoot. Het is vooral belangrijk om je gevoelens daarover te delen, (weer) aandacht te besteden aan je lichaam en aan je conditie te werken om fit te worden. Je zult zien dat je juist in deze periode geniet van kleine dingen die voorheen onbelangrijk leken. Het lukt je waarschijnlijk ook beter je grenzen te bepalen, waardoor je steviger in je schoenen staat en je heel verbonden voelt met degenen die je nastaan. Het proces van aanpassen is complex. Als het je niet lukt in je eentje tot een vernieuwd zelfbeeld te komen, kun je om professionele begeleiding en steun vragen.
Sociale problemen
Tijdens de intensieve behandelperiode voelde Anna zich geleefd door de vele afspraken in het ziekenhuis. De regelmaat van die bezoeken gaf haar echter ook houvast. Nu alles achter de rug is, moet ze een nieuw ritme zien te vinden en dat valt niet mee, vertelt Anna de oncologieverpleegkundige: ‘Alles wat vanzelfsprekend was, is door de ziekte veranderd. Ik was altijd onafhankelijk, patiënt zijn vind ik moeilijk.’ Eerst belemmerden de behandeling en de bijwerkingen haar om te werken en haar gezin draaiend te houden. Nu staan de vermoeidheid en de verwerking van alle gebeurtenissen dat in de weg. Anna wil dolgraag weer optimaal functioneren. ‘Maar die verdraaide vermoeidheid komt opeens opzetten en ik kan me maar moeilijk concentreren. Leg dat maar eens uit aan een collega.’ Bovendien heeft ze momenten dat de tranen maar blijven stromen. Er is geen houden aan. Het is een rare gewaarwording dat alle emoties in alle hevigheid naar buiten komen, vindt ze. Het ligt tenslotte allemaal achter haar.
Als je eierstokkanker hebt, heeft dat consequenties voor je sociale en maatschappelijke omgeving. Het zal je namelijk niet lukken je alledaagse rollen te vervullen zoals je dat voor de diagnose deed.
Veranderingen in relaties
Door de kanker is je dagelijkse routine verstoord in de relatie met mensen uit je directe omgeving, met name je partner en kinderen. Zeker je partner wordt aan veel stress blootgesteld, net als jij.
Onzekerheid, angst, de bijwerkingen van de behandelingen en jouw emoties trekken een zware wissel op de relatie met je partner en soms ook met de kinderen. Door je beperkingen ben je afhankelijker van je partner, die daardoor meer (zorg)taken op zich neemt dan voorheen.
Ook komt het normale gezinsfunctioneren onder druk te staan. De diagnose en de emoties die daaruit voortkomen moeten de ouders zelf verwerken, maar tegelijkertijd moeten zij hun kinderen het slechte nieuws vertellen en maken zij zich zorgen over de impact voor hun kinderen. De ervaring leert dat het belangrijk is om de ziekte niet te verzwijgen, maar dat erover praten met elkaar uiteindelijk het beste is. Dit zorgt voor vertrouwen binnen het gezin. Houd de kinderen op de hoogte en bereid ze voor op wat te verwachten is. Door verandering in de relaties binnen het gezin en veranderingen van de dagelijkse gang van zaken is het belangrijk om als gezin bij elkaar betrokken te blijven. Heb aandacht voor elkaars wel en wee en zorg ervoor dat je als gezin tijd neemt voor elkaar. Reacties van kinderen op dit alles zijn onder andere afhankelijk van hun leeftijd en hun ontwikkelingsniveau.
Arbeidsproces
De diagnose heeft gevolgen voor het werk dat je doet. Je vraagt je na de diagnose vast af of je je ziek moet melden en of je nog wel (deels) kunt blijven werken. Voor de meeste vrouwen is overleven van de ziekte prioriteit nummer één en staat het werk op een andere plaats. Waar de één behoefte heeft aan rust en ruimte om met de nieuwe situatie om te gaan, wil de ander het dagelijks leven voortzetten, voor zover het kan. De rol die het werk in iemands leven heeft, hangt af van de levensfase, gezinsleven en privé-situatie van de vrouw. De behandelend arts kan je informeren over de invloed die de ziekte en de behandeling (bijwerkingen) kunnen hebben op je leven en over de verwachte duur van het herstel. Tijdens de behandeling en in de herstelperiode kun je zoveel last hebben van bijwerkingen als vermoeidheid, concentratie- en geheugenproblemen dat het moeilijk is je werkzaamheden uit te voeren. Belangrijk is dat je je werkgever op de hoogte brengt van de situatie. Onderzoek wijst uit dat het gemakkelijker is naar je werk terug te keren als je tijdens de behandeling en de herstelfase contact houdt met een aantal mensen op je werk.
Als je je ziek meldt en als je weer wilt gaan werken, komt de bedrijfsarts in beeld die je begeleidt. Het is gebleken dat het goed is dat je na je herstel weer deelneemt aan het arbeidsproces, vooral ook voor de verwerking. Het kan zijn dat je oorspronkelijke werkzaamheden te zwaar zijn. In dat geval wordt er meestal gezocht naar alternatieven.
Verwerken
Het besef dat kanker je leven op zijn kop heeft gezet komt meestal pas als de behandeling achter de rug is. Toch begint het omgaan met de ziekte al vanaf het moment dat je door klachten voor het eerst aan kanker denkt. Daarvoor was kanker vooral iets wat anderen overkomt en nu word jij ermee geconfronteerd. De ingrijpende veranderingen die kanker teweegbrengt, gaan gepaard met hoog oplopende emoties en vragen om aanpassingen. De verwerking van al die veranderingen is een actief proces. Een voorwaarde om iets te kunnen verwerken is dat je de emoties toelaat en ze kunt uiten en delen met anderen. Dat valt niet mee; je kunt er zelfs bang voor zijn. Het komt ook voor dat iemand alle emoties onderdrukt in een poging controle te krijgen over de verwarrende situatie. Zonder emoties is het echter niet mogelijk om iets te verwerken. Dit zorgt ervoor dat het ‘echte’ verwerken pas begint na de turbulente periode van behandeling.
In de periode dat behandeling plaatsvindt zijn de meeste patiënten letterlijk alleen maar bezig met overleven. Ze leven bij de dag en die dag wordt vooral bepaald door de behandeling. Hun sociale leven wordt daardoor kleiner, wat betekent dat het ook lastiger is om emoties te delen.
Pas als ze met goede moed proberen het gewone leven na de behandeling op te pakken, komen de gevolgen van de ziekte en de behandeling in volle omvang aan het licht. Problemen met concentreren, vermoeidheid en (onderdrukte) emoties belemmeren je in het oppakken van je oude leven. Dit gebeurt als je omgeving denkt dat het hele proces achter de rug is, terwijl het echte verwerken dan pas begint. Ook dan blijft het heel belangrijk om je emoties te delen met anderen. Dit kan door erover te praten, maar je kunt ook een blog of dagboek bijhouden. Zorg in deze periode extra goed voor jezelf, zowel psychisch als fysiek. Leef gezond, zoek rust en kracht in muziek, meditatie of in de natuur en werk aan je lichamelijke conditie en ontspanning. Het vinden van een nieuw evenwicht kost tijd, gun jezelf die tijd. Lukt het je niet alleen? Blijf je bijvoorbeeld maar piekeren en heb je om de haverklap huilbuien, slaap je slecht en moet je niet denken aan eten? Schroom dan niet om een professionele hulpverlener in te schakelen die je kan helpen. Wacht daar niet te lang mee. Het is geen teken van zwakte, maar juist van kracht. Waarom zou je langer in de put zitten dan nodig is?
- Kaart de situatie aan bij je behandelend arts en de oncologieverpleegkundige. Zij kunnen je geruststellen en je adviseren.
- Zij zijn in staat onderliggende problemen en knelpunten te signaleren en weten ook bij wie je het beste terechtkunt voor begeleiding en ondersteuning. Zo zijn maatschappelijk werker, geestelijk verzorger, psycholoog of psychiater geschikt om je psychisch weer op de rails te krijgen.
- Voor je fysieke herstel bestaat de oncologische revalidatie. Deze behandeling bestaat uit verschillende modules die je individueel of in groepsverband kunt volgen. Daar werk je aan je lichamelijke conditie en bevorder je je herstel.
- Tot slot kan lotgenotencontact een grote rol spelen bij de verwerking. Bij Stichting Olijf vind je daar allerlei informatie over.
Stichting Olijf
Olijf is het netwerk voor vrouwen met gynaecologische kanker. Gynaecologische kanker heeft vaak een enorme impact op het leven van de vrouw en hun naasten: Olijf is er dan voor ze. Bij Olijf zetten ze zich, vanuit een onafhankelijke positie, in voor preventie, onderzoek, voorlichting, lotgenotencontact en belangenbehartiging.
Het resultaat van het werk van Olijf is dat vrouwen zich beter geïnformeerd voelen en daardoor beter keuzes kunnen maken als het gaat om hun gezondheid en hun leven. Het geeft de vrouwen meer grip op hun leven om hun ervaringen te delen met ‘mensen die aan een half woord genoeg hebben’. Stichting Olijf gaat vaak verder waar de (na)zorg stopt. Neem eens een kijkje op www.olijf.nl.
Samenvatting
De diagnose eierstokkanker beïnvloedt je dagelijks leven door fysieke, psychische en sociale problemen. Opvallend is dat vaak tijdens de behandeling en in de eerste periode daarna vooral de fysieke klachten op de voorgrond staan. Psychische en sociale problemen nemen op een later moment een grotere rol in. De meeste mensen die behandeld zijn voor kanker, realiseren zich pas na de behandeling hoe de ziekte hun leven beïnvloedt. In eerste instantie staat overleven voorop. In het jaar na de behandeling verschuift de aandacht naar het vinden van een nieuw evenwicht om de draad van je leven op te pakken.
Schroom niet via je behandelend arts of oncologieverpleegkundige een professionele hulpverlener in te schakelen. Voor het fysieke herstel bestaat oncologische revalidatie en voor extra ondersteuning en begeleiding bij problemen op psychisch en sociaal gebied zijn een maatschappelijk werker, geestelijk verzorger, psycholoog of psychiater geschikt.
Ook Stichting Olijf kan je helpen, bijvoorbeeld als je behoefte hebt aan lotgenotencontact.
Als behandeling niet meer mogelijk is - palliatieve zorg
Als alle behandelmogelijkheden zijn uitgeput om de ziekte tot staan te brengen, breekt de laatste levensfase aan. Op weg naar het levenseinde staat palliatieve zorg op de voorgrond. Alle aandacht gaat naar pijnbestrijding en het verlichten van symptomen. Het naderende afscheid staat centraal.
Palliatieve fase
Vanaf de eerste keer dat de eierstokkanker terug was (recidief) en Marit hoorde dat ze niet meer kan genezen, is zij in de palliatieve fase van haar ziekte (figuur 17). Zo lang behandeling met chemotherapie mogelijk is, is dat bij eierstokkanker een goede manier om de klachten die de ziekte geeft, te bestrijden. Eierstokkanker is vaak lang gevoelig
voor chemotherapie en reageert er meestal snel op. Dit betekent dat de klachten verminderen, waardoor het effect van de chemotherapie opweegt tegen de bijwerkingen van de chemotherapie (ziektegerichte palliatie). Nu het effect van chemotherapie bij Marit echter nog maar zo kortstondig is, is de fase aangebroken dat de behandeling er alleen op gericht is Marit zo weinig mogelijk klachten te laten hebben (symptoomgerichte palliatie) voor zo lang als dat mogelijk is.
Ascites
Ascites is de ophoping van vocht in de vrije buikholte. Ascites is meestal heldergeel, soms is het troebel en/of bloederig. Ascites komt veel voor bij eierstokkanker, omdat die zich heel vaak uitzaait naar het buikvlies. Een derde van de patiënten heeft ascites bij het stellen van de diagnose en nog een derde krijgt er in een later stadium last van.
Het wordt veroorzaakt door een combinatie van factoren die met de aanwezigheid van kanker in het buikvlies samenhangen: de kankercellen zorgen ervoor dat de bloedcapillairen (kleinste bloedvaten) makkelijker vocht doorlaten en de afvoer van het vocht via de lymfebanen verloopt moeizamer.
De klachten en lichamelijk onderzoek maken snel duidelijk of er sprake is van ascites. Soms is een echografie nodig om een vermoeden te bevestigen. Er kan ook sprake zijn van ascites voordat klachten ontstaan. Dan wordt het gezien op de echografie die de gynaecoloog doet of op een CT-scan die om een andere reden is gemaakt.
De meest voorkomende klachten door ascites hangen samen met de toename van de buikomvang. De broek of rok kan niet meer dicht.
De mobiliteit vermindert door moeite met bewegen door de dikke buik en door vermoeidheid. De beweeglijkheid van de darmen is minder, waardoor obstipatie ontstaat. Druk op de buikwand en de rug veroorzaakt pijn, druk op het middenrif veroorzaakt kortademigheid en door druk op de maag vermindert de eetlust. Het gewicht neemt toe door de ophoping van vocht. Bij veel ascites zie je bij lichamelijk onderzoek een sterk opgezette, glanzende buik en een navel die niet meer diep ligt (verstreken navel).
De snelste behandeling van ascites is het laten aflopen van het vocht door een naald via de buikhuid in de buikholte te plaatsen (ontlastende ascitespunctie). Na terugtrekking van de naald blijft een klein kathetertje achter, waardoor het vocht naar buiten kan aflopen (figuur 18). Dit is een eenvoudige ingreep die makkelijker uit te voeren is dan een bloedafname en het heeft bijna altijd meteen effect op de klachten. Als het vocht is afgelopen, wordt het kathetertje verwijderd. Helaas duurt het effect van een ontlastende ascitespunctie vaak niet langer dan één à twee weken. Herhaalde puncties zijn dan nodig, waardoor het plaatsen van een permanente ascitesdrain nodig is. Dat gebeurt door de radioloog. Het deel van de katheter dat zich buiten de buik bevindt, is met een kraantje afgesloten. Als je denkt dat het nodig is, zet je het kraantje open en kan het vocht uit de buikholte lopen.
Het grote voordeel hiervan is dat je hiermee klachten van ascites voorkomt. De thuiszorg verzorgt de permanente ascitesdrain één à twee keer per week. De thuiszorg kan ook behulpzaam zijn bij het laten aflopen van de ascites, maar de ervaring leert dat de meeste mensen dit zelf doen.
Een permanente ascitesdrain kan verstopt raken en moet dan gewisseld worden. Ook kan er lekkage naast de katheter optreden. Vaak kan dit met verbandmateriaal opgevangen worden. Heel zelden treedt een infectie op. Door pocketvorming in de buikholte lukt het soms niet meer om de ascites af te laten lopen. Dat komt doordat de kleine holtes (pockets), waarin het vocht zich ophoopt, niet (meer) met elkaar in verbinding staan.
Bij eierstokkanker hebben vochtafdrijvende medicijnen, diuretica, nauwelijks effect bij ascites. Daarom is een ontlastende ascitespunctie de enige zinvolle behandelingsmogelijkheid als chemotherapie niet meer effectief is.
Obstipatie
Een groot probleem bij uitgezaaide eierstokkanker is het vastlopen van de ontlasting. Omdat de ziekte vaak in de gehele buik aanwezig is, hebben de darmen het moeilijk om te functioneren en zich te ontlasten. Er ontstaat hardlijvigheid oftewel obstipatie, wat betekent dat er weinig frequent en met moeite ontlasting is. Gemiddeld is bij gezonde personen sprake van ontlasting driemaal daags tot eenmaal per twee dagen. Als deze frequentie afneemt, kun je buikpijn krijgen, misselijk zijn en braken. In het ergste geval komen de darmen helemaal stil te liggen en spreken we van een ileus. Obstipatie heeft grote gevolgen voor de kwaliteit van leven.
Zodra eierstokkanker zich verspreid heeft in de buik is dagelijkse stoelgang van belang. Regelmatig is ondersteuning met laxeermiddelen nodig om de ontlasting zacht te maken. Daarbij bepaalt de reactie op het laxeermiddel de dosering. Als je een laxeermiddel voorgeschreven krijgt, pas je zelf de dosering aan, afhankelijk van de frequentie van je stoelgang en de vastheid van je ontlasting. Daarnaast is het belangrijk dat je voldoende drinkt (ten minste 1,5 liter per dag), dat je zo regelmatig, gevarieerd en vezelrijk mogelijk eet en zoveel mogelijk beweegt. Als de ziekte vordert en het moeilijker voor je is deze leefregels vol te houden helpen de laxeermiddelen je stoelgang op gang te houden.
Een andere oorzaak voor obstipatie is medicijngebruik. Vooral morfine en morfine-achtigen (opioïden) veroorzaken dat euvel. Bij gebruik daarvan krijg je daarom laxeermiddelen voorgeschreven. Ook dan zijn gezond eten, voldoende drinken en lichaamsbeweging weliswaar belangrijk om de stoelgang op orde te houden, maar dat zal niet altijd meer lukken.
Ileus
Bij een ileus is de functie van de darmen stil komen te liggen. Dit kan het gevolg zijn van een gedeeltelijke of totale afsluiting op één of meer plaatsen in de darm (mechanische ileus) door grote tumormassa’s. Een verminderde of opgeheven beweeglijkheid van de darmen (paralytische ileus) kan er ook aan ten grondslag liggen (vaak bij ascites). Een combinatie van beide komt vaak voor bij patiënten bij wie de eierstokkanker in het buikvlies is uitgezaaid. Ernstige misselijkheid en hevig braken zijn het gevolg, meestal meteen nadat je iets gegeten of gedronken hebt. Stoelgang is er niet of nauwelijks. Als het braken pas vele uren later gebeurt, komen opgehoopt vocht en voeding in grote golven naar buiten. Dit zogenoemde projectielbraken lucht vaak enorm op. Bij een ileus kan het braaksel naar poep (feces) ruiken. Dit heet ‘fecaal braken’. Er wordt niet letterlijk poep gebraakt, maar door de langdurige aanwezigheid van het vocht in de dunne darm heeft dit door bacteriële processen de geur van poep gekregen.
Een ileus geeft ook pijn, zowel aanvalsgewijs door darmspasmen als continu door uitzetting van de darmen of door druk van de tumor. Als de buik is opgezet door ophoping van lucht en/of vocht in de darm, ontstaat pijn.
Bij het lichamelijk onderzoek is soms sprake van luide darmgeluiden (‘gootsteengeruis’) en op andere momenten is de buik juist stil. Een staande röntgenfoto van de buik laat vaak zien dat de darmen uitgezet zijn en daarin zijn vloeistofspiegels zichtbaar.
De behandeling van een ileus is allereerst gericht op het ontlasten van de darmen. Je mag dan niet eten of drinken en klysma’s maken de darmen leeg. Een infuus met vocht voorkomt uitdroging en een afhangende maagsonde, ingebracht via de neus, voert maagsappen af. Een maagsonde is niet prettig. Voortdurende misselijkheid en braken is echter ook zeer belastend. Bovendien bestaat het gevaar dat je je verslikt tijdens het braken, waardoor maaginhoud in de longen terechtkomt en een longontsteking kan ontstaan.
Als blijkt dat de darmen worden geblokkeerd door een tumormassa is soms een operatie mogelijk. Dat hangt onder andere af van de wens, de conditie, de technische mogelijkheden en de levensverwachting van de patiënt. Meestal betekent dit dat een stoma wordt aangelegd, waardoor de darm zich kan ontlasten.
Als een ileus niet verbetert, is de levensverwachting beperkt. Kunstmatige voeding via een infuus draagt meestal niet bij aan de kwaliteit van leven en ook vochttoediening via een infuus wordt meestal na enige tijd gestopt. Vaak is er nog wel enige inname en passage van vocht mogelijk. Veel patiënten gaan naar huis of naar een hospice voor de laatste levenstijd. Een infuus buiten het ziekenhuis is mogelijk, maar is ook een technische handeling die extra onrust kan veroorzaken. Daarbij kan het de maag- en darmsapproductie in stand houden of zelfs stimuleren, terwijl het juist het doel is om deze productie zoveel mogelijk te remmen. Op dorstgevoel heeft kunstmatige vochttoediening weinig invloed. Om dit te voorkomen of te bestrijden is goede mondverzorging belangrijk. Als de maagsonde blijft zitten, kan dit een gevoel van droge mond geven. Dat komt doordat je vaak met open mond moet ademen, omdat je neus deels geblokkeerd is. Het is dus altijd goed te overwegen of de maagsonde verwijderd kan worden.
Pleuravocht
Door kankercellen op de longbladen kan er vocht ontstaan bij de longen. Dit pleuravocht hoopt zich op tussen de twee longbladen (pleura). Het mechanisme van vochtvorming is hetzelfde als bij ascites: de kankercellen zorgen ervoor dat de capillairen makkelijker vocht doorlaten en de afvoer van het vocht via de lymfebanen gaat moeizamer. De symptomen van pleuravocht zijn kortademigheid en pijn. De behandeling bestaat net als bij ascites uit het aanprikken van het vocht. De belangrijkste risico’s van het aanprikken van pleuravocht is het ontstaan van een klaplong en een infectie.
Als het pleuravocht snel terugkeert kan worden besloten om de long ‘te plakken’ (pleurodese). Via een grotere drain wordt in enkele dagen al het vocht weggezogen, waarna een etsende stof wordt ingespoten. Dit verwondt de longbladen, waardoor ze tijdens het genezingsproces met elkaar verkleefd raken. Hierdoor kan zich niet opnieuw vocht ophopen tussen de longbladen.
Vaginaal bloedverlies
Vaginaal bloedverlies komt niet veel voor bij uitgezaaide eierstokkanker, doordat de vrouwelijke geslachtsorganen bij de operatie verwijderd zijn. Toch kan het voorkomen dat er lokaal weer kanker aanwezig is op de top van de vagina en dat dit klachten geeft van bloedverlies. Indien dit hevig is kan lokale bestraling overwogen worden.
Pijn
Bij uitgezaaide eierstokkanker komen buikpijn en rugpijn voor. De pijn is meestal niet het gevolg van een lokale tumormassa en daarmee is bestraling als behandeling niet mogelijk. Ook is bestraling van afwijkingen in de buik niet aantrekkelijk omdat door beschadiging van omliggende darmen de kans op diarree groot is.
Pijnstillers zijn de meest aangewezen behandeling, met als eerste stap het starten van paracetamol. Als dit onvoldoende werkt worden sterkere pijnstillers behorend tot de groep van de NSAID’s (zoals diclofenac, naprosyne en etoricoxib) toegevoegd of er wordt gestart met morfine of morfine-achtigen (opioïden) naast paracetamol. Voor de opioïden geldt dat er geen standaarddosering is, maar dat de juiste dosering individueel wordt vastgesteld. Een onderhoudsdosering van langer werkende opioïden wordt gecombineerd met kortwerkende opioïden voor gebruik als de pijn tijdelijk erger is. Bij frequent gebruik van het kortwerkende opioïde kan de onderhoudsdosering omhoog. De belangrijkste bijwerkingen van opioïden zijn obstipatie en verwardheid. Laxeermiddelen worden altijd voor zo nodig voorgeschreven en bij lichte verwardheid kan haloperidol gegeven worden. Als dit onvoldoende helpt moet gekeken worden of de dosering opioïde verlaagd kan worden of dat geswitcht moet worden naar een andere opioïde.
Verminderde eetlust en gewichtsverlies
Verminderde eetlust en gewichtsverlies komen om verschillende redenen vaak voor bij uitgezaaide eierstokkanker. Een aantal redenen is hiervoor genoemd (ascites, obstipatie, ileus, medicatiegebruik). Ze kunnen ook een gevolg zijn van nog niet geheel begrepen mechanismen onder invloed van de gevorderde kanker, het zogenoemde anorexie- cachexiesyndroom. Bestrijden van het gewichtsverlies door kunstmatige voeding is meestal niet zinvol, omdat het gewichtsverlies onvermijdelijk en niet beïnvloedbaar is. Soms worden op proef corticosteroïden gegeven, omdat die de eetlust kunnen bevorderen.
Als dit middel niet werkt, is het belangrijk er na enkele dagen mee te stoppen.
Het is belangrijk te kijken of het lukt weer plezier te krijgen in eten door te eten wat lekker is en door vaker kleine beetjes te eten. Eten heeft een sociale functie en die valt weg als eten niet meer lukt. Dit kan zorgen voor schuldgevoel, omdat genieten van met zorg en liefde klaargemaakt eten niet meer lukt. Bij de partner kan het gevoelens van onmacht geven. Verlies van eetlust is een duidelijke confrontatie met de naderende eindigheid van het leven. Daarbij verandert het uiterlijk door ernstig gewichtsverlies, wat kan leiden tot gevoelens van schaamte en sociale isolatie. Deze opeenvolging van gebeurtenissen wordt wel de cascade of losses genoemd: verlies van plezier in het eten, verlies van de sociale functie van de maaltijden, verlies van gevoel van aantrekkelijkheid, zelfgevoel en identiteit, verlies van de rol van partner of ouder en tot slot verlies van gevoel van controle.
Vermoeidheid
Vermoeidheid komt veel voor bij kanker en veel patiënten vinden het ‘het ergste leed dat kanker veroorzaakt’. Het komt voor in alle stadia van kanker, tijdens de behandeling ervan en ook jaren later klagen mensen die genezen zijn van kanker soms nog over vermoeidheid. Het is heviger dan vermoeidheid na inspanning en verbetert niet na rust of slapen. Het overvalt je van het ene op het andere moment, waardoor je niet meer in staat bent ook maar iets te doen. Je moet daarom steeds afwegen aan welke activiteit je voorrang geeft. Dat belast je dagelijks leven in grote mate, meer nog dan pijn. De kans dat je in een sociaal isolement belandt, is levensgroot.
Verschillende uitingsvormen van vermoeidheid
- Lichamelijke vermoeidheid (je bent niet in staat tot lichamelijke inspanning).
- Mentale vermoeidheid (je hebt moeite met denken en beslissingen nemen).
- Emotionele vermoeidheid (je bent snel geïrriteerd en labiel).
- Verminderde interesse en motivatie.
Vermoeidheid bij kanker is meestal niet te behandelen. Er is weinig bekend van de oorzaak; waarschijnlijk ontstaat het door verschillende factoren. Soms is er sprake van bloedarmoede en af en toe geeft bloedtransfusie verbetering van de vermoeidheid en kortademigheid. Bij een beperkte levensverwachting zijn corticosteroïden het proberen waard. Als dit niet binnen enkele dagen effect heeft, moet die medicatie gestopt worden.
Het belangrijkste is echter dat je vasthoudt aan een dagritme en de balans vindt tussen inspanning en rust. Bepaal je prioriteiten en focus je vooral op wat je nog kunt. Het bijhouden van een dagboek kan hierbij helpen.
In de allerlaatste levensfase (de laatste maand) trekt vermoeidheid niet zo’n zware wissel meer op de kwaliteit van leven. Het kan je dan zelfs bescherming bieden tegen het lijden door klachten als pijn of kortademigheid, ook doordat je meer zult slapen.
Delier
Een delier is een ernstige aandoening waarbij het bewustzijn wisselend gestoord is en er verwardheid of juist apathie optreedt. Een delier ontstaat altijd als gevolg van een lichamelijke aandoening, zoals een infectie, uitdroging, ernstige ziekte, of als bijwerking van medicatie.
Met name opioïden hebben delier als bijwerking.
Het is belangrijk een delier tijdig te onderkennen en maatregelen te nemen. Allereerst moet naar de mogelijke oorzaak voor het ontstaan van een delier gekeken worden. Als het mogelijk is moet dit behandeld of bestreden worden. Als het gebruik van een opioïde de oorzaak is van het delier moet gekeken worden of de dosering verlaagd kan worden of dat het door een andere opioïde vervangen kan worden. Daarnaast is het belangrijk om een rustige omgeving te creëren. Tot slot kan medicatie gegeven worden om het delier te bestrijden. Soms is een delier een uiting dat het lichaam het opgeeft en is herstel niet meer mogelijk. De stervensfase is dan ingetreden; de onrust kan een reden zijn om te beginnen met palliatieve sedatie.
Tekenen dat een delier aan het ontstaan is (prodromen)
- Omkering van dag-en-nachtritme.
- Levendige dromen of nachtmerries (of toename hiervan).
- Voorbijgaande hallucinaties.
- Moeilijkheden met concentreren en helder denken, snelle afleidbaarheid.
- Overgevoeligheid voor prikkels zoals licht en geluid.
- Rusteloosheid, angst, irritatie of juist teruggetrokkenheid met apathie.
- Emotionele labiliteit.
- Desoriëntatie.
De stervensfase
Vaak is er in de dagen voor het overlijden een omslagpunt herkenbaar. Het is dan duidelijk dat het overlijden niet ver weg meer is en dat de stervensfase is ingegaan. Als zorgverleners dit zien, is het belangrijk dat zij dit bespreken zodat bewust afscheid kan worden genomen. Dat heeft veel waarde, ook voor de latere rouwverwerking.
Het is daarnaast belangrijk dat zorgverleners dan bespreken dat kort voor het overlijden de ademhaling hoorbaar (reutelen) of onregelmatig kan worden (Cheyne-Stokesademhaling). Dit is te verklaren door een wegzakkend bewustzijn. Als de naasten dit niet weten kunnen ze het gevoel hebben dat de stervende aan het stikken is.
Soms is er in de laatste levensweek sprake van symptomen die een te grote belasting zijn voor de stervende en die niet te verlichten zijn door behandeling. Dan kan de arts ervoor kiezen om te starten met slaapmedicatie (sedativum) tot het moment van overlijden. Dit heet palliatieve sedatie.
Palliatieve sedatie wordt vaak verward met euthanasie. Beide zijn beslissingen die plaatsvinden rond het levenseinde. Bij palliatieve sedatie overlijdt de stervende door de ziekte. Bij euthanasie overlijdt de patiënt op diens eigen verzoek op een afgesproken moment aan door de arts toegediende medicatie. Palliatieve sedatie valt onder normaal medisch handelen, euthanasie niet.