Geen producten in de winkelwagen.
Parkinson

Er valt heel veel te vertellen over de ziekte van Parkinson, zijn verschijningsvormen en de invloed die de ziekte heeft op het leven van alle betrokkenen. Zowel de patiënt als zijn omgeving vindt in Parkinson en nu? een schat aan betrouwbare informatie geschreven in begrijpelijke taal. Behalve over het ontstaan van de ziekte en het verloop ervan, vertelt het boek de verhalen van velen die kampen met ‘parkinson’. Daardoor bevat het boek vele praktische tips die leven met de ziekte van Parkinson makkelijker maken.
Bestel ons boek over Parkinson
Verschijnselen van de ziekte van Parkinson
Tot een aantal jaren geleden werd de ziekte van Parkinson door neurologen beschouwd als een ziekte die alleen invloed had op het bewegen. Tegenwoordig weten we dat de ziekte veel meer is dan een bewegingsstoornis. Wat de ziekte allemaal inhoudt en wat de symptomen zijn, komt in dit eerste hoofdstuk aan de orde.
Er bestaan veel misvattingen over de ziekte van Parkinson. Enkele jaren geleden wilde de Parkinson Vereniging weten wat het beeld is dat de gemiddelde Nederlander heeft van de ziekte van Parkinson. Het bleek dat de meeste mensen dachten dat deze ziekte alleen maar voorkomt bij ouderen en dat het belangrijkste symptoom bestond uit beven.
Feit is dat de ziekte al op heel jonge leeftijd kan ontstaan en er zelfs een aparte benaming is voor de patiënten die de ziekte tussen hun eenentwintigste en veertigste jaar krijgen: YOPpers (Young-Onset Parkinson’s). Geschat wordt dat tussen de 5 en 10 procent van alle parkinsonpatiënten tot deze categorie behoort.
Gemiddeld openbaart de ziekte zich voor het eerst vooral tussen het veertigste en zestigste levensjaar.
Parkinson komt dus zeker niet alleen bij oudere mensen voor. In totaal lijden op dit moment in Nederland ongeveer 50.000 patiënten aan de ziekte van Parkinson. Dat is gemiddeld drie op de duizend mensen. Dit aantal zal de komende tien tot vijftien jaar toenemen tot 75.000, op basis van de vergrijzing. Op hogere leeftijd komt de ziekte namelijk beduidend vaker voor; boven de zeventig jaar bij ongeveer twee op de honderd mensen.
De ziekte van Parkinson is een langzaam progressieve chronische ziekte, dat wil zeggen dat er (nog) geen vertraging of genezing van de ziekte mogelijk is en iemand dus zijn verdere leven last houdt van de ziekte. Deze last zal vanwege dit langzaam progressieve karakter van de ziekte geleidelijk aan toenemen. Het goede nieuws is echter dat veel symptomen goed behandeld kunnen worden, hetgeen een reden is om regelmatig door specialisten op dit terrein gezien te worden, zodat een optimale behandeling voor een individuele patiënt gekozen kan worden.
Verschijnselen in een notendop
Parkinson is een neurologische ziekte die een grote invloed heeft op het dagelijks leven van patiënten. Wie aan de ziekte lijdt, kan uiteenlopende klachten hebben. De volgende symptomen zijn het bekendst, omdat ze ook voor leken goed herkenbaar zijn:
- het trillen van handen, benen, kin of tong, maar niet van het hoofd (tremor)
- moeite met bewegen en bewegingsarmoede (bradykinesie)
- pijnlijke stijfheid van spieren (rigiditeit)
- een instabiele houding. Dit kan leiden tot evenwichtsproblemen, een voorovergebogen houding, vallen (in het bijzonder als de ziekte al langer aanwezig is), het ‘bevriezen’ van de benen tijdens het lopen, waardoor het voelt alsof de voeten aan de vloer blijven plakken.
Deze verschijnselen komen niet steeds allemaal bij alle patiënten voor. Voor de diagnose (zie ook hoofdstuk 3) moeten ten minste stijfheid samen met bewegingsarmoede en/of tremor aanwezig zijn. Daarnaast zijn er andere symptomen van de ziekte van Parkinson die voor een buitenstaander niet zichtbaar zijn, bijvoorbeeld pijnklachten of moeite met het ophouden van de urine. De ernst van de symptomen en het beloop van de ziekte verschillen van patiënt tot patiënt.
Ook stemmingsstoornissen, slaapstoornissen en geheugen- en concentratiestoornissen kunnen voorkomen. Hierna wordt nader ingegaan op al deze symptomen en de bijbehorende klachten.
Allereerste verschijnselen
Bij goed navragen blijkt dat de ziekte van Parkinson eigenlijk al enkele jaren voordat de diagnose uiteindelijk wordt gesteld, begint. Maar de klachten en symptomen worden eerst meestal niet als zodanig herkend. Deze symptomen worden ook wel pre-motore symptomen genoemd. Het gaat daarbij om vermindering van de reuk, ernstige obstipatie, onrustige bewegingen en hardop praten/schreeuwen ’s nachts.
Ernstige obstipatie
Ernstige obstipatie behoort ook tot de vroege pre-motore symptomen van parkinson, hetgeen te maken heeft met de vertraagde maag-darmlediging, doordat in een vroeg stadium de zenuwen die betrokken zijn bij de beweeglijkheid van maag en darmen, betrokken raken bij het ziekteproces. Ernstige obstipatie behoort ook tot de vroege pre-motore symptomen van parkinson, hetgeen te maken heeft met de vertraagde maag-darmlediging, doordat in een vroeg stadium de zenuwen die betrokken zijn bij de beweeglijkheid van maag en darmen, betrokken raken bij het ziekteproces.
Onrustige bewegingen en hardop praten/schreeuwen ’s nachts
Deze symptomen worden altijd alleen maar opgemerkt door de bedpartner, de patiënten zelf klagen er nooit over. Het onrustige gedrag blijkt vooral op te treden tijdens de droomslaap (ook wel de remslaap genoemd, afgeleid van rapid eye movements, snelle oogbewegingen). Deze droomslaap gaat gepaard met snelle oogbewegingen, hetgeen de enige beweging is die iemand op dat moment normaliter maakt, omdat gezonde personen tijdens deze remslaap volledig verslapt zijn. Bij patiënten met de ziekte van Parkinson ontstaat er een foute schakeling in de hersenstam, waardoor patiënten juist onrustig gaan bewegen en roepen en schreeuwen tijdens deze droomslaap, alsof ze hun dromen uitbeelden. Hierbij wordt
niet zelden de bedpartner betrokken. Deze remslaap gerelateerde gedragsstoornissen hebben een grote voorspellende waarde, omdat het optreden hiervan betekent dat iemand een kans heeft van meer dan 50 procent om binnen tien jaar een hersenziekte te krijgen, waaronder de ziekte van Parkinson. Dit is dus vaak geen onschuldig symptoom, zoals lange tijd is gedacht.
Motorische verschijnselen
De motorische kenmerken van de ziekte van Parkinson zijn in te delen in vijf hoofdgroepen. Voor de diagnose moet iemand ten minste twee van deze kenmerken hebben, waarbij er altijd stijfheid aanwezig moet zijn om de diagnose te mogen stellen (zie ook hoofdstuk 3). Daarbij is het typisch dat de symptomen aan één kant beginnen en aan die zijde ook blijven overheersen. Het is zelfs zo dat als de symptomen symmetrisch voorkomen, dit de diagnose parkinson minder waarschijnlijk maakt.
De vijf belangrijke motorische kenmerken van parkinson zijn: traagheid, stijfheid, tremor, houdings- en balansstoornissen, en loopstoornissen.
Traagheid
Opvallend is dat de bewegingen traag op gang komen. De automatische bewegingen worden minder, zoals het knipperen met de ogen en het slikken. Er moet steeds over nagedacht worden over hoe een beweging gestart moet worden. De bewegingen zijn daardoor minder spontaan.
De bewegingen die eerst vanzelf gingen moeten nu bewust gedaan worden. Allerlei handelingen kosten daarom meer moeite, zoals draaien in bed en het vastmaken van kleine knoopjes. Sommige mensen hebben ook problemen met het op tijd stoppen van de beweging en gaan steeds sneller lopen (dribbelen) waardoor er kans is op botsingen en vallen, ook wel propulsie genoemd. Traagheid en stijfheid gaan vaak hand in hand.
Stijfheid(rigiditeit)
De stijfheid begint vrijwel altijd eenzijdig, met klachten van stijfheid van een arm en/of been. Ook de nekspieren, schouder-, arm- of onderrugspieren kunnen klachten van stijfheid geven. Het kan een zwaar moe en naar gevoel veroorzaken. De stijfheid kan gepaard gaan met pijn en verkramping, afhankelijk van de ernst. Ook de gezichtsspieren kunnen verstijven, waardoor er een strakke gezichtsuitdrukking ontstaat, het zogeheten maskergelaat. Dit maskergelaat wordt vooral bepaald door een verminderd knipperen van de oogleden en een al dan niet openstaande mond.
Het gelaat toont door die strakheid weinig emotie. Het lijkt daardoor vaak alsof een parkinsonpatiënt maar wat voor zich uit zit te staren en niet goed luistert. Dit kan de buitenwereld een heel verkeerde indruk geven.
Tremor
Beven bij parkinson bestaat vooral uit beven in rustpositie, bijvoorbeeld als iemand rustig zit. Daarbij kunnen zowel de armen en benen, alsook de kin en de tong meedoen. Trillen van het hoofd hoort niet typisch bij de diagnose parkinson!
Houdings- en balansstoornissen
Door de stijfheid kan de lichaamshouding veranderen, waarbij de houding voorovergebogen wordt. Daarnaast kan er een gebogen houding optreden van alle ledematen, waardoor de typische houding van iemand met parkinson ontstaat.
De armen worden strak langs het lichaam gehouden, de elleboog en pols zijn een beetje gebogen en bewegen tijdens het lopen niet soepel mee.
Daarnaast kan de balans zijn aangedaan, waardoor er een valneiging ontstaat. Dit uit zich in verstoringen van het evenwicht bij het wisselen van positie, bijvoorbeeld omdraaien of opstaan, of wanneer iemand wordt afgeleid.
Loopstoornissen
Het lopen gebeurt met kleine passen, waarbij de voeten dicht bij elkaar staan, waardoor het lopen schuifelend wordt.
Onbedoelde blokkades tijdens een beweging zijn een ander probleem. Dit fenomeen wordt ook wel bevriezen of ‘freezing’ genoemd. Dit treedt vooral op tijdens draaien, als het patroon van de ondergrond verandert, of wanneer de ruimte zich plotseling vernauwt, zoals bij het naderen van een deuropening.
Als daarentegen de ondergrond waarop gelopen wordt een regelmatig patroon vertoont, kan dit juist freezing voorkomen en een vast looppatroon in gang houden.
Dit wordt soms door patiënten ingezet, door bijvoorbeeld het aanbrengen van strepen met een vaste onderlinge afstand op de grond.
Niet-motorische symptomen
Hoewel de ziekte van Parkinson vooral gezien wordt als een bewegingsstoornis, wordt het meest invaliderende deel van de ziekte veroorzaakt door de niet-motorische problemen, die voor een deel wat minder zichtbaar zijn.
De meest voorkomende niet-motorische symptomen zullen hierna worden besproken.
Spraakproblemen
Soms zijn er al spraakproblemen voordat de diagnose parkinson is gesteld. De stem wordt zachter en de articulatie gaat moeilijker. Ook stotteren en problemen met het vinden van woorden kunnen voorkomen. Daardoor kan er een hapering midden in een zin of verhaal optreden. De stem klinkt vaak hees en de spraak is monotoon. Het spreektempo ligt in het algemeen laag.
Slikproblemen en speekselvloed
In het verloop van de ziekte van Parkinson kunnen kauw- en slikklachten optreden. Het slikken verloopt niet meer automatisch en daardoor kost het meer moeite om het voedsel weg te krijgen. Verslikken komt voor als het voedsel uit de mond in de luchtpijp terechtkomt. Hierdoor kan er een longontsteking ontstaan. Een andere consequentie is het moeilijk weg kunnen slikken van speeksel, waardoor er speekselvloed ontstaat. Speekselvloed ontstaat dus niet door een verhoogde speekselproductie. Speekselvloed wordt versterkt door een verminderde motoriek van de aangezichtsspieren, inclusief de spieren rondom de mond, waardoor het speeksel door de openstaande mond en de voorovergebogen lichaamshouding uit de mond loopt.
Plasproblemen
Ook de werking van de blaas wordt door de ziekte van Parkinson beïnvloed. De aansturing van de blaasspier verloopt niet goed. De spier die de blaas samentrekt, is vaak wat overactief. Hierdoor ontstaat er al een reflex om te plassen als de blaas nog maar zeer ten dele is gevuld. Dit leidt tot een frequente aandrang om te plassen, waarbij er snel aan deze aandrang gehoor moet worden gegeven, omdat anders de blaasspier al samentrekt en de urine afloopt. Dit probleem wordt ook wel urge-incontinentie genoemd.
Ongeveer 75 procent van de parkinsonpatiënten heeft problemen bij het plassen. De problemen zijn uiteenlopend. Het vaak ’s nachts uit bed moeten om te plassen (nycturie) komt vaak al vroeg in het ziekteproces voor. Dit geeft een forse verstoring van de nachtrust.
Als er problemen zijn met het goed ledigen van de blaas en de plasstraal steeds zwakker wordt, is er bij mannen mogelijk sprake van een vergrote prostaat. Dit is een reden om de uroloog te consulteren. Bovendien is het niet goed kunnen legen van de blaas een belangrijke risicofactor voor een blaasinfectie.
Bij vrouwen moet bij problemen met de continentie of bij herhaalde urineweginfecties gedacht worden aan bijvoorbeeld een verzakking van de blaas en/of baarmoeder. Hiervoor kan een uroloog of gynaecoloog geraadpleegd worden.
Het is van groot belang deze klachten goed onder de aandacht van de specialist te brengen, daar problemen met het plassen veel stress veroorzaken. De angst voor urine-incontinentie, of daadwerkelijk ongewild urineverlies, maakt iemand onzeker, hetgeen niet zelden leidt tot sociale isolatie.
Vermoeidheid
Bij de ziekte van Parkinson kost alle inspanning meer energie, onder andere door de traagheid en stijfheid
van de spieren. Vermoeidheid is onderdeel van de ziekte. Het is niet de vermoeidheid na een flinke inspanning. Er zijn diverse factoren die de vermoeidheid kunnen versterken, zoals een stemmingsstoornis, slecht slapen ’s nachts en het gebruik van bepaalde medicijnen, zoals bètablokkers.
Pijn
Pijn komt bij 40 procent van de parkinsonpatiënten voor. De pijnklachten kunnen heel divers zijn en zitten vooral in de spieren en gewrichten. Pijn kan een regelrecht gevolg zijn van de ziekte, maar ook van het uitgewerkt raken van antiparkinsonmedicijnen. Soms kan de pijn verbeterd worden door een betere instelling op anti-parkinsonmedicatie.
Wazig zien/dubbel zien
De oorzaak van wazig zien bij de ziekte van Parkinson wordt niet veroorzaakt door een probleem van de ogen zelf, maar door slechte samenwerking van de oogspieren. Doordat de oogspieren niet goed samenwerken, wordt vooral bij een poging te focussen op voorwerpen dichtbij, zoals bij lezen, geen scherp beeld verkregen. Het verdient aanbeveling om bij deze klacht een opticien of oogarts te bezoeken om andere oorzaken van wazig zien uit te sluiten, zoals staar of netvliesproblemen, dan wel een niet optimale breking van de ooglens, hetgeen wel met een (aangepaste) bril gecorrigeerd kan worden.
Droge ogen
Omdat het knipperen van de oogleden afneemt, bestaat de kans dat de ogen gaan uitdrogen. Oogknipperen is namelijk nodig om het traanvocht regelmatig over de oogbol te verdelen. Te droge ogen kunnen gemakkelijker ontsteken of geïrriteerd raken. Wanneer dat gebeurt, kan het goed zijn om enkele malen per dag ‘kunsttranen’ (methylcelluloseoogdruppels) in de ogen te druppelen.
Ook bij droge ogen ten gevolge van het gebruik van sommige antiparkinsonmiddelen (anticholinergica) kan het gebruik van kunsttranen goed helpen.
Slaapstoornissen
Veel mensen met de ziekte van Parkinson hebben slaapproblemen. Inslapen gaat meestal wel goed.
Deze problemen bestaan vooral uit een gefragmenteerde slaap, waarbij patiënten vaak wakker zijn en korte slaapjes doen van twee tot drie uur.
Daarnaast zijn er andere klachten die de slaap kunnen beïnvloeden, zoals vaak moeten plassen of het niet goed kunnen omdraaien in bed door stijfheid. Niet zelden komen tijdens de slaap daarnaast nog nachtelijke spierschokken (myoclonieën) en ritmische beenbewegingen (Periodic Limb Movements of Sleep, PLMS) voor.
Een bijzonder verschijnsel is een onrustige droomslaap met soms heftige bewegingen en roepen of schreeuwen (remslaap gerelateerde gedragsstoornissen), hetgeen goed behandeld kan worden.
Autonome verschijnselen
Autonome verschijnselen ontstaan als het niet-willekeurige zenuwstelsel het laat afweten. Dat kan gepaard gaan met diverse verschijnselen, zoals:
- lage bloeddruk bij staan (orthostatische hypotensie). Hierbij daalt de bloeddruk fors als iemand gaat staan of lopen, waardoor er duizeligheid, of draaiduizeligheid dan wel vallen en/of bewustzijnsverlies kan optreden. Ook kan de bloeddruk bij zitten of liggen spontaan variëren.
- erectiestoornissen.
- hevig transpireren. Dit komt doordat de normale functie van talg- en zweetklieren in de huid verstoord raakt. Dat leidt tot een toegenomen productie van huidsmeer, waardoor vooral het gezicht opvallend vettig kan zijn. Overmatig transpireren kan ook optreden als gevolg van het uitgewerkt raken van antiparkinsonmedicijnen, of als er extra ongewilde bewegingen ontstaan als gevolg van de medicijninname.
- obstipatie. Als er niet een dagelijkse stoelgang is met een normale samenstelling van de ontlasting is er sprake van obstipatie. Veel patiënten hebben klachten over een vertraagde stoelgang, hetgeen het directe gevolg is van een vertraagde maag-darmbeweeglijkheid door de ziekte van Parkinson. Daarnaast wordt er vaak veel te weinig gedronken (ten minste anderhalve liter per dag) en wordt er te weinig bewogen, waardoor de obstipatie alleen maar erger wordt.
Cognitieve stoornissen/dementie
Bij de ziekte van Parkinson komen ook veranderingen in geheugen, aandacht, planning en ruimtelijk inzicht voor, die worden samengevat onder de term cognitieve stoornissen. Als deze cognitieve stoornissen leiden tot steeds meer problemen in de uitvoering van allerlei dagelijkse taken, zoals wassen, aankleden en eten, kan de diagnose dementie worden gesteld. Uiteindelijk wordt bij meer dan 60 procent van alle patiënten met de ziekte van Parkinson de diagnose parkinsondementie (PDD) gesteld.
Daarbij is het opvallend dat patiënten met vooral stijfheid en traagheid een grotere kans hebben op parkinsondementie in vergelijking met tremor-dominante patiënten. PDD moet echter niet verward worden met alzheimer, dat heel andere verschijnselen heeft. Veel patiënten met de ziekte van Parkinson ervaren al cognitieve veranderingen vanaf het begin van de ziekte, maar dan nog in een milde vorm. Vooral het niet meer kunnen uitvoeren van verschillende taken tegelijk (‘multitasking’), traagheid, en moeilijk kunnen switchen van de ene naar de andere taak zijn problemen die dan vaak al aanwezig zijn. Deze komen bijvoorbeeld naar voren bij een complexe handeling zoals autorijden.
Hieronder worden de belangrijkste cognitieve klachten en symptomen nog wat nader omschreven.
- Vergeetachtigheid, met name problemen met het kortetermijngeheugen.
- Planningsproblemen, zich vooral uitend in problemen met een vloeiende spraak en moeite met omschakelen van de ene taak naar een andere. Dat omschakelen is nodig wanneer men tijdens een gesprek plotseling even op iemand anders moet reageren.
- Verminderde aandacht, vooral het richten van de aandacht op een bepaalde bezigheid kost moeite. Ook het vasthouden, het verdelen en het verplaatsen van aandacht kost moeite. In grotere gezelschappen waar de gespreksonderwerpen snel wisselen, is het moeilijk de draad van het verhaal vast te houden.
- Verminderd ruimtelijk inzicht, waardoor het bijvoorbeeld moeite kost om afstanden te schatten (bijvoorbeeld tussen traptreden) of een kubus na te tekenen.
- Hallucinaties, wanen en illusionaire vervalsingen
Hallucinaties zijn waarnemingen (zien, ruiken, horen en/of voelen) die niet berusten op de werkelijkheid. De hallucinaties bij de ziekte van Parkinson zijn meestal in het begin niet angstaanjagend, maar worden wel als zeer vervelend ervaren. Hallucinaties kunnen zich uitbreiden met denkbeelden die niet op de werkelijkheid berusten. Dit worden wanen genoemd. Veel wanen leiden tot achterdocht. Een illusionaire vervalsing berust op het verkeerd interpreteren van beelden die ook door anderen kunnen worden waargenomen.
Als hallucinaties optreden, moet altijd gedacht worden aan provocerende factoren zoals uitdroging en infectie.
- Depressie
Bij een depressie is er sprake van een allesoverheersende neerslachtigheid, waarbij iemand geen plezier meer beleeft aan de normale activiteiten. Daarnaast zijn er vaak slaapstoornissen, een verminderde eetlust, alsmede een gevoel van minderwaardigheid en een algeheel gevoel van malaise en futloosheid. Daarbij kunnen er ook allerlei vage lichamelijke klachten ontstaan.
Een depressie komt regelmatig voor bij de ziekte van Parkinson, maar wordt niet altijd tijdig herkend. Soms is een depressie het eerste teken dat iemand aan de ziekte lijdt. Ook later in het ziekteproces kan een depressie optreden.
- Impulsief gedrag
Impulscontrolestoornissen kunnen zich op verschillende manieren uiten, bijvoorbeeld als gok-, seks- of koopverslaving. Vooral jonge mannelijke patiënten lijken het grootste risico te lopen, mede onder invloed van bepaalde medicijnen, zoals dopamine-agonisten.
- Angst
Angst kan zich op diverse manieren uiten. Patiënten zijn vaak snel nerveus en prikkelbaar, hetgeen gepaard gaat met opstandig of agressief gedrag. Vooral drukte en lawaai kunnen dit uitlokken. De angst kan ook sterk samenhangen met de inname van medicijnen en kan dan vooral optreden als ‘off-periode’-fenomeen.
- Excessieve slaperigheid overdag
Als de aandacht overdag te wensen overlaat, kan dit leiden tot snel in slaap vallen, als er geen prikkels van buitenaf aanwezig zijn. De aandacht als voorwaarde voor bewuste waarneming is dan te laag, waardoor iemand in slaap valt.
Parkinson Monitor
Om alle symptomen goed in kaart te brengen heeft de Parkinson Vereniging de Parkinson Monitor ontwikkeld. Door deze monitor in te vullen, kunt u uw dagelijks functioneren vastleggen. Samen met uw behandelend arts kunt u zo volgen hoe het met u gaat. De Parkinson Monitor is bedoeld om de communicatie tussen u en uw behandelaar te vereenvoudigen. U vindt de monitor op www.parkinson-vereniging.nl.
Behalve de Parkinson Monitor zijn er nog diverse andere mogelijkheden door lokale ziekenhuizen ontworpen om uw klachten in kaart te brengen.
Samenvatting
Gemiddeld lijden in Nederland drie op de duizend mensen aan de ziekte van Parkinson, en dat zijn niet alleen oudere mensen. Het is een neurologische ziekte die veel invloed kan hebben op het leven van de patiënten. Vaak begint de ziekte al enkele jaren voordat de diagnose wordt gesteld, maar de klachten in die eerste fase – vermindering van de reuk, ernstige obstipatie en onrustige bewegingen en hardop praten/schreeuwen ’s nachts – worden dan meestal niet herkend. De vijf belangrijke motorische kenmerken van parkinson zijn: traagheid, stijfheid (als de gezichtsspieren verstijven is er sprake van een maskergelaat), tremor, houdings- en balansstoornissen, en loopstoornissen (de patiënt schuifelt en er kunnen onbedoelde blokkades optreden, het zogeheten freezing, bevriezen). Daarnaast zijn er de niet-motorische symptomen, die voor een deel wat minder zichtbaar zijn: spraakproblemen, slikproblemen en speekselvloed, plasproblemen, vermoeidheid, pijn, wazig zien, droge ogen, slaapstoornissen, autonome verschijnselen (lage bloeddruk bij staan, erectiestoornissen, hevig transpireren, obstipatie), cognitieve stoornissen/dementie, hallucinaties, wanen en illusionaire vervalsingen, depressie, impulsief gedrag, angst en excessieve slaperigheid overdag.
Samenvatting
Gemiddeld lijden in Nederland drie op de duizend mensen aan de ziekte van Parkinson, en dat zijn niet alleen oudere mensen. Het is een neurologische ziekte die veel invloed kan hebben op het leven van de patiënten. Vaak begint de ziekte al enkele jaren voordat de diagnose wordt gesteld, maar de klachten in die eerste fase – vermindering van de reuk, ernstige obstipatie en onrustige bewegingen en hardop praten/schreeuwen ’s nachts – worden dan meestal niet herkend. De vijf belangrijke motorische kenmerken van parkinson zijn: traagheid, stijfheid (als de gezichtsspieren verstijven is er sprake van een maskergelaat), tremor, houdings- en balansstoornissen, en loopstoornissen (de patiënt schuifelt en er kunnen onbedoelde blokkades optreden, het zogeheten freezing, bevriezen). Daarnaast zijn er de niet-motorische symptomen, die voor een deel wat minder zichtbaar zijn: spraakproblemen, slikproblemen en speekselvloed, plasproblemen, vermoeidheid, pijn, wazig zien, droge ogen, slaapstoornissen, autonome verschijnselen (lage bloeddruk bij staan, erectiestoornissen, hevig transpireren, obstipatie), cognitieve stoornissen/dementie, hallucinaties, wanen en illusionaire vervalsingen, depressie, impulsief gedrag, angst en excessieve slaperigheid overdag.
Ontstaan van de ziekte van Parkinson
De ziekte van Parkinson ontstaat doordat er in de hersenen een abnormale stapeling van eiwitten plaatsvindt die ervoor zorgt dat er zenuwcellen afsterven. Maar waarom gaan die eiwitten eigenlijk stapelen? Op die vraag wordt in dit tweede hoofdstuk een antwoord gegeven.
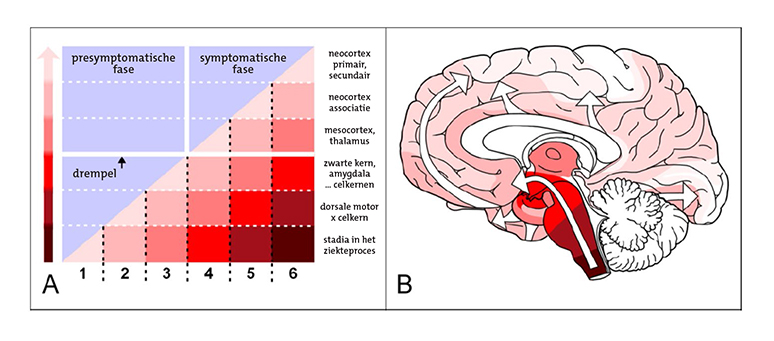
Figuur 1: De stadia die te onderscheiden zjn in de ziekte van Parkinson.
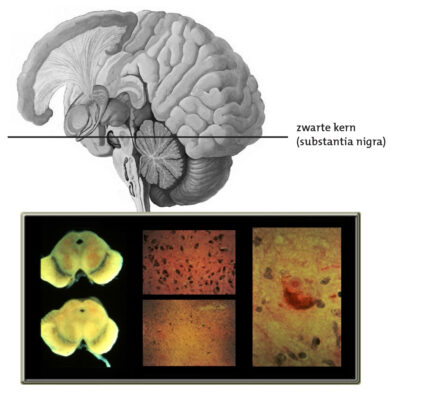
Figuur 2: Substantia nigra (zwarte kern) in de hersenstam.
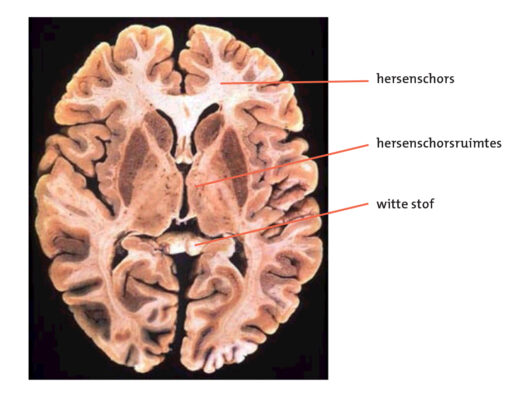
Figuur 3: Basale kernen van bovenaf gezien.
De ziekte van Parkinson ontstaat door een abnormale stapeling van het eiwit alfa-synucleïne, die uiteindelijk de zenuwfunctie verstoort doordat de zenuwcellen door deze eiwitten afsterven. Dit proces begint laag in de hersenstam (zie figuur 1) en breidt zich vandaar geleidelijk aan uit over de hoger gelegen delen van de hersenstam en doet uiteindelijk ook de grote hersenen aan.
Een van de zenuwcelkernen, de zwarte kern (substantia nigra), wordt in dit proces vrij vroeg aangedaan. De zwarte kern, die zwart is omdat deze een zwart pigment bevat (zie figuur 2), bestaat uit zenuwcellen die dopamine produceren en vervolgens afgeven aan andere belangrijke zenuwcellen in de basale kernen, die midden in de grote hersenen gelegen zijn (zie figuur 3).
Dopamine is een neurotransmitter, een boodschapper, die signalen tussen zenuwcellen kan doorgeven. De dopamine wordt eerst afgegeven in een ruimte tussen de zenuwcellen, de synaps, en hecht zich dan aan dopaminereceptoren van andere zenuwcellen, als een sleutel die in het slot past, waarmee een signaal aan die zenuwcel wordt doorgegeven (zie figuur 4).
De basale kernen (of basale ganglia) functioneren daarbij als een soort schakelcentrum. De basale kernen zijn onder andere betrokken bij de uitvoering van bewegingen en bij het handhaven van de houding. Daarnaast regelen de basale kernen de rustspanning in de spieren. De basale kernen doen dit in samenwerking met de hersenschors, waar het uiteindelijke commando om te bewegen of te veranderen van beweging vandaan komt. Er is een constante stroom van informatie en terugkoppeling van informatie tussen de hersenschors, de basale kernen en de hersenstam (zie figuur 5).
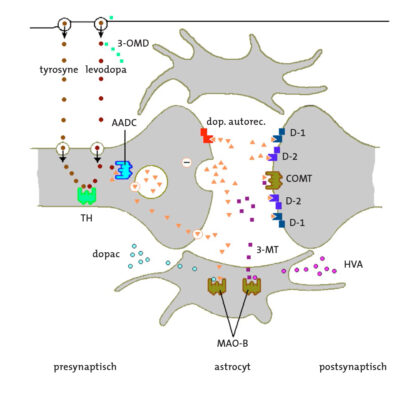
Figuur 4: Dopaminereceptor/synaps
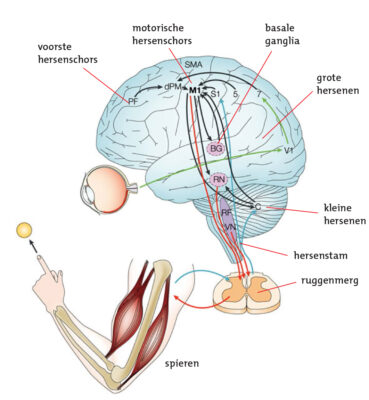
Figuur 5: De relatie tussen hersenschors, kleine hersenen en de uiteindelijke aansturing van beweging.
Basale kernen en aangeleerde bewegingen
Bij elke beweging die we maken, zijn verschillende spieren betrokken, die in de juiste volgorde, en met de juiste snelheid in actie moeten komen. De meeste van deze bewegingen voeren we vrijwel automatisch uit, zonder dat we bij elke spierbeweging moeten nadenken hoe en in welke volgorde het moet. Dat is eenmaal geleerd door hard te oefenen, bijvoorbeeld bij het aanleren van lopen, fietsen en/of tennissen. Zolang de basale kernen goed functioneren, is het uitvoeren van dergelijke aangeleerde handelingen geen probleem. Een van de belangrijkste neurotransmitters in de basale kernen is dopamine. Als de dopamine-aanwezigheid in de synaps met meer dan 50 procent daalt, gaat de normale beweeglijkheid verloren, en worden de eerste verschijnselen van de ziekte van Parkinson merkbaar.
Kleine hersenen en de timing van beweging
De kleine hersenen werken samen met de hersenschors om een beweging in tijd en ruimte goed te kunnen plaatsen. Dat betekent bijvoorbeeld dat bij het vastpakken van een kopje, dat kopje niet wordt omgestoten, maar vloeiend wordt vastgepakt en leeggedronken.
Informatieoverdracht door neurotransmitters
In elk zenuwceluiteinde bevinden zich kleine blaasjes met daarin een kleine hoeveelheid neurotransmitter. Wanneer er een zenuwimpuls door de zenuw loopt en het uiteinde bereikt, zullen die blaasjes openspringen en komen de neurotransmitters via de wand van het zenuwceluiteinde, in de synaps. Op het oppervlak van elke naastgelegen zenuwcel bevinden zich de zogeheten receptoren (ontvangers). Die geven, zodra ze met een bij hen passende neurotransmitter in aanraking komen, een stroompje af, waarna het signaal verder wordt doorgegeven.
Wanneer het signaal is doorgegeven, wordt de ‘gebruikte’ neurotransmitter weer opgenomen door een transporteiwit in de celwand van de zenuwcel die de transmitter had afgegeven, om opnieuw te worden hergebruikt.
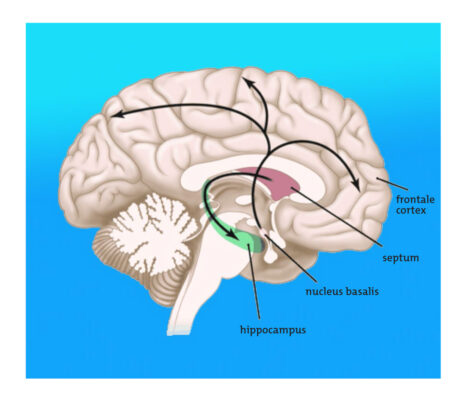
Figuur 6: Cholinerge zenuwvezels naar de hersenschors.
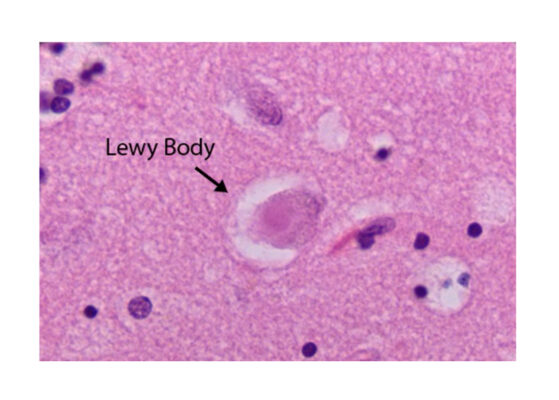
Figuur 7: Lewy-lichaampjes.
Minder productie van andere neurotransmitters
Als de ziekte voortschrijdt, worden behalve de zwarte kern ook andere kernen in de hersenstam aangetast door de genoemde stapeling van eiwitten, waardoor ook andere neurotransmitters, zoals serotonine, acetylcholine (zie figuur 6) en noradrenaline, minder geproduceerd worden en het contact met de basale kernen en de hersenschors verslechtert.
Acetylcholine is vooral betrokken bij geheugen- en aandachtsprocessen; (nor)adrenaline, dat onder andere de bloeddrukregulatie verzorgt, speelt ook een rol bij het regelen van onze stemming; en serotonine, is van belang bij het regelen van emoties en stemming.
Zo ontstaan er dus behalve de problemen met het goed uitvoeren van bewegingen ook klachten over de stemming, over de bloeddrukhandhaving bij staan en van het geheugen en de aandacht. En dat verklaart waarom parkinson veel meer is dan alleen een bewegingsstoornis.
De grote verschillen die de diverse patiënten ervaren in hun symptomen hebben alles te maken met de mate waarin de neurotransmitters niet meer worden aangemaakt. Waardoor deze verschillen uiteindelijk veroorzaakt worden, is nog onbekend.
Een kijkje in de hersenen
Als iemand de ziekte van Parkinson heeft, moet er dus een ongewone stapeling van het eiwit alfa-synucleïne te zien zijn in de hersenen. En dat is ook zo: het meest karakteristieke kenmerk bij de ziekte van Parkinson is de aanwezigheid van de zogeheten Lewy-lichaampjes (die zijn genoemd naar de ontdekker ervan) in de hersenen. Deze Lewy-lichaampjes (zie figuur 7) bevatten namelijk alfa-synucleïne. Als er dus Lewy-lichaampjes in de hersenen gevonden worden, kan met zekerheid worden vastgesteld dat het om de ziekte van Parkinson gaat. Hersenweefsel kan echter pas verkregen worden na het overlijden, dus dat helpt niet om tijdens leven de diagnose met zekerheid te stellen.
Rol van alfa-synucleïne
De rol van alfa-synucleïne bij patiënten met parkinson is tot op heden niet duidelijk. Wat wel duidelijk is, is dat dit eiwit gaat stapelen, omdat het niet normaal wordt afgebroken. Een fout in het alfa-synucleïne-gen in een grote Italiaans-Amerikaanse familie was de eerste aangetoonde erfelijke afwijking, die voldoende was om de ziekte van Parkinson van generatie op generatie door te geven. Inmiddels is er nog een aantal monogenetische vormen van parkinson beschreven. Hierbij zorgt een afwijking in slechts één gen ervoor dat de ziekte overerft van de ene naar de andere generatie. Slechts bij 5 procent van alle parkinsonpatiënten wordt de ziekte door een afwijking in één gen veroorzaakt, waardoor de kans dat nakomelingen van deze patiënten de ziekte overerven, varieert van 25 tot 50 procent. Maar bij het overgrote deel van de patiënten bepalen waarschijnlijk diverse kleine afwijkingen in het genoom, de single nucleotide polymorfisms (SNP’s), met elkaar of iemand wel of niet de ziekte krijgt (zie figuur 8).

Figuur 8: Afwijkingen van het genoom bij parkinsonpatiënten in Nederland.
Onderzoek naar oorzaak
De afgelopen decennia is er het nodige onderzoek gedaan naar het ontstaan van de ziekte van Parkinson. Uit dat onderzoek zijn zeer veel aanwijzingen gekomen dat er waarschijnlijk niet een enkelvoudige oorzaak is aan te wijzen bij de meeste patiënten. De ziekte van Parkinson wordt veroorzaakt door diverse factoren, die er samen voor zorgen dat iemand uiteindelijk de ziekte krijgt. Hierna zal een aantal mogelijke risicofactoren en mogelijke oorzaken de revue passeren.
Erfelijkheid
Wanneer er iemand in de familie aan de ziekte van Parkinson lijdt, is het begrijpelijk dat andere familieleden zich afvragen of deze ziekte erfelijk is. De ervaring leert namelijk dat ongeveer 15 procent van alle parkinsonpatiënten één of meer familieleden heeft met dezelfde ziekte. De kans om de ziekte te krijgen, is ongeveer driemaal groter bij mensen die een eerstegraads familielid (vader, moeder, broer of zus) hebben met de ziekte van Parkinson (2,4 procent in plaats van 0,8 procent). Dit risico is met name verhoogd als het gaat om een vroeg beginnende ziekte van Parkinson; bij een begin voor het vijfenvijftigste jaar is dit risico zelfs 5 tot 8 procent. Door onderzoek naar familiaire vormen van de ziekte van Parkinson is van elf genen hun rol bij het ontstaan van de ziekte van Parkinson vastgesteld. Daarnaast zijn er diverse kleine veranderingen vastgesteld (mutaties) die een bijdrage lijken te leveren aan het ontstaan. Bij het eerst ontdekte parkinsongen in 1997, PARK1, bleek een fout in het alfa-synucleïne-gen de oorzaak te zijn van een autosomaal dominant overervende vorm van parkinson. Sindsdien zijn er ook andere genetische typen gevonden, die genummerd zijn in volgorde van ontdekking: PARK2, PARK3 enzovoort (zie figuur 9). Van een aantal parkinsongenen is de functie van het eiwit min of meer bekend en daaruit blijkt dat het om uiteenlopende functies gaat. In sommige gevallen betreft het een rol bij de functie van mitochondria, die de energie voor de cellen leveren. In andere gevallen gaat het om een functie bij de vorming van blaasjes die de neurotransmitters moeten opslaan en afgeven in de synaps. Bij de huidige stand van zaken is genetisch onderzoek niet zinvol bij mensen die op latere leeftijd de ziekte van Parkinson krijgen en bij wie geen andere familieleden zijn aangedaan.
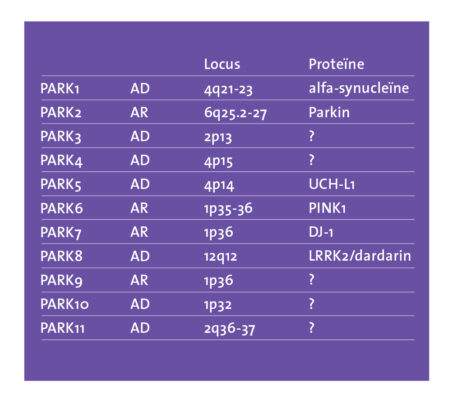
Figuur 9: Hereditair parkisonisme.
Bestrijdingsmiddelen
De heer B. was een bollenkweker van 58 jaar, die volgens zijn familie de laatste jaren alsmaar trager was geworden. Ook was het opgevallen dat twee buren in dezelfde straat, eveneens bollenkwekers, dezelfde klachten hadden. Een van deze buren had inmiddels de huisarts bezocht, die hem had verwezen naar de neuroloog. Die had al tijdens het eerste consult de diagnose ziekte van Parkinson gesteld. Er was gevraagd of dit ook in zijn familie voorkwam, maar dat was niet het geval.
Hierop werd de heer B. ook verwezen naar de neuroloog. Tijdens het consult vroeg de neuroloog naar het gebruik van bestrijdingsmiddelen. De heer B. vertelde dat hij die jaren achtereen onbeschermd had gebruikt. De echtgenote en kinderen van de heer B. vertelden daarna dat hij regelmatig letterlijk geel en groen zag bij thuiskomst, omdat hij hele dagen in de weer was geweest met bestrijdingsmiddelen. Dit was al jaren aan de gang en nooit had hij hier enige last van gehad. Bovendien deed iedereen in de omgeving dit, voor zover bekend zonder problemen. Na enkele jaren bleek dat de ziekte van Parkinson veel vaker voorkwam in de streek waar de heer B. woonde. Ook werd internationaal bekend dat het zeer waarschijnlijk is dat het gebruik van gewasbestrijdingsmiddelen een sterk verhoogde kans geeft op de ziekte van Parkinson.
Omgevingsfactoren
Dat erfelijkheid niet de enige factor is die bepaalt of iemand wel of niet de ziekte van Parkinson krijgt, blijkt bijvoorbeeld uit onderzoek onder eeneiige tweelingen, van wie vaak slechts één van beiden door de ziekte getroffen bleek te zijn. Een ander bewijs voor de rol van omgevingsfactoren is het ontstaan van Parkinson na vergiftiging met de heroïne-achtige stof MPTP en het voorkomen van parkinsonverschijnselen bij mijnwerkers in mangaanmijnen. Tegenwoordig neemt men dus aan dat er bij het ontstaan van de ziekte van Parkinson zowel erfelijke als omgevingsfactoren een rol spelen, naast verouderingsprocessen. Het is aannemelijk dat het aandeel van de verschillende factoren bij iedereen met de ziekte van Parkinson verschillend is.
Invloed van de westerse wereld
In geïndustrialiseerde landen komt de ziekte van Parkinson duidelijk vaker voor dan in ontwikkelingslanden. Sinds de jaren vijftig van de vorige eeuw neemt het aantal parkinsonpatiënten in de westerse wereld zelfs toe. Dat pleit voor de opvatting dat er schadelijke invloeden vanuit de omgeving zijn die het ontstaan van de ziekte van Parkinson bij daarvoor gevoelige mensen kunnen bevorderen. Daarvoor zijn inmiddels diverse aanwijzingen gevonden, zoals het voorkomen van de ziekte van Parkinson bij mensen die veel contact hebben gehad met bepaalde gewasbestrijdingsmiddelen, bijvoorbeeld paraquat. In Nederland vindt onderzoek plaats naar de relatie tussen omgevingsfactoren, zoals het gebruik van pesticiden, en het vóórkomen van parkinson. Al langer is namelijk bekend dat parkinson in landbouwgebieden vaker voorkomt dan in stedelijke gebieden. De vraag is echter of dit te wijten is aan het gebruik van pesticiden of dat hieraan ook andere factoren bijdragen.
Invloed van chronische ontstekingen
Een mogelijk belangrijke bijdrage aan het ontstaan van de ziekte van Parkinson is het (frequent) optreden van bepaalde infecties, die in de hersenen een steriele ontstekingsreactie kunnen veroorzaken, waardoor mogelijk zenuwcellen afsterven. Dit heeft in diermodellen al geleid tot verlies van zenuwcellen in de zwarte kern.
In dit kader wordt ook gekeken naar het effect van infecties op het ontstaan en de progressie van de ziekte van Parkinson, omdat bekend is dat patiënten vaak tijdelijk verslechteren als ze een infectie doormaken. Maar de effecten van frequente infecties bij gezonde mensen zijn nog onduidelijk.
Is roken gezond?
Mensen die roken blijken minder vaak de ziekte van Parkinson te krijgen dan niet-rokers. Dit is een interessant gegeven dat steeds weer uit diverse onderzoeken naar voren komt. Met andere woorden: patiënten die de ziekte van Parkinson krijgen, hebben gemiddeld veel minder of niet gerookt. Hetzelfde geldt ook voor het drinken van koffie, waarbij vooral de duur van het roken en koffiedrinken van belang is, veel meer dan de hoeveelheid. Dit verband is niet gevonden voor het drinken van alcohol. Er zijn verschillende verklaringen mogelijk.
Roken stimuleert de nicotinereceptor, die beschermend zou kunnen werken op processen die de celafbraak sturen. Een andere verklaring is dat er bij rokers meer antioxidanten ontstaan, die de cel beschermen tegen afbraak. Overigens zijn deze gegevens geen stimulans om te gaan roken. De gezondheidsrisico’s van roken in brede zin overtreffen namelijk de bescherming tegen de ziekte van Parkinson vele malen!
De stofwisseling als mogelijke oorzaak
Recent is aan de mogelijke oorzaken van de ziekte van Parkinson nog een bijzondere oorzaak toegevoegd: een fout in de stofwisseling, die op celniveau leidt tot stapeling van bepaalde stoffen. Het gaat hierbij om een zeldzame stofwisselingsziekte, de ziekte van Gaucher, die in een bepaalde vorm, door het niet goed functioneren van het enzym glucocerebrosidase (GBA) kan leiden tot de ziekte van Parkinson. Hier wordt nu veel onderzoek naar gedaan; deze variant komt vooral voor bij Joodse families.
Samenvatting
In de hersenen liggen de basale kernen en zolang die goed werken, kunnen mensen hun aangeleerde handelingen uitvoeren. Dopamine is een van de belangrijkste neurotransmitters, boodschappers, in die basale kernen. Als de dopamine-aanwezigheid echter met meer dan 50 procent daalt, gaat de normale beweeglijkheid verloren en worden de eerste verschijnselen van de ziekte van Parkinson merkbaar. Die dopaminedaling wordt veroorzaakt door een abnormale stapeling van eiwitten, de zogeheten alfa-synucleïnes, in de hersenen. Als de ziekte voortschrijdt, zorgt de stapeling van die eiwitten ervoor dat ook andere neurotransmitters, zoals serotonine, acetylcholine en noradrenaline, minder worden geproduceerd. Zo ontstaan er niet alleen problemen met bewegen maar ook klachten over de stemming, de bloeddrukhandhaving bij staan en het geheugen en de aandacht. Dat verklaart waarom parkinson veel meer is dan alleen een bewegingsstoornis. De grote vraag is natuurlijk waarom dit eiwit gaat stapelen. Het antwoord daarop is vooralsnog lastig: erfelijke maar ook andere factoren spelen een rol.
Het stellen van de diagnose
Het is niet eenvoudig om de diagnose ziekte van Parkinson te stellen, omdat er aanvankelijk sprake is van vage en onduidelijke klachten. Bovendien kan geen enkele test volledige zekerheid verschaffen. Hoe een arts toch tot een (waarschijnlijkheids)diagnose komt, wordt in dit derde hoofdstuk uit de doeken gedaan.
De ziekte van Parkinson wordt niet altijd goed herkend, omdat de beginklachten vaag en onduidelijk kunnen zijn. De gemiddelde duur tussen het aanwezig zijn van de eerste verschijnselen en het stellen van een diagnose ligt rond de vijf jaar. De diagnose kan wat sneller worden gesteld als tremor tot de beginsymptomen behoort, omdat er dan sneller aan de ziekte van Parkinson wordt gedacht.
De diagnose ziekte van Parkinson is primair een klinische diagnose. Dat wil zeggen dat de specialist de diagnose stelt aan de hand van typische klachten en verschijnselen met een typisch beloop in de tijd, op basis van een interview en het neurologisch onderzoek in de spreekkamer. Zoals al in hoofdstuk 1 aangegeven, komen de verschijnselen niet steeds allemaal bij alle patiënten voor. Voor de diagnose moet ten minste stijfheid samen met bewegingsarmoede en/of tremor aanwezig zijn.
Er bestaat geen enkele test die tijdens het leven met 100 procent zekerheid de ziekte van Parkinson kan vaststellen. Dit is alleen mogelijk als na het overlijden van de patiënt de hersenen onder een microscoop bekeken worden. Zelfs de meest ervaren specialist moet het tijdens het leven dus doen met een waarschijnlijkheidsdiagnose. Gelukkig zijn artsen steeds beter in staat de juiste diagnose te stellen. Zo misten parkinsonexperts in een onderzoek 6 procent van de patiënten die achteraf de ziekte van Parkinson bleken te hebben. Hoe langer de ziekte bestaat, hoe gemakkelijker het wordt om de diagnose te stellen.
De diagnose parkinson dient gesteld te worden door een specialist met specifieke kennis en ervaring op het gebied van deze ziekte, zoals een neuroloog. Een patiënt kan natuurlijk vragen naar een neuroloog met speciale belangstelling voor en ruime ervaring met de ziekte van Parkinson.
Medisch onderzoek
MRI-scan
In Nederland is afgesproken dat iedereen met de verdenking op de ziekte van Parkinson ten minste eenmaal een MRI-scan van het hoofd moet krijgen om andere mogelijke oorzaken voor dezelfde klachten uit te sluiten. Mogelijke andere oorzaken zijn:
- doorbloedingsproblemen van de hersenen (vasculair parkinsonisme);
- een waterhoofd (hydrocefalus). Dit is een hersenaandoening waarbij de hersenkamers die het hersenvocht bevatten zijn uitgezet;
- aan parkinson verwante ziekten (de bijlage ‘Atypische vormen van parkinsonisme’).
- Op basis van zo’n MRI van de hersenen kan echter op dit moment nog niet de diagnose parkinson worden gesteld.
DAT-SPECT-scan
Als er twijfel bestaat of er sprake is van parkinsonisme, kan een DAT-SPECT-scan of een F-Dopa PET-scan van de hersenen gemaakt worden.
De F-Dopa PET-scan kan maar in enkele ziekenhuizen worden gemaakt. Daarmee wordt onderzocht of er een verlaagde afgifte van dopamine in de basale kernen aanwezig is. Dit is onder andere het geval bij de ziekte van Parkinson, maar ook andere vormen van parkinsonisme kunnen deze verlaagde afgifte van dopamine tonen. Daarom is dit onderzoek vooral zinnig als er getwijfeld wordt aan de aanwezigheid van parkinsonistische verschijnselen. Een DAT-SPECT-scan is een functieonderzoek van de hersenen waarbij gebruikgemaakt wordt van een radioactieve stof die zich hecht aan het eiwit dat dopamine transporteert uit de zenuwcel in de ruimte tussen zenuwcellen (synapsen). De dosis radioactieve stof is echter zo laag dat dit niet schadelijk is. Hiermee is er een indirecte maat voor het aantal nog functionerende zenuwcellen die dopamine maken. Een dopaminetekort is een belangrijk kenmerk van de ziekte van Parkinson.
Bij de meeste patiënten is het niet nodig om een DAT-SPECT-scan te maken. Het klinische beeld en de reactie op de therapie geven vaak al een goede indicatie van de aanwezigheid van een dopaminetekort in de hersenen.
Er zijn verschillende redenen om toch een DAT-SPECT-scan te maken:
- als er twijfel is over de diagnose;
- als de arts twijfelt aan de oorzaak van een tremor;
- als de arts vermoedt dat de patiënt verschillende aandoeningen naast elkaar heeft, bijvoorbeeld de ziekte van Parkinson gecombineerd met een slechte doorbloeding van de hersenen (vasculair parkinsonisme) of de ziekte van Parkinson gecombineerd met medicamenteus geïnduceerd parkinsonisme, waarbij parkinsonsymptomen worden veroorzaakt door het gebruik van bepaalde medicijnen.
FDG-PET-scan
Als er getwijfeld wordt tussen de diagnose ziekte van Parkinson of atypisch parkinsonisme kan besloten worden een FDG-PET-scan van de hersenen te maken. FDG-PET is de afkorting van fluor-de-oxyglucose positron-emissie-tomografie. Het is een techniek die gebruikmaakt van suiker (glucose) dat gekoppeld wordt aan een stof die een lage dosis straling uitzendt (fluor 18). Dit zegt iets over de stofwisseling van de hersenen. Hoe meer straling wordt opgevangen, hoe meer suiker er wordt gebruikt en hoe actiever dat hersendeel dan is. Een FDG-PET-scan wordt alleen gedaan in daarvoor gespecialiseerde centra.
Transcraniële echografie
Transcraniële echografie is een vorm van onderzoek waarbij een echo van de hersenen wordt gemaakt via het dunne schedelbot van de slaap. Om uit te zoeken of een patiënt lijdt aan de ziekte van Parkinson of aan een vorm van atypisch parkinsonisme kan de neuroloog een transcraniële echo aanvragen. Dit onderzoek wordt nog niet routinematig uitgevoerd, maar alleen in een aantal specialistische centra die veel ervaring met deze techniek hebben.
Neuropsychologisch onderzoek
Als er een vermoeden is van cognitieve functiestoornissen (zie hoofdstuk 1), kan er een aanvullend neuropsychologisch onderzoek gedaan worden. De testen in dit onderzoek zijn vooral gericht op de vier belangrijkste cognitieve functiestoornissen die aanwezig kunnen zijn bij de ziekte van Parkinson, te weten het geheugen, de aandacht, de planning en het ruimtelijk inzicht.
Klinisch neurofysiologisch onderzoek
Dit is onderzoek waarbij het zenuwstelsel wordt doorgemeten. Voorbeelden hiervan zijn slaap- of tremorregistratie en het doormeten van het autonome zenuwstelsel. In het laatste geval worden onder meer de effecten van houdingsverandering op de bloeddruk en van persen op het hartritme geregistreerd.
Genetisch onderzoek
Over het algemeen is genetisch onderzoek niet noodzakelijk. De kans op een mogelijke genetische oorzaak is het grootst bij patiënten bij wie de eerste klachten ontstaan op jonge leeftijd, vooral onder de veertig jaar, of waarbij de verschijnselen niet typisch passen bij de ziekte van Parkinson, dan wel als er verscheidene eerstegraads familieleden met de ziekte van Parkinson zijn. In die gevallen kan genetisch onderzoek wel worden overwogen.

Figuur 10: Meerwaldtkaart.
Samenvatting
Het stellen van de juiste diagnose bij de ziekte van Parkinson is niet eenvoudig. In eerste instantie is er sprake van onduidelijke klachten. Er kunnen soms jaren verstrijken tussen de eerste verschijnselen en de uiteindelijke diagnose. Die diagnose is primair klinisch, dat wil zeggen dat de specialist de diagnose stelt aan de hand van de klachten en verschijnselen, op basis van een interview en neurologisch onderzoek in de spreekkamer. Voor de diagnose moet er behalve van stijfheid ook sprake zijn van bewegingsarmoede en/of tremor. Er bestaat namelijk geen enkele test die met 100 procent zekerheid kan vaststellen dat er sprake is van Parkinson. Dat kan eigenlijk alleen via microscopisch onderzoek na overlijden. Bij leven moet de patiënt het dus doen met een waarschijnlijkheidsdiagnose. Maar gelukkig zijn artsen daartoe steeds beter in staat, mede doordat er ook het nodige aanvullende onderzoek kan worden gedaan. Een neuroloog kan gebruikmaken van MRI-scans, een DAT-SPECT-scan of een F-Dopa PET-scan van de hersenen, transcraniële echografie, neuropsychologisch onderzoek en eventueel genetisch onderzoek.
Behandelmogelijkheden
De ziekte van Parkinson kan niet worden genezen of vertraagd. De behandeling is erop gericht de symptomen te bestrijden. Daarvoor zijn verschillende geneesmiddelen op de markt. Daarnaast zijn er tal van andere behandelmogelijkheden. In dit vierde hoofdstuk worden ze allemaal besproken.
De behandeling van de ziekte van Parkinson wordt primair gedaan door neurologen in samenwerking met parkinsonverpleegkundigen, in goede samenspraak en afstemming met de huisarts. Deze behandelaars vormen met elkaar het kernteam. Vanuit dit kernteam kunnen paramedici en andere specialisten in consult worden gevraagd. De betrokkenheid van andere zorgverleners is afhankelijk van de specifieke problemen die de patiënt ervaart.
Andere zorgverleners kunnen zijn:
- apotheker
- diëtist
- ergotherapeut
- fysiotherapeut
- klinisch geriater
- logopedist
- maatschappelijk werker
- neurochirurg
- opticien en/of oogarts
- psychiater
- psycholoog, neuropsycholoog of gezondheidszorgpsycholoog
- revalidatiearts
- seksuoloog
- medewerkers van de thuiszorg
- uroloog
- specialist ouderengeneeskunde.
Wanneer medicijnen?
De behandeling van de ziekte van Parkinson is erop gericht de patiënt zo lang mogelijk onafhankelijk en met een goede kwaliteit van leven te laten functioneren in het dagelijks leven. Parkinson is een voortschrijdende ziekte. Daarom is het noodzakelijk om de medische en psychosociale aspecten regelmatig te laten controleren.
Het is altijd een lastige beslissing wanneer nu precies gestart moet worden met medicatie. Als vuistregel wordt aangehouden dat gestart moet worden met medicijnen, of dat de al voorgeschreven dosering moet worden verhoogd indien in het dagelijks leven problemen ontstaan op een van de volgende terreinen:
- werk;
- hobby’s;
- zelfverzorging;
- mobiliteit (het veilig kunnen en durven verplaatsen);
- vervelende symptomen waarvoor de patiënt zich bijvoorbeeld schaamt.
Op basis van de klachten, de leeftijd en een aantal specifieke zaken zal de neuroloog een keuze maken voor een bepaald type medicijn.
Tot op heden zijn er geen geneesmiddelen die de ziekte van Parkinson kunnen genezen of het ziekteproces kunnen vertragen. De behandeling is daarmee hoofdzakelijk gericht op het onderdrukken van de symptomen door het dopaminetekort aan te vullen, om daarmee de kwaliteit van leven van de patiënt te verbeteren.
Geneesmiddelen bij motorische klachten
De meest gebruikte medicijnen zijn levodopa en de zogeheten dopamine-agonisten. Deze geneesmiddelen vullen het tekort aan dopamine aan (levodopa) of stimuleren net als dopamine zelf de dopaminereceptoren (dopamine-agonisten). Vrijwel alle patiënten krijgen deze medicijnen vroeg of laat voorgeschreven. Parkinsonmiddelen kunnen uiteraard ook bijwerkingen geven. De arts streeft dan ook naar een evenwicht tussen het gewenste effect en de bijwerkingen van de medicatie. De werking van de geneesmiddelen en de ernst van de bijwerkingen verschillen per persoon.
Levodopa
Levodopa is een natuurlijk voorkomende stof in de hersenen dat de hoeveelheid dopamine in de hersenen verhoogt. Levodopa is het meest effectieve medicijn om de symptomen van de ziekte van Parkinson te onderdrukken. Levodopa is een goede optie om als middel van eerste keuze voor te schrijven bij parkinsonpatiënten in de vroege fase van de ziekte. De dosis levodopa wordt opgebouwd aan de hand van de klachten. Daarbij is het doel een zo laag mogelijke dosering te vinden waarmee een goed effect wordt bereikt. De patiënt is de belangrijkste schakel bij het bepalen van het optimale effect. Die kan immers als enige aangeven of de problemen in het dagelijks leven afgenomen zijn.
Het heeft geen zin om behandeling met medicijnen langer dan noodzakelijk uit te stellen met het idee dat dit het beloop op langere termijn gunstig zou beïnvloeden of wisselingen in het functioneren daardoor zou uitstellen. Hiervoor bestaat geen bewijs. Uitstel van behandeling om deze redenen wordt dan ook niet aangeraden.
De beste kwaliteit van leven, ook op lange termijn, wordt verkregen als er gestart wordt met behandelen als dit klinisch wenselijk lijkt, dat wil zeggen als de patiënt zodanige klachten ervaart dat dit zijn dagelijkse bezigheden beperkt.
Er zijn verschillende levodopa-preparaten verkrijgbaar, die onderling verschillen in de hulpstoffen die aanwezig zijn of in de afgiftesnelheid (snel, normaal en vertraagd). Veelgebruikte middelen zijn: levodopa in combinatie met benserazide (Madopar) en levodopa in combinatie met carbidopa (Sinemet). Qua werkzaamheid zijn deze middelen vergelijkbaar. De begindosering bestaat meestal uit driemaal daags 62,5 mg. Afhankelijk van de klachten en bijwerkingen kan de dosering worden verhoogd, tot regelmatig drie- à viermaal 250 mg per dag of soms nog hoger, tot wel viermaal 500 mg per dag. Alles staat of valt met de individuele reactie op de medicijnen en het persoonlijke bijwerkingenprofiel.
Bijwerkingen die in het begin het meest voorkomen zijn misselijkheid en een licht gevoel in het hoofd bij het opstaan. De misselijkheid is goed te behandelen met domperidon en verdwijnt vaak na een aantal weken. Het langdurig niet goed kunnen verdragen van levodopa in de vroege fase is vrij zeldzaam bij patiënten met de ziekte van Parkinson en zou mogelijk kunnen wijzen op de aanwezigheid van een vorm van atypisch parkinsonisme.
In de eerste jaren na de diagnose ziekte van Parkinson merken de meeste patiënten een stabiele verbetering bij gebruik van bijvoorbeeld driemaal daags levodopa. Vaker doseren is in die fase meestal niet zinvol. Na een aantal jaren kunnen echter zogenoemde responsfluctuaties ontstaan. Dit zijn schommelingen in het functioneren, die in het begin samenhangen met het tijdstip van inname van de medicatie. Op bepaalde momenten van de dag, meestal aan het einde van de werkingsduur van een medicatiegift, ervaart de patiënt dan meer parkinsonverschijnselen, waaronder toegenomen stijfheid en traagheid. Ook kunnen er perioden zijn waarin de patiënt juist overbeweeglijk wordt, omdat de medicatie als het ware zijn doel voorbijschiet. Deze responsfluctuaties kunnen worden verminderd door de dosering aan te passen, door de frequentie van inname te veranderen, door een ander middel te gaan gebruiken of door bijvoorbeeld een dopamine-agonist aan levodopa toe te voegen.
Dopamine-agonisten
Dopamine-agonisten stimuleren, net als het lichaamseigen dopamine, de dopaminereceptoren in de hersenen. De symptomen van de ziekte van Parkinson kunnen goed behandeld worden met dopamine-agonisten. Dopamine-agonisten werken in vergelijking met levodopa minder krachtig, maar ze geven minder responsfluctuaties, vooral bij patiënten bij wie voor hun veertigste jaar de ziekte van Parkinson werd vastgesteld.
In de ongecompliceerde fase kan de behandelend specialist ook als eerste medicament kiezen voor een van de dopamine-agonisten. De voorkeur gaat daarbij uit naar zogeheten non-ergot dopamine-agonisten, zoals pramipexol, ropinirol en rotigotine. Alleen bij wijze van uitzondering, als de patiënt deze middelen niet verdraagt, kan een ergot dopamine-agonist worden voorgeschreven, zoals bromocriptine of pergolide. De reden voor de terughoudendheid met de ergot dopamine-agonisten is het optreden van specifieke bijwerkingen, onder meer bindweefselvorming aan de hartkleppen. Daarom dienen de volgende symptomen bij elk bezoek aan de specialist gecontroleerd te worden als een patiënt pergolide of bromocriptine gebruikt:
- hartruis (souffles);
- tekenen van hartfalen (decompensatio cordis);
- snelle kortademigheid.
Patiënten die ergot dopamine-agonisten gebruiken, moeten jaarlijks worden gecontroleerd door de cardioloog. Die zal een echo laten maken van de hartkleppen.
Het gebruik van dopamine-agonisten moet volgens een vast schema worden opgebouwd. Dit schema staat in de bijsluiter.
Het streven is steeds een goed effect te krijgen met een zo laag mogelijke dosering. Dat beperkt namelijk het risico van bijwerkingen.
Als er bijwerkingen zijn of één bepaalde dopamine-agonist onvoldoende effect heeft, kan de behandelend specialist een andere dopamine-agonist voorschrijven.
Dopamine-agonisten met een vergelijkbare werking zijn: pramipexol (Sifrol), ropinirol (Requip), rotigotine (Neupro), apomorfine (Britaject), bromocriptine (Parlodel) (nauwelijks meer voorgeschreven), pergolide (Permax) (nauwelijks meer voorgeschreven). Rotigotine wordt door middel van een pleister toegediend, apomorfine via een subcutane injectie of via een subcutaan naaldje.
Bijwerkingen die in het begin het meest voorkomen zijn misselijkheid en een licht gevoel in het hoofd bij het opstaan. De misselijkheid is goed te behandelen met domperidon en verdwijnt vaak na een aantal weken.
Levodopa of een dopamine-agonist?
De keuze tussen levodopa of een dopamine-agonist hangt af van individuele factoren. Hierbij spelen de volgende factoren een rol:
- leeftijd;
- medische voorgeschiedenis;
- mogelijke andere ziekten of aandoeningen;
- eerdere ervaringen met bijwerkingen;
- wensen en doelstellingen van de patiënt;
- voorkeuren van de patiënt (en soms ook van de behandelend specialist);
- ernst van de beperkingen.
Bij relatief ernstige functiebeperkingen heeft levodopa de voorkeur. Wanneer dopamine-agonisten niet (meer) voldoende werken, moet niet geaarzeld worden om levodopa voor te schrijven. Veruit de meeste patiënten worden vroeg of laat behandeld met een combinatie van beide.
Overige antiparkinsonmedicijnen
MAO-B-remmers
MAO is de afkorting van mono-amine-oxidase. MAO-B-remmers behoren tot een groep medicijnen die het enzym mono-amine-oxidase-B remmen. Dit enzym bevordert normaal de afbraak van dopamine. Het remmen van het enzym door een MAO-B-remmer leidt dan ook tot een verhoogde beschikbaarheid van dopamine.
Als er sprake is van lichte functiebeperkingen die nog geen wezenlijke beperking geven van het functioneren in het dagelijks leven, kan een van de zogenoemde MAO-B-remmers voorgeschreven worden. Uit deze categorie zijn in Nederland twee middelen beschikbaar: selegiline en rasagiline. Beide geneesmiddelen kunnen een verbetering geven van de parkinsonverschijnselen. Selegiline heeft als specifieke bijkomstigheid dat het kan helpen tegen slaperigheid overdag. Als het echter te laat op de dag wordt ingenomen kan het ’s nachts juist slapeloosheid veroorzaken. Rasagiline heeft als specifiek voordeel dat het slechts eenmaal per dag gedoseerd hoeft te worden. In het algemeen geldt dat het gebruik van MAO-B-remmers wordt afgeraden wanneer de patiënt last heeft van hallucinaties, al of niet in combinatie met cognitieve stoornissen.
Amantadine
Patiënten met lichte functiebeperkingen kunnen amantadine voorgeschreven krijgen. De dosering is tweemaal daags 100 mg. Amantadine moet niet worden voorgeschreven aan oudere patiënten of aan patiënten met cognitieve stoornissen, want dit medicijn geeft in die groepen een verhoogd risico op visuele hallucinaties.
Anticholinergica
Bij ernstige tremoren kunnen anticholinergica worden voorgeschreven. Dit medicijn is alleen geschikt voor relatief jonge parkinsonpatiënten, die vooral functiebeperkingen hebben als gevolg van het trillen (dus weinig last hebben van de andere parkinsonsymptomen) en die geen cognitieve klachten of symptomen hebben. Anticholinergica geven geen verbetering van de andere parkinsonsymptomen. Vanwege de vrij grote kans op bijwerkingen – onder meer slaperigheid, droge mond en verminderd reactievermogen – is dit medicijn echter niet de eerste keuze.
Wisselende motorische symptomen
Ergens in het beloop van de ziekte van Parkinson maakt de stabiele reactie op medicijnen plaats voor een minder stabiele fase, waarin merkbaar wordt dat medicijnen aanslaan en weer uitgewerkt raken.
Dan wordt het belangrijk te achterhalen wat de effecten zijn van een enkele gift medicijnen. Als dat bekend is kan gerichte aanpassing plaatsvinden.
Er zijn dan grofweg twee subtypes te onderscheiden. Bij patiënten met onvoorspelbare wisselingen heeft het zin om het medicatieschema aan te passen op basis van de waargenomen wisselingen. Hierbij kunnen medicijnen zoals COMT-remmers worden ingezet. Daarnaast zijn er patiënten met onvoorspelbare wisselingen die geen enkel verband meer zien tussen hun functioneren en de inname van medicijnen. In dat geval is het erg moeilijk, zo niet onmogelijk, om een rationele aanpassing van hun medicatieschema te maken. Gelukkig zijn er dan nog wel medicamenteuze opties over om het functioneren te verbeteren, namelijk continue subcutane infusie met apomorfine (ApoGo) of continue intestinale infusie met levodopa/carbidopagel (Duodopa). Daarnaast bestaat de mogelijkheid van stimulatie van een van de basale kernen, onder andere de nucleus subthalamicus (STN), die verderop nog wordt besproken.
COMT-remmers
COMT is de afkorting van catechol-O-methyltransferase. Dit is een groep medicijnen die het enzym catechol-O-methyltransferase remt en daarmee de afbraak van levodopa, zodat er meer levodopa in de hersenen beschikbaar komt.
Parkinsonpatiënten die voorspelbare responsfluctuaties (schommelingen) hebben ontwikkeld bij het gebruik van levodopa, kunnen worden behandeld door het toevoegen van een van de zogeheten COMT-remmers. De twee in Nederland beschikbare medicijnen zijn entacapon en tolcapon. Het middel entacapon heeft de voorkeur vanwege het gunstiger bijwerkingenprofiel. Entacapon moet gelijktijdig met levodopa worden ingenomen. Entacapon dient vooral geprobeerd te worden wanneer er sprake is van een te kort durend effect, met steeds een ‘off’-periode tussen de diverse medicatiegiften in. Wanneer entacapon geen of onvoldoende effect geeft of wanneer de patiënt te veel bijwerkingen ervaart, kan tolcapon een alternatief zijn. Dit middel heeft echter het risico van leverfunctiestoornissen. Daarom moeten bij aanvang van gebruik en elke twee weken gedurende het eerste jaar de leverfuncties bepaald worden. Deze controle kan op verzoek door de huisarts gedaan worden.
Apomorfine
De toediening van apomorfine met een pompje is geschikt voor patiënten in de gecompliceerde fase met onvoorspelbare off-perioden die met medicatie in tabletvorm niet meer goed behandeld kunnen worden. Apomorfine kan onderhuids (subcutaan) via een naaldje worden toegediend. Als de ‘off’-perioden weinig frequent voorkomen, is het voldoende om af en toe een injectie te gebruiken. Als de ‘off’-perioden echter vaker voorkomen – meer dan vijf keer per dag – kan apomorfine via een pompje constant worden toegediend (zie figuur 11). Het naaldje dat onderhuids wordt geprikt, moet dagelijks vervangen worden om lokale stapeling van de afbraakproducten van apomorfine te voorkomen, omdat dit een lokale prikkelingsreactie kan geven van de huid.
Om misselijkheid en braken te voorkomen wordt samen met apomorfine domperidon voorgeschreven. De patiënt moet ten minste een dag voor aanvang van de behandeling met het gebruik van domperidon beginnen. De standaarddosis van de domperidon is driemaal daags 20 mg. Na enkele weken gebruik kan geprobeerd worden de domperidon weer af te bouwen. De meeste patiënten zijn dan minder gevoelig geworden voor de bijwerkingen van de apomorfine. Omdat domperidon hartritmestoornissen kan geven, moet voor het starten van domperidon bij iedere patiënt aanvullend laboratoriumonderzoek plaatsvinden (o.a. op kalium en natrium) met een ECG om vast te stellen of de uitkomsten daarvan goed zijn.

Figuur 11: Apomorfinepomp.
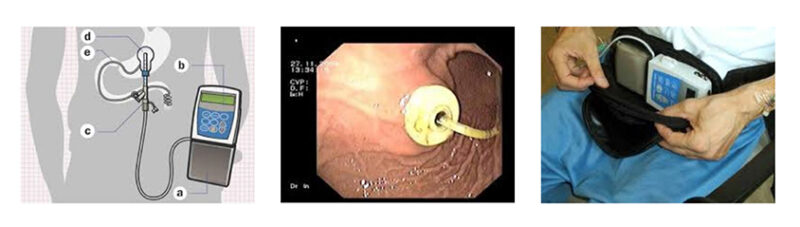
Figuur 12: PEG-sonde met ankerplaatje vanuit de binnenkant van de maag bezien.
Levodopa/carbidopa intestinale gel (via de dunne darm)
Het toedienen van levodopa/carbidopa-gel via de twaalfvingerige darm (duodenum) kan geschikt zijn voor een bepaalde groep patiënten, in een gevorderd stadium van de ziekte. Het gaat om patiënten die, ondanks een optimale instelling op antiparkinsonmiddelen, last blijven houden van onvoorspelbare responsfluctuaties. Voor die patiënten is naast apomorfine ook deze behandeling beschikbaar. De gel wordt via een zogeheten PEG-sonde middels een opening in de buikwand naar de twaalfvingerige darm getransporteerd (zie figuur 12).
BBehandeling van niet-motorische symptomen
De in hoofdstuk 1 behandelde niet-motorische symptomen kennen diverse behandelmogelijkheden die hieronder schematisch worden benoemd. Deze behandelopties kunnen dan met de behandelend specialist worden besproken.
Slaapstoornissen
- Inslaapproblemen: atypische slaapmedicatie (Zolpidem en Zopiclon).
- Doorslaapproblemen indien veroorzaakt door stijfheid: Madopar Dispers,
- rotigotine, continue apomorfine infusie.
- Rusteloze benen/PLMS: langwerkende dopamine-agonisten voor de nacht.
- Droomslaap met onrust: clonazepam.
- Depressie: antidepressiva (nortryptiline, citalopram, sertraline).
Gewichtsverlies
- Analyse andere oorzaken voor het gewichtsverlies, zoals een kwaadaardige ziekte of een schildklierprobleem.
- Als sprake is van regelmatig optredende overtollige bewegingen, moet de dosering worden verlaagd.
Voedingssupplementen.
- Verwijzing naar een diëtist.
Slikstoornissen
- Verwijzing naar een logopedist.
- Bij het vermoeden van een vernauwing in de slokdarm doorverwijzing naar KNO-arts.
- Voor de korte termijn kan drinkvoeding worden voorgeschreven.
- Voor de lange termijn kan sondevoeding een oplossing zijn.
- Wat de medicatie betreft kan toedienen door middel van een pleister (rotigotine) een voordeel zijn. In latere fasen kan een subcutane apomorfinepomp of levodopa via een duodenumsonde worden toegepast.
Voor meer informatie over slikproblemen kan men de richtlijn ‘Logopedie bij de ziekte van Parkinson’ bekijken. Deze is gemaakt door de Nederlandse Vereniging voor Logopedie en Foniatrie (NVLF), zie www.nvlf.nl.
Obstipatie
- Verwijzing naar een diëtist voor een grotere inname van voedingsvezels en vocht (minimaal twaalf tot vijftien glazen water per dag).
- Meer en dagelijks bewegen.
- Vezelsupplementen, zoals psyllium en methylcellulose.
- Laxeermiddelen, in het bijzonder osmotisch werkende middelen (bijvoorbeeld movicolon).
- Zo nodig een klysma.
- Domperidon, om de maag-darmbeweeglijkheid te verbeteren.
Bloeddrukdaling bij staan
- Het bed schuin zetten, met het hoofdeinde iets omhoog (ca. 15 cm).
- Langzaam opstaan.
- Veel zout en vocht innemen (11/2-2 liter vocht per dag en 6-12 gram zout).
- Steunkousen (zeker bij opgezette voeten).
- Stoppen of verlagen van dosering van medicijnen tegen hoge bloeddruk (hypertensie).
- Dosering dopamine-agonisten verlagen/stoppen en kiezen voor middelen met minder risico op lage bloeddruk, zoals levodopa.
- Domperidon (30-60 mg/dag).
- Fludrocortison (100-200 ug/dag).
- Midodrine (10-30 mg/dag).
- Pyridostigmine (40-240 mg/dag).
Blaasproblemen
- Bij vaak plassen ’s nachts:
- ’s avonds minder drinken
- anticholinergica (remmen blaascontracties)
- dermopressie voor de nacht (stopt urineproductie
- ’s nachts)
- condoomcatheter.
- Bij onvoldoende uitplassen: consult uroloog.
Overmatig transpireren
- Medische oorzaken, zoals een chronische infectie of een te snel werkende schildklier uitsluiten.
- Bij off-gerelateerd transpireren medicatie aanpassen.
- Anticholinergica of bètablokkers.
- Overmatige speekselvloed
- 1 procent atropinedruppels tweemaal daags onder de tong.
- Botuline-toxine-injecties in de speekselklieren.
- Bestraling van de speekselklieren. Dit gebeurt tijdens twee kortdurende behandelingen, waarbij met een heel lage dosis straling een deel van de functie van de speekselklieren wordt stilgelegd. De behandeling is eenvoudig en effectief, maar is niet overal beschikbaar.
- Glycopyrriumbromide (driemaal daags 1 mg, drankje).
Pijn
- Bij stijfheid proberen de dopaminerge medicatie te verhogen.
- Zenuwpijn kan bestreden worden met onder meer amitriptyline en anti-epileptica, zoals pregabaline en gabapentine.
- Pijnstillers of fysiotherapie.
Psychose
- Onderzoek van cognitieve functies en deze bij gevonden afwijkingen behandelen.
- Uitsluiten van een delier. Een delier is een plotselinge ernstige verwardheid. Deze wordt bij oudere patiënten meestal veroorzaakt door medicijnen, plasproblemen, een urineweginfectie of koorts door een infectie elders.
- Start clozapine.
- Probeer dopamine-agonisten, amantadine en selegiline, af te bouwen indien mogelijk.
- Indien clozapine niet wordt verdragen: probeer quetiapine.
Parkinsondementie
- Als de diagnose PDD gesteld is, kan gestart worden met rivastigmine (dosering 4,6-9,5 mg /dag als pleister of 3-12 mg in capsules).
- Alleen als de kwaliteit van leven van de patiënt zo slecht is dat behandeling met rivastigmine niet meer zinvol lijkt, is stoppen met dit middel raadzaam. Als de cognitieve functies na het staken van de behandeling weer verslechteren, dan moet de patiënt opnieuw met rivastigmine beginnen.
- Innemen van medicijnen en therapietrouw
Het innemen van medicijnen is in het algemeen iets waar de meeste patiënten moeite mee hebben. In de eerste plaats omdat ze het idee hebben dat er lichaamsvreemde stoffen worden toegediend, met eigen effecten en bijwerkingen. Nu is de situatie bij de ziekte van Parkinson in sommige gevallen wel speciaal, omdat bijvoorbeeld het middel levodopa een volledig lichaamseigen stof is, een omzetting van het aminozuur tyrosine, dat als aanvulling wordt gegeven op de achterblijvende productie van levodopa door het lichaam zelf. Dat betekent dat levodopa meestal ook goed wordt verdragen. Wel is het zo dat levodopa altijd in combinatie wordt gegeven met een stof die de omzetting van levodopa naar dopamine in de bloedbaan of lever voorkomt, omdat dopamine niet door de bloedhersenbarrière (de vaatwand) komt en daardoor niet kan worden opgenomen in het hersenweefsel. Dat is wel het geval met levodopa. De overige antiparkinsonmiddelen komen niet in natuurlijke vorm in de hersenen voor.
Trage maag-darmbewegingen
Parkinsonpatiënten zijn niet alleen traag in het bewegen, maar hebben ook een vertraagde maag-darmmotoriek. Dat betekent dat er een vertraagde maaglediging is, die ook de effectiviteit van medicijnen beïnvloedt. Medicijnen worden namelijk opgenomen in de twaalfvingerige darm (het duodenum) en moeten, om daar te komen, uit de maag worden getransporteerd. Als de maaglediging traag verloopt heeft dat dus een direct gevolg voor de opname en het effect van alle antiparkinsonmedicijnen. Om dat te verbeteren kan bijvoorbeeld domperidon worden gegeven. Toediening via een route die de opname via maag en darmen omzeilt, zoals een pleister, kan dit probleem ook ondervangen.
Een andere klacht ten gevolge van de vertraagde maag-darmlediging is obstipatie. Middelen die de obstipatie kunnen verbeteren, kunnen daardoor bijdragen aan een beter effect van medicijnen, omdat daardoor de doorstroming van maag en darmen verbetert, en daardoor ook de opname van medicijnen.
Wanneer moeten medicijnen worden ingenomen?
Het is belangrijk dat levodopa zoveel mogelijk buiten de maaltijden om wordt ingenomen, omdat eiwitten uit de voeding de opname van levodopa nadelig kunnen beïnvloeden. Het advies is dan ook om levodopa ten minste een halfuur tot een uur voor of na de maaltijd in te nemen, om deze invloed zoveel mogelijk te vermijden. Dit advies geldt niet voor de overige antiparkinsonmedicatie. Daarnaast is het belangrijk dat alle medicijnen worden ingenomen met water, al of niet koolzuurhoudend, en/of met zure drankjes zoals sinaasappelsap. Dit is nodig, omdat een lage zuurgraad (door een hoge concentratie van een zuur sap) de opname van medicijnen verbetert, waardoor een beter effect kan ontstaan. Vooral melk moet gemeden worden om medicijnen mee in te nemen. Dit doet namelijk het tegenovergestelde: het verhogen van de zuurgraad (maaginhoud wordt minder zuur), waardoor de opname van antiparkinsonmiddelen afneemt.
Wat te doen bij responsfluctuaties?
Het is van belang om te kijken of er een stabiel effect is van de medicijnen gedurende de dag. Zolang dat het geval is, is er sprake van een goede en gewenste effectiviteit van de medicijnen.
Helaas krijgen de meeste patiënten na een paar jaar last van zogeheten responsfluctuaties, waarbij men gaat merken dat medicijnen gaan werken en weer uitgewerkt raken. Zolang dat op voorspelbare momenten gebeurt, kan de medicatie hierop aangepast worden. Daarom moet de patiënt opletten hoelang het duurt voordat een bepaald middel gaat werken en hoelang dat effect aanhoudt. Met die gegevens kan een goed innameschema worden gemaakt. Zo’n schema is altijd beter dan wachten met het innemen van nieuwe medicijnen op het moment dat het fout gaat en iemand ‘off’ wordt. Dan is men namelijk altijd te laat, omdat het gemiddeld ongeveer een halfuur duurt, in het gunstigste geval, voordat nieuwe medicijnen weer effect hebben. Dus inname op gevoel, hetgeen veel patiënten toch doen, geeft onnodig veel ‘off’-momenten, die met een goed schema voorkomen kunnen worden. In een dergelijk schema kan men anticiperen op de momenten van verslechtering.
Invloed van onnauwkeurige medicijninname
Het niet precies innemen van medicijnen, ook voor de ziekte van Parkinson, komt veel voor en heeft grote consequenties voor de patiënten zelf en voor de kosten van de gezondheidszorg. Niet zelden worden patiënten door onnauwkeurige medicijninname onnodig ‘off’, waardoor ze bijvoorbeeld vallen en een heup of schouder breken, met alle consequenties van dien.
De onderzoeken bij patiënten met de ziekte van Parkinson laten zien dat meer dan 50 procent van alle voorgeschreven medicatie niet juist wordt ingenomen. Dit betreft dan zowel een onjuiste dosering als inname op andere tijdstippen dan voorgeschreven of in het geheel geen inname van de voorgeschreven medicijnen. Dit probleem heeft alles te maken met de vaak complexe medicijnschema’s met zeer frequente tijdstippen van inname overdag, en soms zelfs ’s nachts. Dit gecombineerd met de vaak aanwezige, al of niet milde, cognitieve stoornissen maakt wel begrijpelijk waarom het zo vaak fout gaat met de medicijnen bij parkinsonpatiënten.
Deze therapieontrouw beïnvloedt de kwaliteit van leven echter aantoonbaar in negatieve zin.
Ook de medische kosten zijn duidelijk hoger bij patiënten die hun medicijnen niet precies innemen: 3000 dollar per jaar per patiënt (Amerikaans onderzoek). In Nederland is ook gekeken naar het effect van het niet trouw zijn aan de therapie. Het blijkt dat hierdoor per jaar 19.000 ziekenhuisopnames extra nodig zijn, voor alle ziektecategorieën, inclusief de ziekte van Parkinson. Bij patiënten ouder dan 65 jaar is de therapietrouw twee keer zo slecht in vergelijking met jongere patiënten. Bij oudere patiënten spelen mogelijk ook geheugen- en aandachtsproblemen een rol. Al met al zijn deze cijfers dermate ernstig dat het probleem van therapietrouw veel meer aandacht verdient, van zowel behandelaars als van patiënten.
Maatregelen ter verbetering van de therapietrouw
Er zijn diverse mogelijkheden om de therapietrouw te verbeteren.
- Het gebruik van voorverpakte medicijnen met een juiste dosis (Baxtersysteem).
- Goede uitleg op schrift met de bijbehorende medicijnschema’s door de behandelaars.
- Gebruik van een medicatiealarm. Dit kan via de smartphone, sms-services of via een eenvoudig alarm op het horloge.
- Gebruik van speciale medicijndozen, waarin zelfs voorgevulde cassettes kunnen worden gebruikt, zodat de juiste medicatie wordt gekoppeld aan het juiste tijdstip (zie onder andere de website van de Belgische parkinsonvereniging: www.parkinsonliga.be).
- Een ‘review’ van alle medicatie door een gespecialiseerde apotheker, met kennis van de behandeling van parkinson, die alle gebruikte medicijnen tegen het licht houdt, om zodoende ongewenste bijwerkingen en interacties van bestaande medicijnen snel op het spoor te komen en waar nodig aan te passen. Dit voorkomt onnodige bijwerkingen, hetgeen hopelijk een gunstig effect heeft op de juiste inname van de medicijnen.
- Hulp van partner, mantelzorger of thuiszorg.
- Behandelingen, anders dan met medicijnen
- Diepe hersenstimulatie
Wanneer er klachten zijn van onvoorspelbare responsfluctuaties, dat wil zeggen dat er geen relatie meer is tussen het functioneren en de ingenomen medicijnen, dan komt een patiënt in aanmerking voor meer continue behandeling, zoals infusie met apomorfine of duodopa, dan wel een hersenoperatie.
De belangrijkste technieken bij hersenoperaties zijn:
- het aanbrengen van een letsel;
- het inbrengen van een elektrode die bepaalde structuren in de hersenen elektrisch stimuleert.
Niet alle patiënten komen in aanmerking voor een hersenoperatie. De neuroloog maakt een nauwkeurige inschatting van het risico en de kans op succes. Deze operaties worden maar in zes centra in Nederland verricht. Iedere patiënt die mogelijk in aanmerking komt voor een dergelijke operatie, zal hiernaar verwezen worden voor advies. Bij goed geselecteerde patiënten wordt het functioneren over de dag stabieler door een hersenoperatie. De ziekte van Parkinson wordt door een operatie echter niet genezen of tot staan gebracht.
STN-stimulatie
Een in Nederland veel toegepaste hersenoperatie is de stimulatie van de subthalamische kern, afgekort als de STN. De subthalamische kern is onderdeel van de basale kernen. Deze hersenkern staat in contact met de zwarte kern, de substantia nigra, en de hersenschors en is een van de belangrijkste schakelcentra van de basale kernen.
Een belangrijk Nederlands langetermijnonderzoek heeft aangetoond dat de STN de voorkeurskern is voor behandeling van een wisselend motorisch functioneren bij de ziekte van Parkinson.
Niet iedere patiënt met de ziekte van Parkinson komt voor STN-stimulatie in aanmerking. Als er sprake is van een situatie zoals hierna genoemd kan STN-stimulatie niet plaatsvinden:
- dementie;
- ernstige depressie of psychose voorafgaand aan de ingreep;
- ernstige, niet door levodopa veroorzaakte psychose of (hypo)manie in de voorgeschiedenis;
- balans- en/of spraakproblemen als het meest ernstige symptoom;
- een slechte algemene gezondheidstoestand, die een groot risico heeft bij chirurgie;
- patiënten die in de beste on-fase nog afhankelijk zijn van anderen voor hun algemene dagelijkse levensverrichtingen;
ernstige schrompeling van de hersenen (atrofie) of uitgebreide doorbloedingsstoornissen op CT- of MRI-scan van de hersenen.
Na een STM-ingreep hebben vrijwel alle patiënten antiparkinsonmedicatie nodig, maar in veel lagere doses.
Bewegen
Het is belangrijk bij de ziekte van Parkinson om in beweging te blijven. Het zorgen voor een goede basisconditie is belangrijk. Een paar keer per dag een rondje wandelen of fietsen is voldoende om een goede conditie te houden. Ook de dagelijkse activiteiten dragen bij aan de nodige beweging en training. Gericht bewegen is nodig als er klachten ontstaan die een belemmering vormen voor de dagelijkse activiteiten.
Tweemaal per dag een halfuur bewegen als aanvulling op de dagelijkse activiteiten is voldoende.
Nordic walking
Veel mensen met de ziekte van Parkinson vinden Nordic walking een prettige manier van bewegen. Het lopen gaat met behulp van stokken gemakkelijker. De armen worden automatisch meegenomen, de paslengte is beter, en de houding is vaak meer rechtop.
Alternatieve behandelingen, waarvan het effect niet is bewezen
Yoga
Yoga (hatha yoga) is gericht op het verminderen van stress. Door gerichte oefeningen wordt ontspanning bevorderd. Geheugen en concentratie kunnen hierdoor verbeteren.
Tai chi
Tai chi komt uit China en is een soepele en harmonieuze manier van bewegen op de in- en uitademing. Naast het oefenen op souplesse richt het zich ook op een diepere ontspanning die als zeer prettig ervaren kan worden.
Paramedische behandelingen
Fysiotherapie
Gericht oefenen bij de ziekte van Parkinson werd lang niet als zinvol gezien. Toch heeft wetenschappelijk onderzoek laten zien dat gerichte training zinvol is. Trainen met aandacht voor balans, conditie, verplaatsingen en lichaamshouding kan de kans op vallen verkleinen. Dat maakt ook de kans op fracturen kleiner. Vroegtijdig signaleren en verwijzen naar de fysiotherapeut is dus belangrijk.
Fysiotherapie bij de ziekte van Parkinson is specifiek gericht op de volgende onderwerpen:
- beperkingen in het lopen (freezing);
- oefenen van het in en uit bed komen;
- opstaan uit een stoel;
- lopen en zich omdraaien;
- balanstraining;
- valpreventie en valtechniek;
- lichaamshouding en looppatroon;
- in stand houden van conditie en functies.
Fysiotherapie via ParkinsonNet
Sinds enkele jaren zijn er in Nederland diverse parkinsongeschoolde fysiotherapeuten werkzaam. Zij zijn te vinden via de zorgzoeker van het ParkinsonNet (zie ook hoofdstuk 8).
Revalidatiecentrum in de tweede lijn
In een aantal revalidatiecentra in het land worden speciale programma’s aangeboden voor mensen met de ziekte van Parkinson. Het gaat om programma’s die in dagdelen per week of gedurende een opname gevolgd kunnen worden. Het aanbod is specifiek gericht op de problemen die voortvloeien uit de ziekte van Parkinson en worden zowel individueel als in groepsverband gegeven. In een revalidatiecentrum zijn verschillende disciplines werkzaam die in teamverband samenwerken onder leiding van een revalidatiearts, zoals fysiotherapie, ergotherapie, logopedie, maatschappelijk werk, psycholoog en arbeidsdeskundige.
Logopedie
Bij de ziekte van Parkinson kunnen er problemen met het spreken ontstaan. Hiervoor kan een logopediste geconsulteerd worden. De klacht die het meest voorkomt, is een zachte stem en een monotone, onduidelijke spraak. De stem kan soms wegvallen en de articulatie neemt af. Het tempo van het spreken kan te hoog of te laag liggen. Ook stotteren en woordvindingsproblemen komen voor.
Een behandeling door de logopedist is erop gericht duidelijker en bewuster en vooral luider te spreken. De Lee Silverman Voice Treatment en Pitch Limiting Voice treatment zijn erop gericht langzamer en luider te spreken. Spraakhulpmiddelen als een spraakversterker of communicatiebord kunnen de spraak ondersteunen.
Ergotherapie
Het aanvragen van hulpmiddelen en aanpassingen is het werkterrein van de ergotherapeut. Een ergotherapeut richt zich op activiteiten als zelfverzorging, vervoer binnens- en buitenshuis, werken, wonen, dagbesteding, hobby’s, communicatie en huishouding. De ergotherapeut bespreekt de problemen die de patiënt bij de ADL-activiteiten tegenkomt en probeert hiervoor een oplossing te vinden. De oplossingen zijn individueel gericht.
Communicatie
De logopedist en de ergotherapeut kunnen samenwerken om op zoek te gaan naar hulpmiddelen om de communicatie te verbeteren, bijvoorbeeld op het terrein van spreken, schrijven, telefoneren en computergebruik.
Woningaanpassing
De ergotherapeut kijkt onder andere naar woningaanpassingen en geeft inrichtingsadviezen gericht op het wegnemen van obstakels en het voorkomen van vallen, draaien in bed, opstaan vanuit de stoel en neer, vervoer binnens- en buitenshuis (elektrische fiets, scootmobiel en aangepaste auto).
Zelfverzorging
Ook richt de ergotherapeut zich op alles wat te maken heeft met eten, drinken, wassen, kleden, persoonlijke verzorging en toiletgang. Van aangepast bestek tot handige hulpmiddelen als elastische veters, toiletbril en kleding met klittenband.
Huishoudelijke aanpassingen
Richt de keuken zo in dat de vaak gebruikte spullen op normale stahoogte zijn opgeborgen, zodat er niet elke keer gebukt hoeft te worden. Maak gebruik van een verrijdbare kruk zodat lang staan vermeden kan worden.
Werk
Hierbij is aandacht voor re-integratie en aanpassingen op de werkplek zoals aanpassingen aan de computer. Zo is het mogelijk een groter toetsenbord te gebruiken of een aangepaste stoel.
Vrije tijd en hobby’s
Hulp bij het vinden van aanpassingen in bestaande hobby’s en het vinden van nieuwe hobby’s.
Samenvatting
De ziekte van Parkinson kan niet worden genezen of vertraagd. De symptomen kunnen worden bestreden met de verschillende geneesmiddelen die er op de markt zijn. Het is lastig te bepalen wanneer met medicatie moet worden gestart. Als vuistregel geldt dat moet worden begonnen als problemen ontstaan op het gebied van werk, hobby’s, zelfverzorging en mobiliteit. De meest gebruikte geneesmiddelen bij motorische klachten zijn levodopa en dopamine-agonisten. Vrijwel alle patiënten krijgen deze medicijnen vroeg of laat voorgeschreven. De keuze tussen beide hangt af van individuele factoren. Daarnaast zijn ook mogelijk: MAO-B-remmers, amantadine en anticholinergica. In de loop van de ziekte maakt de stabiele reactie op medicatie plaats voor een minder stabiele. Ook voor de niet-motorische symptomen bestaan er tal van behandelmogelijkheden. Belangrijk is dat de patiënt zijn parkinsonmedicijnen trouw inneemt, dat buiten de maaltijden om doet en alert is op responsfluctuaties. Ten slotte is er aandacht voor niet-medicamenteuze behandeling, zoals diepe hersenstimulatie, bewegen, fysiotherapie, logopedie en ergotherapie.
De rol van voeding
Gezonde en gevarieerde voeding is voor iedereen van belang, net als bewegen. Meestal zijn voedingssupplementen dan niet nodig. Voor parkinsonpatiënten die problemen hebben met de opname van voeding of aandoeningen hebben aan het maag-darmstelsel kunnen daar wel behoefte aan hebben.
Vitamines en antioxidanten
Regelmatig hebben patiënten vragen over de mogelijke positieve effecten van vitamines, antioxidanten en co-enzym Q10.
Q10
Q10 is een antioxidant dat bij patiënten met de ziekte van Parkinson verlaagd is in de zogeheten mitochondria, onderdelen van de cellen die zorgen voor de energieproductie. Samenvattend is er geen bewijs dat Q10 effect heeft op het functioneren van patiënten met de ziekte van Parkinson, of op de voortgang van de ziekte. Q10 wordt dan ook niet regulier voorgeschreven.
Vitamine B6
Vitamine B6 heeft verschillende functies. Het is een antioxidant, maar het is ook betrokken bij de productie van diverse neurotransmitters, waaronder dopamine. Daarnaast speelt het een rol bij de opbouw van rode bloedcellen en bij de afbraak van methionine, een belangrijk aminozuur in de stofwisseling. Hierdoor kan er bij een vitamine B6-tekort een stijging optreden van homocysteïne, een stof die is geassocieerd met het verlies van zenuwcellen (neurodegeneratie). Onderzoek in een groep Rotterdammers toonde aan dat er een verlaagd risico was op het krijgen van de ziekte van Parkinson bij proefpersonen met een verhoogde inname van vitamine B6. Bij verlaagde concentraties, vaak door incomplete voeding, kunnen onder andere vermoeidheid en toename van parkinsonklachten ontstaan. Er is echter geen bewijs dat extra inname van vitamine B6 op voorhand effectief is bij patiënten met een reeds vastgestelde diagnose ziekte van Parkinson. Inname van hogere doseringen kan zelfs de zenuwen in armen en benen aantasten (neuropathie).
Vitamine B12
Een tekort aan vitamine B12 kan ontstaan door langer gebruik van hoge doseringen levodopa. Een tekort aan vitamine B12 kan onder andere een neuropathie (aantasting van de zenuwen in armen en benen) veroorzaken, waardoor het lopen kan verslechteren door een verminderde balans. Een tekort aan vitamine B12 kan ook leiden tot vermoeidheid op basis van bloedarmoede.
Daarom is bij patiënten die meer dan 1000 mg levodopa gebruiken controle op hun vitamine B-status aan te bevelen, vooral als er klachten zijn over vermoeidheid, een veranderd gevoel in armen en benen en/of een verminderde balans.
Vitamine C en E
Vitamine C en E zijn eveneens antioxidanten. Tot op heden is er echter geen aanleiding om deze voor te schrijven bij patiënten met de ziekte van Parkinson. Onderzoek heeft geen beschermend effect aangetoond van met name vitamine E. Hogere doseringen vitamine E zouden zelfs schadelijk kunnen zijn. Het is dus niet zo dat het principe ‘baat het niet, dan schaadt het niet’ geldt voor het gebruik van vitamines in het algemeen.
Vitamine D
Diverse onderzoeken hebben laten zien dat er een verhoogde kans op een verlaagd vitamine D is bij patiënten met parkinson. Dit geldt overigens ook voor patiënten met alzheimer. De vraag is of dit iets met de ziekte zelf van doen heeft, dan wel met het verminderd buiten komen, omdat vitamine D onder invloed van zonlicht wordt aangemaakt. Bij patiënten die weinig buiten komen, bestaat er een grote kans op een gebrek aan vitamine D. Een tekort verhoogt het risico op osteoporose (botontkalking), dat op zijn beurt het risico op fracturen weer verhoogt. Volgens de richtlijn ‘Polifarmacie bij ouderen 2012’ wordt daarom vitamine D3 aanbevolen bij ouderen die in instellingen verblijven en weinig buiten komen.
Vitamine K2
Vitamine K2 speelt een rol bij de energiehuishouding van cellen, in de zogeheten mitochondria, de energiefabriekjes van de cel. Om die reden is vitamine K2 onderzocht in fruitvliegjes met erfelijke defecten, zoals die ook voorkomen bij een kleine subgroep van patiënten met de ziekte van Parkinson.
Bij deze fruitvliegjes gaf toevoeging van vitamine K2 een herstel van de energiebalans en konden deze vliegjes weer vliegen, iets wat voordien niet mogelijk was. Daarom zou vitamine K2 een rol kunnen spelen bij patiënten met de ziekte van Parkinson. Op dit moment is daar echter geen enkel bewijs voor.
De invloed van eiwitrijke voeding op het effect van levodopa
Eiwitrijke voeding kan de opname van levodopa vanuit de darmen naar de bloedbaan vertragen. Veel patiënten hebben de ervaring dat het langer duurt voordat levodopa werkt of dat het middel minder goed werkt als het tijdens de maaltijd wordt ingenomen.
Naarmate de maaltijd meer eiwitten bevat, kan deze invloed op de opname van levodopa groter worden. Eiwitten in de voeding bevatten grote aminozuren, die een competitie aangaan met de levodopa (eveneens een aminozuur) waardoor de levodopa minder kan worden opgenomen. Dit kan gevolgen hebben voor die patiënten die last hebben van schommelingen in het functioneren, ondanks stipte medicatie-inname. Het is daarom beter om levodopa een halfuur voor of een uur na de maaltijd in te nemen. Eiwitarme voeding is niet aan te raden. Eiwitten zijn namelijk belangrijke bouwstenen voor onder andere de opbouw en handhaving van spiermassa.
Bijwerkingen van medicijnen
De bijwerkingen van de medicijnen kunnen ervoor zorgen dat er problemen ontstaan ten aanzien van de inname en verbruik van voeding.
Smaak- en hongerverlies komen regelmatig voor en kunnen in relatie staan met reukverlies. Hierdoor worden soms maaltijden overgeslagen. De kans hierop wordt groter als patiënten daarnaast cognitieve stoornissen krijgen. Overbeweeglijkheid als bijwerking van de medicijnen kan zorgen voor gewichtsverlies. Het is mogelijk veel af te vallen in korte tijd door deze bijwerking, soms wel tot 10 kilo binnen een jaar. In dat geval moeten er extra calorieën worden ingenomen om ondergewicht te voorkomen. Geconcentreerde calorie-inname met bijvoorbeeld Nutridrink is dan een mogelijkheid.
Te veel eten en overgewicht komen ook voor. Bij patiënten die slecht slapen komt het nogal eens voor dat de neiging ontstaat om ’s nachts te gaan eten.
Ook veel snoepen komt voor bij patiënten die bepaalde medicijnen gebruiken, zoals pramipexol, clozapine of antidepressiva.
Zeer zelden geeft levodopa een bittere of metaalachtige smaak na inname, hetgeen kan leiden tot vermindering van de eetlust.
Gewichtsverlies bij de ziekte van Parkinson
Bij ongeveer de helft van de parkinsonpatiënten komt gewichtsverlies voor ondanks voldoende inname van voedsel. Gewichtsverlies komt vaker bij vrouwen voor dan bij mannen. Het gewichtsverlies kan soms oplopen tot meer dan 10 kilo per jaar. De precieze oorzaak is nog onduidelijk. Het ontstaan van overbewegingen (hyperkinesieën) door het gebruik van medicijnen om de parkinsonklachten te bestrijden, kunnen een rol spelen bij gewichtsverlies. Daarnaast spelen klachten als moeilijk kauwen en slikken een rol bij de inname van voedsel. Daardoor kan er onvoldoende worden ingenomen. Ook veranderingen in het gedrag en de stemming kunnen bijdragen aan onvoldoende inname, evenals smaak- en reukstoornissen die de eetlust verminderen.
Ondervoeding kan ontstaan als er onvoldoende inname is van calorieën en voedingsstoffen of als er bij normale inname een zeer hoog verbruik is. Neem verschillende kleine maaltijden tussendoor en gebruik volle producten zoals volle melk en roomboter.
Behandeling
Verwijzing naar een diëtiste om het eetpatroon te evalueren en eventueel aanvullende voeding (Nutridrink) voor te schrijven.
Aanpassing van de medicijnen tegen de parkinsonklachten; het verminderen van de dosering kan helpen de overbewegingen tegen te gaan, waardoor het afvallen afneemt of stopt.
Gewichtstoename
Gewichtstoename kan ontstaan door bepaalde medicamenten zoals antidepressiva en antipsychotica. Ook de aandrang om meer te gaan eten door bepaalde anti-parkinsonmedicatie, zoals pramipexol (Sifrol), komt voor. Evenals nachtelijk eten vanwege een extra behoefte aan zoet en vet. Het gewicht kan hierdoor duidelijk toenemen. Het is echter belangrijk om niet te veel aan te komen, omdat dit een extra belasting is voor de gewrichten en spieren. Bij overgewicht wordt bewegen extra moeilijk. Bij een hoger gewicht is het bovendien vaak noodzakelijk hogere doseringen antiparkinsonmedicijnen in te nemen, wat een extra belasting voor het lichaam betekent en waarbij de kans op bijwerkingen toeneemt.
Vertraagde maagontlediging
Vanaf het begin van de ziekte kan de maagontlediging vertraagd zijn. Dit betekent dat voedsel en ook de medicijnen veel langer in de maag blijven en daarom vertraagd opgenomen worden in de dunne darm. Dit kan de werking van de medicijnen beïnvloeden.
Problemen met de stoelgang
Obstipatie heeft te maken met verminderde darmbewegingen, waardoor de passage traag verloopt. Dit is bijna altijd het geval bij patiënten met de ziekte van Parkinson. Als de ontlasting moeilijk verloopt door te harde ontlasting of als er geen dagelijkse ontlasting meer is, is er sprake van obstipatie. Obstipatie kan als eerste klacht van de ziekte van Parkinson optreden, nog voordat de motorische verschijnselen zich aandienen.
Behandeling:
- domperidon om de darmbewegingen te stimuleren;
- voldoende drinken (anderhalve liter per dag);
- voldoende beweging;
- lauw water drinken op nuchtere maag;
- starten met ontbijt;
- vezelrijk eten en laxerende voedingsmiddelen gebruiken;
- laxerende medicijnen, zoals Duphalac of Movicolon.
Effect van vaak plassen
Als iemand vaak naar het toilet moet, kan dit ervoor zorgen dat er minder gedronken wordt. Dit kan ook nog versterkt worden door het ontbreken van een dorstgevoel. In de praktijk blijkt daarom voldoende vochtinname voor parkinsonpatiënten vaak een lastige opgave te zijn. Een praktisch hulpmiddel daarbij kan zijn het dagelijks gebruik van een anderhalve liter fles met water in de koelkast. Hiermee kan eenvoudig worden gecontroleerd of er die dag voldoende is gedronken.
Slikken en kauwen
Moeite met kauwen en slikken komt vaker voor in een gevorderd stadium van de ziekte. Er is een risico op verslikken, waardoor het voedsel in de luchtpijp terechtkomt met kans op luchtweginfecties.
Er is een aantal tips om hiermee om te gaan. Neem altijd kleine hapjes en neem geen nieuwe hap voordat de vorige is weggeslikt. Het drinken van koud water tussendoor bevordert de slikrefex. Ook een goede lichaamshouding tijdens het eten – rechtop zitten met het hoofd een beetje gebogen – kan het slikken verbeteren. Aangepast bestek en serviesgoed kunnen eveneens behulpzaam zijn. Overleg met de logopedist en een ergotherapeut kan bij slikklachten hulp bieden.
Samenvatting
Voor mensen met de ziekte van Parkinson is gezonde voeding van groot belang. Ook het bevorderen van een goede basisconditie staat hoog in het vaandel. Besproken wordt of parkinsonpatiënten (extra) behoefte hebben aan antioxidanten en vitamines. Van belang is verder te weten dat eiwitrijke voeding de opname van levodopa vanuit de darmen naar de bloedbaan kan vertragen. En dat de bijwerkingen van medicijnen voor problemen kunnen zorgen bij de inname en het verbruik van voeding. Bij ongeveer de helft van de parkinsonpatiënten komt gewichtsverlies voor ondanks voldoende inname van voedsel. Dit gebeurt vaker bij vrouwen dan bij mannen. Waarom is nog onduidelijk. Er kan ook een gewichtstoename ontstaan door bepaalde medicamenten zoals antidepressiva en antipsychotica. Parkinsonpatiënten kunnen ook last krijgen van een vertraagde maagontlediging, obstipatie of een verhoogde aandrang om te plassen. Het gevaar is dan dat iemand minder gaat drinken.
Ten slotte zijn kauwen en slikken van groot belang voor een goede voedselpassage en -opname.
Parkinson en seksualiteit
Zowel bij mannen als bij vrouwen heeft de ziekte van Parkinson gevolgen voor de seksualiteit. Welke problemen er kunnen ontstaan en wat daaraan eventueel te doen valt, komt in dit hoofdstuk aan bod.
De frequentie van seksueel contact vermindert meestal sterk bij parkinsonpatiënten. Ook de tevredenheid over het seksueel functioneren is vaak verminderd, vooral bij mannen. De aanpak van seksuele problemen bij de ziekte van Parkinson is geen eenvoudige zaak. Praten over de factoren die seksualiteit moeilijk maken ligt gevoelig, maar heeft vaak een therapeutisch effect. Bij de zaken die het vrijen verstoren, lijkt het zinvol om alleen die aspecten te bespreken waaraan iets te doen is. Vaak ervaren partners een verschil in seksuele behoeften. De arts kan proberen een eventueel negatief beeld van de partner (‘Hij wil seks door de medicijnen, niet door mij’) te veranderen. Door de nadruk meer op knuffelen en strelen te leggen kan de druk op de partner verminderen. De arts kan de patiënt voorstellen een medisch seksuoloog te raadplegen.
Praten
De seks kan om allerlei redenen minder aangenaam en leuk geworden zijn. De ziekte van Parkinson zelf kan de zin in seks doen afnemen, of soms juist onnatuurlijk doen toenemen door het gebruik van bepaalde medicijnen. Met name dopamine-agonisten kunnen ongewenste hyperseksualiteit veroorzaken. Daarnaast kan de ziekte van Parkinson functies aantasten die voor een goed seksleven noodzakelijk zijn, zoals het krijgen en behouden van een goede erectie en het vermogen tot zaadlozing. Een bevredigend seksueel contact wordt vaak moeilijk als de partner de verzorgersrol op zich moet nemen en er dan geen sprake meer is van een gelijkwaardige relatie. Ook het apart slapen vanwege nachtelijke problemen zoals onrustige benen of heftig dromen kan seks in de weg staan. Partners hebben nogal eens dubbele gevoelens en vinden het vaak moeilijk om hun emoties te bespreken, omdat ze bang zijn om de ander te kwetsen. In alle gevallen is het bespreekbaar maken van de problemen de belangrijkste eerste stap.
Het is belangrijk de oorzaak van de klachten te vinden. Daarom is een goede analyse van de problemen noodzakelijk. Het zoeken van hulp kan een drempel zijn, maar toch is het bespreken van de problemen heel belangrijk en kan dit als een opluchting ervaren worden. Het is belangrijk erachter te komen welke hulp u zoekt bij de problemen die u ervaart.
Praten over seks is in de praktijk niet gemakkelijk. Het is een intieme zaak tussen twee mensen. Hier met anderen over te spreken is een drempel die genomen moet worden. Maar inzicht in elkaars behoeften en de grenzen die er zijn, bieden mogelijkheid voor meer begrip en respect. De bakens verzetten door minder daadgericht te zijn, kan een bevrijdend gevoel geven. Zich richten op de dingen die nog wel lukken, bijvoorbeeld meer knuffelen en strelen, is ook een mogelijkheid. Seksualiteit is intimiteit! Aandacht geven aan elkaar is belangrijk. Zorg voor goede voorwaarden, zoals gezelligheid, en tijd voor elkaar. Geniet van elkaar. Probeer zo aantrekkelijk mogelijk te zijn, zorg voor een goede lichamelijke hygiëne. Plan de seks op momenten dat u zich fit voelt. Maak zo nodig gebruik van medicijnen of hulpmiddelen, maar zorg ook voor humor.
Mannen
Bij 60 tot 70 procent van de mannen komen erectiestoornissen voor en het niet tot stand komen van een orgasme en zaadlozing of voortijdige zaadlozing. De kwaliteit van het seksuele contact neemt af. De seksuele interesse kan ook afnemen door depressieklachten of door motorische problemen (tremor) waardoor er belemmeringen ontstaan om seksueel actief te zijn. Als het verlangen er wel is maar het niet lukt, kan dit als zeer frustrerend ervaren worden.
Bij de behandeling van erectiestoornissen moeten de volgende zaken worden overwogen:
- de aanwezigheid van hormonale stoornissen, zoals een te traag werkende schildklier, of een te lage testosteronspiegel (het mannelijke geslachtshormoon);
- het gebruik van PDE-5-remmers, zoals sildenafil (Viagra), tadalafil (Cialis) of vardenafil (Levitra), die erecties bij mannen kunnen bevorderen. De genoemde middelen verschillen onderling vooral door de werkingsduur. Een belangrijke bijwerking is het risico op plotselinge bloeddrukdaling na opstaan (orthostatische hypotensie). Deze middelen mogen niet gebruikt worden door patiënten met klachten over pijn op de borst of een recent hart- of herseninfarct (in de afgelopen zes maanden). Een nadeel van deze middelen is dat de seks hierdoor gepland en minder spontaan verloopt;
- een eventuele depressie. Deze moet zo nodig behandeld worden;
- het gebruik van alprostadil, dat via injecties in de penis voor een erectie kan zorgen.
Vrouwen
Ook bij vrouwen met de ziekte van Parkinson zijn er problemen met de lust, opwinding en orgasme. Het krijgen van een orgasme duurt vaak veel langer en is minder intens. Pijn tijdens de gemeenschap door te weinig opwinding en een te droge vagina zijn vervelende klachten. Bij oudere vrouwen kan ook de overgang hieraan extra bijdragen. Eventueel kan een glijmiddel worden gebruikt. Bij problemen met het orgasme kan een vibrator geprobeerd worden.
Het seksueel contact kan ook verminderen door lichamelijke factoren zoals overmatig transpireren, speekselvloed, incontinentie en door cognitieve veranderingen waardoor de partner als persoon veranderd is.
De invloed van medicijnen op seks
Als bijwerking van parkinsonmedicatie kan seksuele overstimulatie ontstaan. Veranderingen in het seksueel gedrag na het starten van parkinsonmedicatie is een aanwijzing voor overstimulatie. Dit kan ook pas na verloop van tijd ontstaan. Het voortdurend denken aan seks, veel vaker seksueel contact willen, en het bezoeken van pornosites kunnen zeer hinderlijke vormen aannemen die voor de directe omgeving alle grenzen overschrijdt. Dit kan uiteraard tot grote problemen in de relatie leiden.
Medicijnen kunnen daarnaast zorgen voor een ejaculatio praecox (vroegtijdig klaarkomen).
Vooral voor veel mannen is de combinatie van toegenomen lustbeleving met een afnemende mogelijkheid om een erectie en/of orgasme te krijgen een groot probleem. Medicatieaanpassing zal dan gericht moeten zijn op een afnemende lustbeleving en waar mogelijk een verbetering van de erecties.
Ook afname van lustgevoelens door medicijnen komt voor. Middelen die dit kunnen veroorzaken zijn bètablokkers, antidepressiva, slaapmiddelen en kalmeringsmiddelen.
Als partners er samen niet goed uitkomen, kan een verwijzing naar een seksuoloog gewenst zijn. Deze kijkt zowel naar lichamelijke, psychische alsook naar relationele factoren. Het kan zeer behulpzaam zijn dat een derde persoon met kennis van zaken de problemen helder en inzichtelijk maakt, zodat naar goede oplossingen gezocht kan worden.
Samenvatting
Zowel bij vrouwen als bij mannen heeft de ziekte van Parkinson gevolgen voor de seksualiteit. Vaak vermindert de frequentie van seksueel contact. Ook de tevredenheid over het seksuele contact neem af. De aanpak van die problemen is niet eenvoudig omdat het geen gemakkelijk gespreksonderwerp is. Maar praten kan wel helpen. De seks kan om allerlei redenen minder aangenaam en leuk geworden zijn. De ziekte van Parkinson zelf kan de zin in seks doen afnemen, of soms juist onnatuurlijk doen toenemen door het gebruik van bepaalde medicijnen. Met name dopamine-agonisten kunnen ongewenste hyperseksualiteit veroorzaken. Bij mannen kan de ziekte bovendien gepaard gaan met erectiestoornissen. Vrouwen kunnen problemen hebben met een veranderde lust, opwinding en orgasme.
Parkinson en rijvaardigheid
Medicijnen kunnen de rijvaardigheid beïnvloeden. Dit wordt aangegeven door een gele sticker op de medicijnverpakking. Hiermee wordt een verhoogd risico aangegeven, waar de patiënt en diens omgeving alert op moeten zijn. De Wegenverkeerswet (artikel 8.1) zegt hierover het volgende: ‘Het is eenieder verboden een voertuig te besturen, terwijl hij verkeert onder zodanige invloed van een stof, waarvan hij weet of redelijkerwijs moest weten (de gele sticker!!!) dat het gebruik daarvan de rijvaardigheid kan verminderen, dat hij niet tot behoorlijk besturen in staat moet worden geacht.’ Dat betekent dat de verantwoordelijkheid bij de bestuurder ligt nadat deze voldoende is geïnformeerd. Een gele sticker is dus geen absoluut verbod op autorijden, maar legt de verantwoordelijkheid voor het adequaat besturen bij de patiënt. Bij de geringste twijfel daarover dus niet autorijden!
Als iemand onder invloed van medicijnen met een gele sticker betrokken raakt bij een ongeval, is diegene wettelijk aansprakelijk. De verzekeraar vergoedt de schade dan in principe niet. De kosten van de veroorzaakte schade moeten dan zelf betaald worden. Probleem hierbij is wel de bewijslast van het feit dat iemand onder invloed van het betreffende middel het ongeval heeft veroorzaakt. Dat is niet zo eenvoudig, omdat eenzelfde dosis van een bepaald middel met gele sticker geheel verschillende effecten heeft op patiënten. Er bestaat ook een rode sticker op medicijnen. Die verbiedt heel duidelijk in alle omstandigheden autorijden in combinatie met het gebruik van de betreffende medicijnen.
Aanvragen/verlengen van het rijbewijs
Bij het aanvragen of verlengen van het rijbewijs voor personen boven de 75 jaar moet een ‘eigen verklaring’ worden ingevuld. Na deze leeftijd moet iemand in elk geval iedere vijf jaar worden herkeurd. Los van de leeftijd moet de diagnose ‘ziekte van Parkinson’ altijd worden gemeld bij het CBR. In deze verklaring moeten alle gezondheidsproblemen en het gebruik van medicijnen gemeld worden. Het CBR kan bepalen dat iemand op basis van het gebruik van bepaalde medicijnen niet meer mag rijden. Ook kan het CBR na inzage van de eigen verklaring besluiten tot het opleggen van een nader medisch onderzoek door een medisch specialist, bij voorkeur niet de behandelend specialist.
Daarnaast is het natuurlijk zo dat bij twijfel aan de rijgeschiktheid voor het 75ste jaar, bijvoorbeeld door toenemende cognitieve stoornissen, de eigen verantwoordelijkheid moet worden genomen om niet meer te rijden. In de praktijk blijken patiënten dit echter maar met moeite te kunnen besluiten, omdat het hun vrijheid ernstig beperkt.
Daarom is het in die gevallen raadzaam om een rijles te nemen om te zien of in de praktijk iemand nog rijgeschikt is. Een alternatieve mogelijkheid is het verrichten van een gevalideerde rijtest in een rijsimulator, die echter maar op een aantal plaatsen in Nederland kan worden afgenomen, onder andere in het UMC te Groningen. Ook kan de eigen verklaring zelf worden verkregen via de gemeente, zodat hiermee een formeel onderzoek door een onafhankelijk medisch specialist kan plaatsvinden, die dan een advies geeft over de rijgeschiktheid.
Op zich is de diagnose ziekte van Parkinson geen reden om niet meer auto te rijden. Maar de meeste patiënten overschatten zichzelf en doen er verstandig aan om de opmerkingen van hun familie of partner hierover serieus te nemen. Als een partner zich niet meer veilig voelt, soms aantoonbaar door diverse kleine ongevalletjes of aanrijdinkjes, dan is het verstandig hier nader onderzoek naar te laten doen. Het vroege optreden van problemen met planning en organisatie hebben vaak al heel snel een groot effect op de kwaliteit van het autorijden. Zie ook de website van het CBR: www.cbr.nl.
Samenvatting
Op zich is de diagnose ziekte van Parkinson niet voldoende reden om geen auto meer te rijden. Maar patiënten overschatten zichzelf vaak en zouden moeten proberen naar raadgevers te luisteren.
Parkinson, werk en inkomen
Werk en Parkinson hoeven elkaar niet in de weg te staan. Afhankelijk van de klachten die iemand heeft, kunnen er problemen ontstaan op het werk. Zodra de diagnose ziekte van Parkinson gesteld is, is het goed dit met de werkgever en bedrijfsarts te bespreken. Begrip kweken voor de aard van de ziekte bij werkgevers en collega’s kan bijdragen aan het tijdig zoeken naar aanpassingen in het werk en de werktijden. De wisselende klachten – minder energie hebben, trager denken en doen, vermoeidheid – zijn van invloed op de draagkracht en daarmee ook op de uitvoering van het werk. Zorg ervoor dat u niet tegen wil en dank het werk wilt volhouden zodat u uitgeput thuiskomt en er geen energie meer is voor activiteiten die zorgen voor ontspanning. Bespreek de problemen waar u tegenaan loopt met de bedrijfsarts. Ga ervan uit dat de kennis over de ziekte bij u aanwezig is en breng anderen op de hoogte. Aanvullende informatie over ziektebeeld en klachten kunt u vragen aan uw neuroloog en parkinsonverpleegkundige. De medische informatie kan na toestemming van de patiënt naar de bedrijfsarts gestuurd worden, waardoor er meer kennis en begrip ontstaat.
Verandering van werk en werktijden kan een opluchting zijn maar ook gevolgen hebben voor uw inkomen. Als u bijvoorbeeld een lagere functie accepteert, kan inkomensverlies het gevolg zijn. Voor het bespreken van dergelijke consequenties kan het inschakelen van een arbeidsdeskundige zinvol zijn; u kunt dit met uw behandelend neuroloog en parkinsonverpleegkundige bespreken.
Ziektewet
Als het niet lukt uw werk vol te houden, zal er gekeken worden naar een oplossing. Soms wordt ervoor gekozen om tijdelijk in de ziektewet te gaan. U krijgt minstens 70 procent van uw inkomen gedurende twee jaar aangevuld met een bedrag dat is vastgelegd in uw contract of in de geldende cao.
WIA
Als het niet lukt na een ziekteperiode van twee jaar het werk te hervatten, moet u een WIA-uitkering aanvragen bij het UWV. Er volgt dan een uitgebreide procedure. Het percentage van de arbeidsongeschiktheid bepaalt de hoogte van de uitkering. Daarnaast wordt gekeken of u ander soort werk, minder belastend dan uw eigen werk, nog wel zou kunnen verrichten, de zogeheten eigen verdiencapaciteit. De WGA-uitkering is een gedeeltelijke uitkering; hierbij is aangepast werken mogelijk. Samen met de werkgever wordt er gekeken hoe dit gerealiseerd kan worden. Het percentage dat u werkt, bepaalt uw inkomen. Voor het overige deel ontvangt u dan een uitkering.
De IVA-uitkering is een uitkering bij volledige arbeidsongeschiktheid: u ontvangt dan 75 procent van uw laatstverdiende loon.
Voor informatie: www.parkinsonenwerk.nl en www.uwv.nl.
Samenvatting
Werk en parkinson hoeven elkaar niet in de weg te staan, maar er kúnnen wel problemen ontstaan op het werk. Het is goed de diagnose met de werkgever en bedrijfsarts te bespreken. Als het niet lukt te blijven werken, kan een beroep worden gedaan op de ziektewet. Als na een ziekteperiode het werk niet kan worden hervat, behoort een WIA-uitkering tot de mogelijkheden.
De zorgcirkel rond de patiënt
Bij de zorg voor patiënten met de ziekte van Parkinson zijn vele disciplines betrokken. Om die allemaal goed te laten samenwerken is de zorg in regionale netwerken ondergebracht.
Organisatie van de zorg
Als het gaat om zorg staan uiteraard de patiënt en diens partner, indien aanwezig, als spil in het zorgproces centraal. De directe cirkel om de patiënt wordt gevormd door de parkinsonneuroloog en de parkinsonverpleegkundige. Daaromheen staan de huisarts, revalidatiearts, de specialist ouderengeneeskunde en de paramedische zorgverleners met specifieke deskundigheid. Vanaf het moment van diagnose tot aan eventuele opname in een zorginstelling is de neuroloog hoofdverantwoordelijke voor de behandeling. Maar de zorg voor parkinsonpatiënten omvat veel meer, en is echt teamwerk, waarin zeer veel disciplines betrokken zijn. Aan de Richtlijn Parkinson 2010 werkten maar liefst negentien disciplines mee, die allemaal een rol kunnen hebben in het zorgproces. Daarom moet al die zorg gecoördineerd worden, om doublures en hiaten te voorkomen. Voor deze regiefunctie is meestal de parkinsonverpleegkundige de meest aangewezen persoon, omdat zij vaak al veel spelers in het veld kent, waardoor contacten makkelijk verlopen.
Afhankelijk van de lokale situatie zouden ook andere hulpverleners deze rol op zich kunnen nemen. De laatste jaren hebben veel parkinsonverpleegkundigen zich ook gespecialiseerd in bepaalde complexe behandelingen voor de ziekte van Parkinson, zoals diepe hersenstimulatie (DBS), continue infusie met apomorfine of infusie van L-dopa via een PEG-sonde (Duodopa). Hierdoor zult u vaak een parkinsonverpleegkundige als eerste aantreffen om de noodzakelijke informatie over een dergelijke behandeling met u te bespreken en uitleg te geven over de consequenties van een dergelijke behandeling.
ParkinsonNet
Om ervoor te zorgen dat hulpverleners ook daadwerkelijk goed op de hoogte zijn van de nieuwste inzichten rondom de begeleiding en behandeling van patiënten met de ziekte van Parkinson, is ParkinsonNet ontwikkeld. Ieder lid van ParkinsonNet heeft aanvullende scholing ontvangen, zodat u ervan uit kunt gaan een kundige hulpverlener te treffen, als deze is aangesloten bij ParkinsonNet. Meer hierover kunt u vinden op de website van ParkinsonNet, www. parkinsonnet.nl. Op deze site kunt u via het submenu ‘Zorgzoeker’ op postcode alle getrainde parkinsonhulpverleners in uw directe omgeving opzoeken, waarbij gegevens van de betreffende hulpverleners, zoals adressen en telefoonnummers direct weergegeven worden.
Binnen het ParkinsonNet wordt iedere deelnemer geschoold om parkinsonpatiënten deskundig te kunnen behandelen. Hierbij maken zij gebruik van een beslissingsondersteunend elektronisch patiëntendossier. Verwijzers binnen ParkinsonNet maken gebruik van speciaal ontwikkelde ParkinsonNet-verwijsformulieren. Hiermee worden patiënten met een indicatie voor (paramedische) behandeling gericht verwezen. Hierdoor wordt de deskundigheid van de betrokken therapeuten verder vergroot, omdat dit leidt tot concentratie en specialisatie. De verwijzingen worden daarnaast ondersteund door een speciale ParkinsonNet-informatiefolder, waarin onder meer de namen en contactgegevens van ParkinsonNet-zorgverleners zijn opgenomen. Het concept ParkinsonNet is in 2006 beloond met de ‘Zorg voor Morgen Prijs’ voor de beste zorgvernieuwing in Nederland.
Omdat alle zorgverleners die zijn aangesloten bij het ParkinsonNet gemakkelijk met elkaar kunnen communiceren, bevordert dit de kwaliteit van de behandeling en de samenwerking tussen de zorgverleners. Uit onderzoek blijkt dat veel parkinsonpatiënten gebruikmaken van eerstelijns paramedische zorg (ergotherapie, fysiotherapie, oefentherapie en logopedie). Vanwege de complexiteit van de aandoening is parkinsonspecifieke deskundigheid een vereiste voor een adequate behandeling. Maar een probleem is dat paramedici die wel de benodigde specifieke deskundigheid hebben, niet altijd bekend zijn bij medisch specialisten en huisartsen, waardoor patiënten niet gericht naar hen doorverwezen worden. Door ook de medisch specialisten met expertise op het terrein van parkinson te laten aansluiten bij ParkinsonNet, kunnen onderlinge verwijzingen nu veel makkelijker tot stand komen en kan sneller gezamenlijk overleg over een patiënt plaatsvinden. Het is daarom van belang dat u vraagt aan uw hulpverleners of zij zijn aangesloten bij ParkinsonNet, omdat dit een kwaliteitskenmerk is en het daarnaast ook het onderlinge contact over uw behandeling met alle betrokken hulpverleners bevordert. De ParkinsonNet-leden kunnen onderling met elkaar communiceren binnen een beveiligd netwerk dat als zorgportaal dient voor patiënten en hulpverleners (zie www.parkinsonnet.nl).
Wetgeving en voorzieningen
Door uw ziekte is het mogelijk dat u een beroep moet doen op extra voorzieningen. Deze brengen vaak extra kosten met zich mee. Deze kosten worden geheel of gedeeltelijk vergoed via de onderstaande regelingen.
Zorgverzekering
Iedereen in Nederland is verzekerd voor ziektekosten. Er kan een persoonlijke keuze worden gemaakt voor een basispakket, al dan niet aangevuld met een aanvullend pakket. De inhoud van de aanvullende pakketten is afhankelijk van de premie en ook kunnen er per zorgverzekering verschillen zijn. Lees daarom altijd de polisvoorwaarden.
Als uw inkomen onder een bepaalde grens ligt, kunt u een tegemoetkoming in de zorgverzekeringskosten krijgen.
AWBZ
De AWBZ is de Algemene Wet Bijzondere Ziektekosten. Deze wet wordt uitgevoerd door de zorgkantoren. Om gebruik te kunnen maken van een AWBZ-voorziening is het nodig een CIZ (Centraal Indicatieorgaan Zorg)-indicatie aan te vragen. De AWBZ zal de komende jaren drastisch verschralen. Vele onderdelen zullen worden overgeheveld naar de Wmo, de Wet maatschappelijke ondersteuning die onder de gemeente valt.
Wmo
De Wet maatschappelijke ondersteuning regelt de vergoedingen voor mensen met een beperking met als doel zo lang mogelijk zelfstandig te blijven. Per gemeente verschilt de uitvoering van de Wmo. Vergoedingen: eenmalige of periodieke financiële tegemoetkoming; persoonsgebonden budget (PGB); voorzieningen in natura, bijvoorbeeld een rolstoel.
CIZ
Indicatie van het Centraal Indicatieorgaan Zorg (CIZ) is nodig om gebruik te kunnen maken van zorg, die valt onder de AWBZ. De indicaties worden steeds verder aangescherpt. Het verzorgingshuis als instelling zal verdwijnen; daarvoor in de plaats komen zorgappartementen die gehuurd kunnen worden en waar zorg kan worden ingekocht. In de toekomst zal het steeds moeilijker worden om in een verpleeghuis te gaan wonen. Het accent zal komen te liggen op het zo lang mogelijk thuis wonen.
PGB
Via AWBZ of Wmo kan het persoonsgebonden budget (PGB) worden aangevraagd als u zorg nodig hebt. U hebt meer vrijheid om de zorg zo te organiseren zoals het bij u past. Het budget dat wordt toegekend, is afhankelijk van de indicatie die het CIZ stelt. Het bedrag wordt niet meer automatisch overgemaakt naar uw persoonlijke rekening maar pas overgemaakt als u hebt laten zien waar u de zorg en de kosten aan besteed hebt. Dit om fraude te voorkomen. Ook kan een PGB via de zorgverzekering worden aangevraagd voor zorg die vergoed wordt. De procedure verschilt per zorgverzekeraar.
Thuiszorg/dagbehandeling/verpleeghuis/activiteitencentrum
Aan zorg van de thuiszorg en deelname aan een dagbehandeling of opname in het verpleeghuis is een eigen bijdrage naar inkomen verbonden vanaf achttien jaar. Aan de hoogte van de eigen bijdrage is een maximum verbonden. De eigen bijdrage wordt vastgesteld door het CAK, het Centraal Administratiekantoor. Een eigen bijdrage aan de AWBZ en Wmo is niet meer aftrekbaar van de belasting. Meer informatie biedt het Zorgboek Ziekte van Parkinson, het algemeen maatschappelijk werk in uw gemeente, en sociale raadslieden.
Hulpmiddelen en aanpassingen
Hulpmiddelen kunnen helpen de dagelijkse bezigheden te ondersteunen. Hulpmiddelen zijn nuttig en niet alleen bedoeld voor ernstige klachten. Ook kleine handigheidjes kunnen bepaalde handelingen makkelijker maken.
Er zijn talrijke hulpmiddelen beschikbaar. Veel hulpmiddelen kunnen een bepaalde periode geleend worden, bijvoorbeeld bij de thuiszorgwinkel. Het is verstandig het hulpmiddel een poosje te gebruiken om te kijken of het bevalt en of u ermee om kunt gaan alvorens het definitief aan te vragen. Hulpmiddelen kunnen worden aangevraagd bij de Wmo of de ziektekostenverzekeraar. De vergoeding is afhankelijk van de Wmo per gemeente (zorgloket) en uw zorgverzekering. Voor advies over hulpmiddelen kunt u terecht bij de ergotherapeut of de parkinsonverpleegkundige.
- Zitten
- Sta-op-stoel
- Trippelstoel
- Rolstoel
- Scootmobiel
- Lopen
- Nordic walking-stokken
- Rollator
- Hoge, stevige schoenen
- Lange schoenlepel
- Eten en drinken
- Keukenaanpassingen, zoals verlaagd aanrecht
- Aangepaste borden, bestek en antislipmat
- Tuitbeker met twee oren
- Rietje
- Trillepel (bij tremor)
- Wassen en douchen
- Handgrepen en steunen
- Verhoging toilet of verhoogde toiletpot
- Urinaal (man + vrouw)
- Aanpassing wastafels
- Beugels en handgrepen in douche, bad en toilet
- Aanpassing deurknoppen
- Antislipmat
- Communicatie
- Aangepaste pen (trilpen)
- Aangepaste toetsenbord, aangepaste muis
- Spraakversterker voor de computer
- Facetime
- Gesproken boeken
- Vergrootschermen
- Slapen
- Elektrisch verstelbaar bed
- Speciaal matras, kussen
- Licht dekbed, lichte dekens
- Gladde lakens
- Betty, pakpaal
- Hoog-laagbed
- Touwladder
- Wonen
- Drempels verwijderen
- Stoep/oprit aanpassen
- Handgrepen aanbrengen
- Trap- of personenlift installeren
- Gladde vloeren verwijderen
- Vloerkleden verwijderen
- Dagelijkse activiteiten
- Sokaantrekker
- Aan- en uitkleedstok
Zie ook de website van het Nederlands Technisch Advies College (NTAC), www.ntac.nl, voor informatie over hulpmiddelen.
Samenvatting
De directe zorgcirkel om de patiënt wordt gevormd door de parkinsonneuroloog en de parkinsonverpleegkundige. Daarnaast zijn er tal van anderen die hulp bieden, zoals een revalidatiearts, ergotherapeut, fysiotherapeut en logopedist. Om ervoor te zorgen dat zij goed op de hoogte zijn van de nieuwste inzichten rondom de begeleiding en behandeling, is ParkinsonNet (www.parkinsonnet.nl) ontwikkeld. Voor vergoeding van eventuele voorzieningen zijn er de zorgverzekering, AWBZ (met een indicatie van het CIZ) en Wmo. Tot slot is er aandacht voor de vele hulpmiddelen die de dagelijkse bezigheden kunnen ondersteunen, van scootmobiel tot gesproken boek.
Parkinsonzorg anno 2020
Het is zeer waarschijnlijk dat het zorglandschap voor parkinsonpatiënten de komende jaren fors gaat veranderen, ervan uitgaande dat er nog niet direct een behandeling beschikbaar zal zijn die het ziekteproces kan vertragen en/of stoppen. Hierbij speelt een aantal ontwikkelingen een belangrijke rol.
De vergrijzing
Allereerst is daar het bekende maar grote probleem van de vergrijzing. Hierdoor zal in de komende tien jaar het aantal parkinsonpatiënten fors toenemen, met een geschat aantal patiënten rond 2020 van 75.000! Hetzelfde zal gelden voor andere leeftijdsafhankelijke ziekten van het zenuwstelsel, zoals de ziekte van Alzheimer. Dit heeft enorme consequenties, want nu al lopen we tegen de grenzen aan van wat er nog betaald kan worden in de gezondheidszorg.
Daarom zal de komende jaren de nadruk liggen op efficiëntie en het maken van keuzes. Steeds vaker zullen patiënten zelf voorzieningen moeten betalen, als zij daar voor kiezen, omdat dit niet meer behoort tot het zogenoemde basispakket. Nu al worden bepaalde categorieën medicijnen niet meer vergoed en moeten ook parkinsonpatiënten het doen met generieke preparaten, die elke zes maanden kunnen wisselen, ondanks de grote verschillen in beschikbare werkzame stof die dit kan veroorzaken. Nu al hebben we dagelijks met de consequenties hiervan te maken.
Toenemende digitalisering
Veel ziekenhuizen hebben al geen papieren dossiers meer. Daarnaast kunnen steeds meer patiënten, zeker van de komende generaties, heel gemakkelijk omgaan met computers en internet en zal ook de communicatie tussen behandelaars en patiënten steeds meer via internet plaatsvinden.
Hiermee zijn de afgelopen tijd een aantal mooie initiatieven getest, die in de toekomst vrijwel zeker een belangrijke rol gaan spelen. Hierbij valt te denken aan het maken van afspraken via speciale websites van het ziekenhuis, op een moment dat de patiënt daar behoefte aan heeft. Nu is het zo dat er van tevoren afspraken worden gemaakt over zes weken of drie maanden, afhankelijk van de inschatting van de behandelaar. Vaak zou de patiënt echter liever later of eerder gezien worden, maar dat kan dan niet. Uit onderzoek blijkt dat als patiënten zelf rechtstreeks via internet een afspraak kunnen maken op het moment dat zij dat willen, er veel efficiënter kan worden gewerkt, omdat veel onnodige afspraken verdwijnen en de gemaakte afspraken veel beter aansluiten bij de wensen van patiënten. Hierin krijgt de patiënt dus veel meer de regie en dat zal in de toekomst steeds vaker het geval zijn.
Internet kan ook gebruikt worden om thuis alvast standaard vragenlijsten in te vullen, waardoor consulten efficiënter kunnen verlopen.
Ook bestaan er al mogelijkheden om via beveiligde FaceTime-verbindingen met de behandelaars contact te hebben, inclusief een videobeeld, waardoor extra bezoeken aan het ziekenhuis uitgespaard kunnen worden. Er zijn al digitale poliklinieken actief en
dit aantal zal de komende jaren alleen maar toenemen. Met dergelijke initiatieven bestaat in Nederland al goede ervaring, waarbij patiënten een platform kunnen creëren, waarop ze met hun behandelaars digitaal contact hebben, maar er ook voor kunnen zorgen dat de diverse behandelaars die betrokken zijn bij hun behandeling, ook gemakkelijk met elkaar contact kunnen hebben. Steeds vaker zullen dus livecontacten vervangen worden door digitale contacten, omdat blijkt dat daarmee al veel problemen en vragen opgelost kunnen worden.
Toenemende concentratie en specialisatie
Door het toenemende aantal mogelijkheden van behandeling en de complexiteit van de ziekte van Parkinson is specialisatie op dit terrein noodzakelijk, omdat anders niet meer de optimale zorg geleverd kan worden. De ontwikkeling dat bepaalde complexe aandoeningen niet meer door iedere medisch specialist behandeld worden, is ook gaande voor de ziekte van Parkinson. Geïnteresseerde parkinsonneurologen kunnen zich aansluiten
bij ParkinsonNet. De verzekeraars en de Inspectie van Volksgezondheid zetten zwaar in op verbetering van kwaliteit en de daarmee samenhangende concentratie van gespecialiseerde zorg. De komende jaren zullen hopelijk duidelijk maken, via onderzoek naar deze kwaliteit, dat specialisatie en concentratie een betere zorg opleveren in vergelijking met de situatie dat iedereen alles doet. Daarbij is het belangrijk dat de betrokken hulpverleners regionaal goed georganiseerd zijn, zodat iedereen van elkaar weet wat zijn of haar rol in het geheel is. Daarbij is goede en geprotocolliseerde samenwerking met de eerste lijn (huisartsen en thuiszorg) van groot belang, omdat de diverse hulpverleners nu vaak niet van elkaar weten wat door wie gedaan moet worden en al gedaan is. Veel zorg gaat nog over de hoofden van patiënten heen, en men vergeet de zorg samen met de patiënt te organiseren. Regionale samenwerking betekent ook dat de zorg zo dicht mogelijk in de directe omgeving van patiënten georganiseerd wordt. Ook dat heeft veel praktische voordelen.
Voorbeelden van dergelijke specialistische parkinsonnetwerken zijn inmiddels al voorhanden, onder andere in de noordelijke provincies van Nederland, onder de vlag Parkinson Platform Noord-Nederland (PPNN).
U kunt de hierbij behorende website raadplegen via: www.ppnn.info.
De patiënt centraal
In alle beleidsdocumenten van zorginstellingen staat dat bij alle activiteiten de patiënt centraal staat. De praktijk leert echter dat dit vaak maar deels het geval is, omdat allerlei andere belangen toch groter blijken te zijn.
Gezien alle ontwikkelingen die hierboven geschetst zijn, lijkt echter nu toch het moment aangebroken dat zorg echt rondom de patiënt georganiseerd gaat worden. Als patiënt en/of familielid met de ziekte van Parkinson wordt u hierbij aangemoedigd daarbij een rol te gaan spelen. Zoals zo vaak kan krapte een goede aanleiding zijn om creatief te gaan zoeken naar nieuwe mogelijkheden. Daarbij onderschatten patiënten te vaak hun eigen mogelijkheden. U zult in de toekomst veel meer dan nu het geval is, gevraagd worden de rol op u te nemen van initiator. Het gaat tenslotte om u. U bent ook nog eens de echte ervaringsdeskundige en u weet beter dan wie ook wat u eigenlijk echt zou willen. Maakt u alstublieft meer gebruik van deze mogelijkheden!
Het goede nieuws is dat de kansen voor deze benadering van gezondheidszorg, waarbij de patiënt echt centraal staat, de komende jaren zullen toenemen.
Atypische vormen van parkinsonisme
De ziekte van Parkinson is de meest voorkomende oorzaak van parkinsonisme. Naast de ziekte van Parkinson bestaat er een groot aantal andere ziekten die eveneens gepaard kunnen gaan met parkinsonisme. Deze ziekten kunnen dus op het eerste gezicht erg lijken op de ‘gewone’ ziekte van Parkinson, maar er zijn ook heel duidelijke verschillen, die vaak tijdens het ziektebeloop steeds meer aan het licht komen. Deze ziekten worden atypische parkinsonismen genoemd. In een vroege fase
is het dus lastig om met zekerheid vast te stellen of het om de ziekte van Parkinson gaat of om een vorm van atypisch parkinsonisme. De veelvoorkomende atypische vormen van parkinsonisme worden hierna besproken.
Postencefalitisch parkinsonsyndroom
Encefalitis, ontsteking van de hersenen (niet te verwarren met meningitis, een ontsteking van de hersenvliezen) kwam vroeger vaker voor dan nu. Tussen 1917 en 1926 raasde er een enorme epidemie over de wereld, die een groot aantal slachtoffers heeft gemaakt. Veel mensen hielden er een Parkinsonsyndroom aan over. Meestal openbaarden zich jaren na de epidemie pas de eerste verschijnselen.
De verschijnselen zijn hierbij ongeveer hetzelfde als bij de ziekte van Parkinson. Alleen openbaren de verschijnselen zich wat eerder (tussen het veertigste en vijftigste jaar) en komen ze vaak slechts aan één lichaamshelft voor. Ook het optreden van verkrampingen van de oogspieren (oculogyre crisis) is kenmerkend voor dit type parkinsonsyndroom.
Parkinsonsyndroom door vergiftiging
Bij geregeld contact met zware metalen (zoals kwik, koper, mangaan en lood), bijvoorbeeld in de werkomgeving, kunnen beschadigingen van de zwarte kernen ontstaan. Ook ten gevolge van een vergiftiging met koolmonoxide of pesticiden kan een parkinsonsyndroom ontstaan.
Parkinsonisme als bijwerking van medicijnen
Er zijn medicijnen die als werking of bijwerking de prikkeloverdracht van dopamine in de basale kernen afremmen, met als gevolg het optreden van parkinsonverschijnselen. Hierbij zijn de zwarte kernen zelf niet beschadigd en men spreekt in deze gevallen van parkinsonisme als gevolg van medicatie (drug-induced parkinsonisme).
De belangrijkste groep medicijnen die parkinsonisme kan veroorzaken, wordt gevormd door de antipsychotica. Dit is een grote groep van kalmerende middelen, die onder meer wordt voorgeschreven bij psychotische verschijnselen zoals hallucinaties en angstige waanideeën. Doordat antipsychotica de dopaminereceptoren blokkeren, veroorzaken zij een situatie die te vergelijken is met een tekort aan dopamine.
De parkinsonverschijnselen bij gebruik van antipsychotica, kunnen optreden bij het begin of na enige tijd en zijn afhankelijk van de dosering die gebruikt wordt. De individuele gevoeligheid voor parkinsonisme ten gevolge van antipsychotica is zeer verschillend en deze vorm van parkinsonisme komt vooral bij ouderen voor. Het parkinsonisme verdwijnt in de regel weer wanneer de dosering van de voor de bijwerking verantwoordelijke medicijnen wordt verlaagd of gestaakt.
Parkinsonisme als gevolg van antipsychotica reageert goed op levodopa en dopamine-agonisten en kan ook verbeteren na het stoppen van de veroorzakende medicijnen.
Vasculair parkinsonisme
Bij vasculair of ‘lower body’-parkinsonisme worden de parkinsonverschijnselen veroorzaakt door een slechte doorbloeding van de hersenen, vaak met één of meer herseninfarcten. Deze infarcten zitten dan vooral in de voorste hersenkwab. Vasculair parkinsonisme is herkenbaar aan een dribbelende loop met een normale armzwaai en heeft als belangrijk verschil met de ziekte van Parkinson het ontbreken van een goede reactie op levodopa (zie hoofdstuk 4).
MSA
MSA (multisysteematrofie) wordt gekenmerkt door een combinatie van parkinsonverschijnselen of ataxie (coördinatiestoornis, stuurloosheid) met autonome verschijnselen, zoals een lage bloeddruk bij opstaan, verlies van hartritmevariatie en een gestoorde blaasfunctie. Verder wordt MSA gekenmerkt door een verminderde of afwezige respons op levodopa.
PSP
PSP (progressieve supranucleaire paralyse) heeft naast bewegingstraagheid als belangrijkste kenmerken een uitgesproken stijfheid van de nek, sterke valneiging, trage oogbewegingen, verlies van spraak en later ook mentale achteruitgang.
DLB
DLB (dementie met Lewy-bodies) wordt gekenmerkt door verschijnselen van dementie met wisselende aandacht en een begin met hallucinaties, gevolgd door milde motorische verschijnselen later in het beloop.
CBD
De zeldzame aandoening CBD (corticobasale degeneratie) wordt gekenmerkt door uiteenlopende verschijnselen van sterke, asymmetrische stijfheid in een arm, gevoelsstoornissen en verlies van doelmatig handelen (apraxie).
Over de Parkinson Vereniging
De Parkinson Vereniging is een actieve vereniging die zich inzet voor een zo goed mogelijke kwaliteit van leven voor alle bijna 40.000 mensen met de ziekte van Parkinson of een parkinsonisme. De rol van partners en kinderen (soms tevens mantelzorger) krijgt ruim aandacht. Er zijn momenteel bijna 9000 leden, waarvan zo’n 300 zich inzetten als vrijwilliger voor de vereniging.
De Parkinson Vereniging heeft de volgende doelstellingen: regie in eigen handen, krachten bundelen, kennis verspreiden, meepraten en meebeslissen, onderzoek en ontwikkeling stimuleren, elkaar ontmoeten.
Onderdeel van deze doelstellingen zijn de, door de overheid vastgestelde, kerntaken van een patiëntenvereniging: lotgenotencontact (elkaar ontmoeten en ervaringen uitwisselen), belangenbehartiging (door lobby bij overheid, politiek en zorgverzekeraars) en informatievoorziening (om bewustwording te creëren en kennis te vergroten).
Regie in eigen handen
Zelfmanagement of zelf de regie houden (of pakken) over je ziekte: het is een hot issue binnen de zorg. De hele maatschappij wordt mondiger, daar is de patiënt zeker geen uitzondering op. Zelf de regie nemen over de ziekte is een logisch gevolg van deze groeiende mondigheid. Maar het is wel belangrijk dat de patiënt de regie neemt op basis de juiste informatie én competenties. Hier ziet de Parkinson Vereniging, als vertegenwoordiger van alle parkinsonpatiënten in Nederland, een belangrijk rol voor zichzelf.
Daarom ontwikkelt de Parkinson Vereniging samen met een aantal samenwerkingspartners verschillende (online) hulpmiddelen en trainingen om de patiënt te helpen deze regie in handen te krijgen.
Krachten bundelen, meepraten en meebeslissen
De Parkinson Vereniging praat en beslist mee over beleid met als doel bewustzijn over de ziekte van Parkinson en de mens met Parkinson te creëren. Zo is de vereniging met lokale en landelijke media in gesprek en is zij aangesloten bij de koepelorganisatie Nederlandse Patiënten en Consumenten Federatie.
Kennis verspreiden
Kennis verspreiden door inzet van alle middelen op het gebied van communicatie en informatievoorziening gericht op patiënt, partner, professional en publiek.
De Parkinson Vereniging biedt in vele vormen informatie aan. Dit gebeurt tijdens landelijke of regionale bijeenkomsten, en in de vorm van brochures, flyers en de digitale nieuwsflits. Ook Parkinson Magazine is een belangrijke bron van actuele informatie voor vele patiënten.
Onderzoek en ontwikkeling
De Parkinson Vereniging initieert en subsidieert onderzoek, voornamelijk projecten die resultaat kunnen opleveren voor de patiënt van nú. De Parkinson Vereniging zet zich daarnaast in voor patiëntenparticipatie in onderzoek waarbij op verschillende manieren patiënten worden betrokken bij projecten.
Lidmaatschap Parkinson Vereniging
Leden van de Parkinson Vereniging:
- ontvangen vijf keer per jaar Parkinson Magazine:
- tijdschrift met laatste nieuws over de ziekte van Parkinson en parkinsonismen, onderzoek en de vereniging
- krijgen korting op trainingen en cursussen
- krijgen korting op landelijke activiteiten
- krijgen korting op Parkinson en nu? van Spreekuur Thuis
- hebben toegang tot een breed netwerk van contactpersonen en Parkinson Cafés. Kijk voor meer informatie op www.parkinson-vereniging.nl/indebuurt .
De contributie wordt vaak vergoed door de aanvullende zorgverzekeringen. Kijk in uw polis voor meer informatie.
Contact
- Parkinson Vereniging
- www.parkinson-vereniging.nl
- e-mail: info@parkinson-vereniging.nl
- telefoon: (030) 656 13 69
www.cbr.nl
www.hethic.nl
www.mailfemale.co
www.mantelzorg.nl
www.mijnparkinsonzorg.nl
www.nvlf.nl
www.nvsh.nl
www.nvvs.info
www.parkinsonliga.be
www.parkinsonnet.nl
www.parkinson-vereniging.nl
www.parkinsonwerk.nl
www.parkinsonzorgzoeker.nl
www.ppnn.info
www.stichtingseptember.nl