Geen producten in de winkelwagen.
Schildklierafwijkingen

Schildklierafwijkingen komen vaak voor, in Nederland bij meer dan een half miljoen mensen van alle leeftijden voor, bij vrouwen viermaal zo vaak als bij mannen. Omdat schildklierafwijkingen in verschillende vormen voorkomen, bestaat er ook een grote verscheidenheid aan klachten, die niet altijd gemakkelijk worden herkend. Hier wordt helder uiteengezet wat de werking en de functie van de schildklier is. Daarnaast komen diagnostiek, aandoeningen en therapie uitgebreid aan de orde.
Bestel ons boek over Schildklierafwijkingen
Wat is de schildklier en wat doet hij?
De schildklier is een vlindervormig orgaan van ongeveer 10 ml (gram) dat zich aan de voorzijde onder in de hals bevindt, onder het strottenhoofd, tegen de luchtpijp. De schildklier bestaat uit twee delen die we kwabben of lobben noemen, waarvan er een aan de linkerkant zit, de linkerkwab, en een aan de rechterkant, de rechterkwab. De twee kwabben – het Latijnse woord voor kwab is
lobus – zijn met elkaar verbonden door een smalle, nauwe verbinding die we istmus (engte) noemen. Soms is vanuit deze istmus naar boven toe nog een streng te zien, de lobus pyramidalis. Deze streng is een restant van een tijdelijke verbinding tussen de schildklier en een opening achter op de tong. Die tijdelijke verbinding ontstaat bij het embryo op het moment dat de schildklier afdaalt in de keel. Dit ‘pad’ waarlangs de schildklier afdaalt, heet ductus thyreoglossus en verdwijnt (vrijwel altijd) vóór de geboorte (zie figuur 1).
Meestal is de schildklier bij het slikken aan weerszijden van de adamsappel te voelen (en soms te zien).
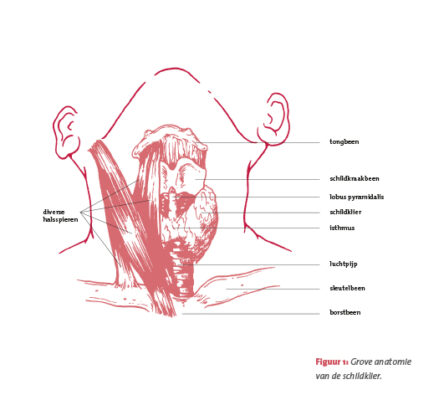
Wat doet de schildklier?
De schildklier maakt schildklierhormonen aan. Hij maakt voornamelijk thyroxine (T4, ca. 100 microgram (µg) per dag) en in mindere mate trijodothyronine (T3, ca. 6 µg per dag). T3 is in feite het actieve schildklierhormoon. T3 kan direct door de schildklier worden gemaakt, maar de grootste hoeveelheid T3 wordt in de verschillende weefsels van het lichaam gemaakt uit T4, dat veel minder actief is dan T3.
Om het schildklierhormoon te kunnen aanmaken, heeft de schildklier jodium nodig. Zowel T4 als T3 bevat jodiumatomen; T4 bevat vier atomen en T3 bevat er drie. We komen later nog terug op de rol van jodium in dit proces.
Hoe worden de processen geregeld?
De werking van de schildklier wordt geregeld door de hypofyse. Dit is een klein orgaan dat als een aanhangsel onder aan de hersenen zit. Deze hypofyse, die we dus ook wel hersenaanhangselklier noemen, produceert talrijke hormonen. Een van die hormonen, het zogenaamde thyreoïd-stimulerend hormoon (TSH) of thyreotropine, zet de schildklier aan tot de productie van het schildklierhormoon. Op zijn beurt staat de hypofyse overigens weer onder controle van de hypothalamus (een hoger hersencentrum), die het thyreotropin-releasing hormone (TRH) produceert.
De werking van de schildklier wordt evenwel niet alleen ‘van buitenaf’ geregeld. In de schildklier vindt namelijk ook een soort zelfregulering plaats. Die zelfregulering houdt in dat de schildklier de opname van het jodium tijdelijk kan verminderen als er te veel van in de omgeving (het bloed) aanwezig is.
De werking van het hypofyse-hormoon TSH wordt voor een deel weer afgeremd door de schildklierhormonen T4 en T3. Deze afremming van TSH vindt plaats door middel van een negatief terugkoppelingsmechanisme en alhoewel T4 wordt opgevat als een voorstadium voor het hormoon T3, verloopt de terugkoppeling naar TSH voornamelijk via dit T4. Dit is mogelijk omdat de hypofyse in staat is om T4 om te zetten in T3, wat we dan weer lokale of perifere conversie noemen. Het lijkt er overigens op dat niet alle organen in het lichaam in staat zijn om in dezelfde mate T4 in T3 om te zetten, zoals de hypofyse dat kan.
Het schildklierhormoon wordt in het bloed vervoerd door eiwitten, waarbij het voor meer dan 99,5% aan die eiwitten gebonden is, en dan in het bijzonder aan het thyroxinebindend globuline (TBG), het thyroxinebindend prealbumine (TBPA) en aan het albumine. Het kleine vrije deel is in feite het actieve hormoon.
Na vervoer worden T3 en T4 in de weefsels opgenomen. Het T4 wordt dan voor een deel omgezet in het actieve T3 (perifere conversie) en voor een deel afgebroken. Het T3 heeft zijn effect via de T3 kernreceptor. De afgebroken bestanddelen van het schildklierhormoon komen terecht in de enterohepatische (darm-lever) kringloop.
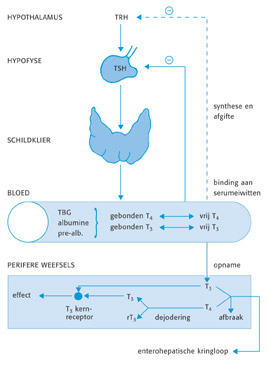
Schematisch overzicht van de stofwisseling van schildklierhormoon.
Bij de perifere conversie kan ook het waarschijnlijk biologisch inactieve reverse T3 (r T3) gevormd worden. Zowel T3 als r T3 worden uit T4 gevormd door afsplitsing van één jodiumatoom van respectievelijk de buiten- en binnenring van het T4-molecuul.
Wat doen de schildklierhormonen?
De schildklierhormonen regelen groei en ontwikkeling, beïnvloeden de stofwisseling en stimuleren de warmteproductie. Ze hebben een positief effect op het hart en hebben zo invloed op de meeste lichaamsprocessen. Een tekort aan schildklierhormoon leidt tot vertraging van die processen. Hierdoor kunnen klachten ontstaan zoals vermoeidheid, kouwelijkheid, slaapzucht, droge huid, obstipatie en menstruatiestoornissen. Een teveel aan schildklierhormoon kan onder meer leiden tot een niet ongevaarlijke versnelling van de hartfrequentie: het hart kan zelfs geheel ‘op hol slaan’. Ook is schildklierhormoon belangrijk voor de ontwikkeling. Zowel de lichamelijke als de geestelijke ontwikkeling van baby’s en kinderen is afhankelijk van de goede hoeveelheid beschikbare schildklierhormonen.
Werking van het schildklierhormoon
Om de werking van het schildklierhormoon beter te begrijpen, is het belangrijk te weten dat het T3 zich aan een ontvangend eiwit bindt, dat we de receptor noemen. Zo’n receptor bevindt zich in de kernen van vrijwel alle lichaamscellen.
Als de binding tussen T3 en de receptor heeft plaatsgevonden, zullen zij samen (het T3-receptorcomplex genoemd) zich binden aan het DNA. Door te binden aan het DNA beïnvloedt schildklierhormoon de productie van allerlei eiwitten (eiwitsynthese) in ons lichaam.
Belang van jodium
Zoals gezegd is voor de opbouw van schildklierhormoon jodium nodig. Jodium kennen we in de praktijk vooral als een middel waarmee wonden worden ontsmet, maar het is ook een noodzakelijk onderdeel van onze voeding. Jodium krijgen we dagelijks via de voeding binnen en wel voornamelijk door het eten van jodiumhoudend zout (ook in brood), melk en vis. Jodium wordt vervolgens actief vanuit het bloed via de schildkliercelmembraan de schildklier in getransporteerd. Hetzelfde gebeurt overigens met tyrosine, een van de zogeheten essentiële aminozuren. Aminozuren zijn de bouwstoffen waaruit eiwitten in ons lichaam worden gemaakt. De toevoeging ‘essentieel’ wil zeggen dat een aminozuur niet door het lichaam zelf wordt aangemaakt, maar net als jodium met het voedsel binnen moet komen.
Het uiteindelijke effect van het schildklierhormoon ligt bij de beïnvloeding van de eiwitsynthese. Uit de opgenomen tyrosines en het jodium worden op het thyreoglobuline-eiwit (T) twee stoffen gevormd: het monojodotyrosine (MIT) en het dijodotyrosine (DIT). Als dat is gebeurd, kan er koppeling plaatsvinden tot T4 (DIT + DIT) en/of T3 (MIT + DIT), wat plaatsvindt onder invloed van een peroxidase-enzym. Daarmee heeft het schildklierhormoon daadwerkelijk vorm gekregen.
Het gevormde schildklierhormoon wordt vervolgens opgeslagen in het colloïd van de schildklier. Dit is de halfvloeibare massa in de follikels of blaasjes van de schildklier. Van daaruit wordt het hormoon vervolgens afgegeven aan het bloed. Een deel wordt ten slotte weer afgebroken tot MIT en DIT en verder van jodium ontdaan (dejodering), zodat dit jodium weer beschikbaar is voor de aanmaak van nieuw schildklierhormoon (zie figuur 3). De meeste van deze processen staan onder invloed van TSH.
Een ernstig tekort aan jodium kan leiden tot mentale retardatie en uiteindelijk ook tot cretinisme, wat in Nederland vrijwel niet voorkomt, vroeger in Zwitserland en ook elders in de wereld wel. Voorbeelden van cretins zijn op blz. 19 afgebeeld.
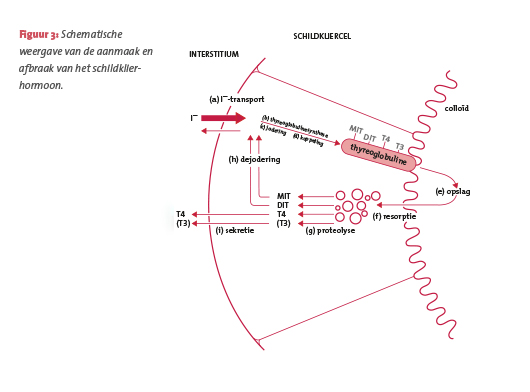
Perifere conversie
In de schildklier wordt voornamelijk T4 gemaakt en slechts een klein gedeelte van het T3. Het meeste T3 in het serum is afkomstig uit de perifere conversie in de diverse organen. Met perifere conversie wordt hier bedoeld de omzetting van T4 in T3 in verschillende organen, vooral in de lever.
Subklinische aandoeningen
Per individu is de serumconcentratie van T4 en T3 vrij constant. Daardoor is het wellicht mogelijk dat er subklinische aandoeningen zijn waarbij de waarden van het schildklierhormoon nog in de vrij brede normale range liggen, terwijl er toch al sprake is van een afwijkend TSH. Dit kan wijzen op een iets verhoogde of verlaagde schildklierhormoonproductie. Verschijnselen zijn er dan in het algemeen niet of nauwelijks, vandaar dat er gesproken wordt van subklinische schildklierafwijkingen.
Schildklierhormoontekort
Omdat de schildklierhormonen invloed hebben op ongeveer alle (stofwisselings)processen in het lichaam, kan een zuigeling zich lichamelijk en geestelijk niet ontwikkelen zonder schildklierhormoon. Een kind of volwassene kan zonder schildklierhormoon evenmin normaal leven, alles gaat als in een vertraagde film. Als een ernstig tekort aan schildklierhormoon niet wordt behandeld, kan het uiteindelijk zelfs dodelijk zijn.
Onderzoek en diagnose
Afwijkingen van de schildklier kunnen we indelen in afwijkingen van de vorm en stoornissen in het functioneren. Deze aspecten kunnen uiteraard ook gecombineerd voorkomen, vandaar dat allebei goed moeten worden bekeken.
De diagnostische mogelijkheden bij schildklieraandoeningen zijn divers en staan vermeld in tabel 1. In eerste instantie is het belangrijk om te vragen (anamnese) naar het bestaan van klachten die bij een afwijkende schildklierfunctie passen (functioneren), maar net zo belangrijk is het om te vragen naar de eventuele bestaansduur en veranderingen van een geconstateerde struma (vorm). Daarbij moet de arts ook altijd nagaan of soortgelijke of andere schildklieraandoeningen in de familie voorkomen.

Lichamelijk onderzoek
Bij het lichamelijk onderzoek kijkt de arts eerst naar de schildklier, al of niet na slikken. Vervolgens zal hij de schildklier palperen (bevoelen) waarbij hij let op de consistentie, de beweeglijkheid, de samenhang met de huid of onderliggende weefsels, de grootte en op eventuele knobbels (noduli). Bij verdenking op hyperthyreoïdie kan de arts ook nog luisteren of er een geruis is over de schildklier. Hoort hij dat geruis, dan bewijst dat de aanwezigheid van hyperthyreoïdie.
Bij een bepaalde vorm van hyperthyreoïdie, de ziekte van Graves, komen specifieke oogafwijkingen voor en kan er sprake zijn van opgezette onderbenen (pretibiaal myxoedeem).
Bloedonderzoek
Voor het vaststellen van de functie van de schildklier is het vaak genoeg om de serum TSH-concentratie te meten, de meest gevoelige waarde voor schildklieraandoeningen. Als het TSH normaal is, betekent dit over het algemeen dat de functie van de schildklier normaal is. Een verlaagd TSH wijst er vrijwel altijd op dat er te veel schildklierhormoon is. Om daar helemaal zeker van te zijn, kan er een FT4-bepaling worden gedaan, die eventueel wordt aangevuld met een bepaling van de T3-spiegel.
De T3-bepaling is vooral van belang als de TSH-waarde laag is en er dus gedacht wordt aan hyperthyreoïdie, terwijl de FT4 normaal is. Als deze situatie zich voordoet, kan er (in 15 procent van de gevallen) sprake zijn van een zogenoemde T3-toxicose; dit is een hyperthyreoïdie met normaal FT4 en verhoogd T3.
Een verhoogd TSH wijst erop dat het functioneren van de schildklier tekortschiet. Hoe ernstig hij tekortschiet, kan worden bepaald aan de hand van een hierop volgende FT4-bepaling. Bij het zoeken naar de oorzaak van een schildklierfunctiestoornis kan bloedonderzoek soms ook behulpzaam zijn. De referentiewaarden staan opgesomd in tabel 2.
Bij bloedonderzoek kan ook het CPK (creatine fosfokinase) verhoogd zijn, wat past bij de bij hypothyreoïdie optredende myopathie (spieraandoening).

Antilichamen
Op het moment dat er in het lichaam stoffen binnendringen die als lichaamsvreemd worden beschouwd, zogeheten antigenen, reageert het afweersysteem van het lichaam daarop door antistoffen of antilichamen aan te maken. Zulke antilichamen zijn van nature in het lichaam aanwezig of moeten door het lichaam worden gemaakt zodra dat nodig is. Soms kan het lichaam antistoffen maken die lichaamseigen cellen of weefsels aantasten of zelfs afbreken. Het lichaam breekt als het ware zichzelf af. In dat geval spreken we van een auto-immuunziekte.
Nu zijn er diverse antilichamen die tegen de schildklier gericht kunnen zijn en die de schildkliercellen kunnen beïnvloeden. Een van de auto-immuunziekten die te maken hebben met de schildklier, is de ziekte van Hashimoto. Bij deze ziekte, die uiteindelijk meestal leidt tot hypothyreoïdie door het langzaam stuk gaan van schildklierweefsel, komen antilichamen voor tegen met name schildklierperoxidase (TPO = thyroid peroxidase) en thyreoglobuline. De laatste komt bij 5 procent van de algemene bevolking voor en is dus minder specifiek.
In combinatie met de ziekte van Hashimoto kunnen ook andere auto-immuunziekten optreden, zoals type 1 diabetes en pernicieuze anemie (een bijzondere vorm van bloedarmoede). Daarbij worden antilichamen tegen bepaalde maagcellen gemaakt, waardoor vitamine B12 niet goed wordt opgenomen. Hierdoor kan bloedarmoede ontstaan en in dat geval zijn vitamine B12-injecties of tabletten nodig.
Bij de ziekte van Graves is eerder sprake van schildklierstimulerende antilichamen (TSAb = thyroid stimulating antibodies = TSH receptor antilichamen of TSI = thyreoid stimulerende immunoglobulines). Deze antilichamen worden bij de meeste patiënten met Graves’ hyperthyreoïdie gevonden. Deze antistoffen kunnen in een deel van de patiënten ook de oogverschijnselen (Graves’ orbitopathie) veroorzaken.
De antilichamen die bij de ziekte van Hashimoto worden gevonden, kunnen ook bij de ziekte van Graves voorkomen. Zij hebben kennelijk bij deze ziekte niet de overhand.
Tumormerkers
Nog specifieker is het onderzoek naar bepaalde schildkliertumormerkers die vooral hun waarde hebben bij de nabehandeling van bepaalde vormen van schildklierkanker.
Zo maakt men bij de nabehandeling van een behandeld folliculair of papillair schildkliercarcinoom gebruik van het serum thyreoglobulinegehalte. Als na volledige verwijdering van de schildklier het thyreoglobuline niet onmeetbaar laag is, moeten er ergens in het lichaam cellen aanwezig zijn. Als dat zo is, heeft de patiënt vaak aanvullende behandelingen nodig.
Overigens kan het thyreoglobulinegehalte ook gebruikt worden bij sommige patiënten met hyperthyreoïdie waarbij de oorzaak onduidelijk is. Als er geen sprake is van een te hard werkende schildklier, maar de patiënt al of niet bewust schildklierhormoon in een (te) hoge dosering slikt is bij hem het serum thyreoglobuline onmeetbaar laag.
Een andere tumor is het medullair schildkliercarcinoom. Deze tumor maakt calcitonine, een stof die normaal (in kleine hoeveelheden) in de C-cellen in de schildklier wordt gemaakt. C-cellen zijn cellen in de schildklier die geen schildklierhormoon maken en eigenlijk tot het zenuwstelsel behoren. Bij het medullair schildkliercarcinoom wordt calcitonine in verhoogde hoeveelheden afgescheiden. Na definitieve behandeling hoort de calcitonineconcentratie in het bloed onmeetbaar laag te zijn. Ook maakt het medullair schildkliercarcinoom vaak de tumormerker CEA, een stof die ook gemaakt wordt door darmtumoren. Bij patiënten die behandeld zijn voor medullair schildkliercarcinoom worden vaak zowel calcitonine als CEA bepaald om in de gaten te houden of de tumor terugkomt.
Afbeeldend onderzoek
Voor afbeeldend onderzoek wordt voornamelijk gebruikgemaakt van scintigrafie en echografie.
Scintigrafie
Scintigrafie is een onderzoek waarmee, na injectie van een kleine hoeveelheid radioactief gemerkt jodium of technetium, de schildklier kan worden afgebeeld. Dat is vergelijkbaar met het inspuiten van contrastvloeistof om aandoeningen aan zachte weefsels in het lichaam zichtbaar te maken.
Het voordeel van de scintigrafie is dat schildklierweefsel dat te veel of te weinig schildklierhormoon maakt ook jodium of technetium abnormaal zal concentreren. Scintigrafie wordt met name gebruikt om de oorzaak van een hyperthyreoïdie vast te stellen. Indien er sprake is van een ontsteking van de schildklier (thyreoïditis) zal er geen opname zijn van jodium of technetium, terwijl bij de ziekte van Graves de opname van jodium of technetium in de hele schildklier verhoogd is. Ook knobbels kunnen zichtbaar worden gemaakt als respectievelijk koude (weinig radioactiviteit opnemende) of warme (veel radioactiviteit opnemende) knobbels. Ook een meer knobbelige struma, de multinodulaire struma, kan zo goed worden vastgesteld (zie figuur 4). Dit laatste kan echter ook met echografie.

De stralenbelasting bij nucleaire scintigrafie is vrijwel te verwaarlozen. Het onderzoek is evenwel arbeidsintensiever en duurt langer dan de echografie. In bepaalde gevallen heeft scintigrafie een meerwaarde boven echografie, zoals bij een afwijkende (te hoge) schildklierfunctie. Om na te gaan of er nog schildklierweefsel is achtergebleven nadat de schildklier helemaal is weggehaald in verband met een schildkliercarcinoom, is het maken van een scintigrafie nuttig. Net zo nuttig is zo’n scan overigens bij schildklierontstekingen waarbij meestal geen of weinig jodium wordt opgenomen. Met radioactief jodium worden ook total body scans, oftewel scans van het hele lichaam gemaakt. Dat gebeurt na therapie met radioactief jodium om te zien of zich nog ergens jodium ophoopt, wat kan wijzen op een uitzaaiing van het schildkliercarcinoom.
Echografie
Echografie is tegenwoordig het meest gebruikte afbeeldend onderzoek bij schildklierpatiënten. Via geluidsgolven wordt de anatomie van de schildklier en omgeving afgetast. Niet alleen kan zo de grootte van de schildklier worden bepaald, maar ook wordt gezien of er al of niet knobbels aanwezig zijn. Ook het aspect van knobbels, en dan in het bijzonder of er in zo’n knobbel (nodus) vocht zit (cyste) of dat er sprake is van abnormaal weefsel, is vaak goed te zien (zie figuur 5). De geoefende echografist of radioloog kan bepaalde kenmerken opsporen, die de verdenking op een kwaadaardige tumor vergroten. Dit zijn: microcalcificaties (kleine verkalkingen), het ontbreken van een halo (een lichte rand om de nodus), onregelmatige begrenzingen, toegenomen bloedstromen in de nodus en een echoarm karakter van de nodus.
Bovendien geeft het onderzoek geen stralenbelasting en kan het dus gemakkelijk worden herhaald. Nadeel is dat bij heel veel mensen kleine knobbeltjes worden gevonden die in feite niet van belang zijn (incidentalomen).
Overig radiologisch en/of nucleair onderzoek
Veel minder vaak zal gebruik worden gemaakt van CT-(computerized tomography) scanning, MRI-scanning (magnetic resonance imaging) of een PET-scan.
Is er sprake van een struma die zo groot is dat hij reikt tot in de borstholte, dan kan een CT- of MRI-scan behulpzaam zijn bij het afbakenen van de afwijkingen. De echografie is daarvoor minder goed bruikbaar. Ook bij oogafwijkingen die bij de ziekte van Graves passen, zeker als ze eenzijdig zijn, is een CT- of MRI-scan zinvol. In het geval van schildklierkanker wordt soms ook een CT of MRI van de hals gemaakt om de uitgebreidheid van ziekte vast te stellen. Dit gebeurt vooral wanneer een patiënt mogelijk opnieuw in dit gebied geopereerd moet worden. Ten slotte kunnen deze onderzoeken in specifieke gevallen worden gebruikt om uitzaaiingen van schildklierkanker op te sporen, bijvoorbeeld in de borstholte (CT) of van de lever (MRI).
Conventioneel radiologisch onderzoek in de zin van een röntgenfoto van borstholte (thorax) en luchtpijp (trachea) kan zichtbaar maken of er sprake is van verdringing en/of vernauwing van de luchtpijp door een struma. Omdat de patiënt daarbij vooral hinder ondervindt bij de inademing, is soms een longfunctieonderzoek zinvol om een inademingsbelemmering op te sporen. Als er afwijkingen worden gevonden bij radiologisch of longfunctieonderzoek kan dit een reden zijn om de struma te verkleinen.
Bij een FDG-PET-scan krijgt een patiënt gelabeld suiker (fluorodeoxyglucose, afgekort FDG) toegediend. Dit gelabelde suiker zal vooral worden opgenomen door weefsels met een hoge stofwisseling (energieverbruik), en kan zo in specifieke gevallen gebruikt worden om bijvoorbeeld uitzaaiingen op te sporen.
Cytologisch onderzoek
Als bij lichamelijk onderzoek of bij echografie één (prominente) of meer knobbels worden vastgesteld, kan met een punctie worden vastgesteld of de knobbels wellicht kwaadaardig zijn (zie figuur 6).
Bij de punctie, die slechts kort duurt, wordt eerst een dunne naald in de betreffende knobbel gestoken. Vervolgens zuigt men cellen op door middel van een spuit, waarmee men vacuüm zuigt. Deze punctie is weinig pijnlijk en kan gemakkelijk worden herhaald. De punctie dient altijd plaats te vinden onder echografische controle, zodat de naald kan worden geplaatst op de positie waar de knobbel op het echobeeld er het meest verdacht uitziet.
De opgezogen cellen worden microscopisch onderzocht om vast te stellen of het om een goedaardige of een kwaadaardige verandering gaat. Een kwaadaardige verandering komt gelukkig niet zo vaak voor. Eventueel kan zelfs een ontsteking worden opgespoord, maar ook dit wordt niet zo vaak gezien. Helaas komt het een enkele keer voor dat het cytologisch onderzoek niet goed kan worden uitgevoerd, omdat de punctie onvoldoende celmateriaal heeft opgeleverd. Herhaling van de punctie is dan aangewezen.
In een deel van de gevallen worden bij cytologisch onderzoek aanwijzingen gevonden waardoor een maligniteit (kwaadaardigheid) niet goed is uit te sluiten. In die gevallen is vaak aanvullend weefselonderzoek (histologie, zie onder) noodzakelijk. In het bijzonder het folliculair adenoom, een goedaardig gezwel, is met behulp van cytologie niet van een carcinoom te onderscheiden. Hierdoor moeten patiënten helaas vaak geopereerd worden voor een afwijking die achteraf goedaardig blijkt te zijn. Er vindt op dit moment daarom veel onderzoek plaats naar bepaalde moleculaire merkers, die bij aanwezigheid de kans op een kwaadaardigheid vergroten. Dit onderzoek is met name nuttig als het cytologisch onderzoek niet geheel conclusief is. Het onderzoek wordt echter nog niet algemeen toegepast.
Histologisch onderzoek
Als tot histologisch (= weefsel)onderzoek wordt besloten, zal in het algemeen een halve schildklier worden verwijderd (hemithyroïdectomie). Indien tot een dergelijke ‘diagnostische’ operatie wordt besloten, blijkt in ongeveer 30 procent van de gevallen daadwerkelijk sprake van een maligniteit. Dat betekent dat dus 70 procent van de patiënten geopereerd worden voor iets wat achteraf goedaardig blijkt te zijn. In geval van maligniteit zal dan doorgaans ook de andere helft van de schildklier operatief worden verwijderd. Bij kleine kwaadaardige afwijkingen (< 1 cm) wordt vaak volstaan met het verwijderen van slechts de halve schildklier, omdat de langetermijnprognose zeer goed is. Er gaan internationaal stemmen op om deze grens van 1 cm in de toekomst uit te breiden naar ook grote tumoren, zeker indien er verder geen andere uitingen zijn van een verhoogd risico.

Beïnvloeding van de diagnostiek
Diverse medicamenten kunnen de diagnostiek van schildklieraandoeningen bemoeilijken (tabel 3). Scintigrafie met jodium of technetium wordt vooral verstoord door jodiumhoudende medicamenten, zoals amiodaron en röntgencontrastmiddelen. In feite is de schildklier dan verzadigd met jodium en kan er geen radioactief jodium of technetium meer bij.
Er zijn ook omstandigheden waarbij afwijkende schildklierfunctietesten kunnen worden gevonden. Bij ernstige ziekte is gewoonlijk het T3 verlaagd, de FT4 kan verhoogd, normaal of verlaagd zijn en de TSH is normaal of verlaagd (ook wel non-thyroidal illness genoemd). Bij acute psychiatrische aandoeningen is de FT4 verhoogd of normaal, de TSH soms aan de lage kant, de T3-spiegel kan laag zijn.

Oorzaken van een verlaagd T3 staan vermeld in tabel 4.
Hypothyreoïdie
- Hypothyreoïdie betekent niets anders dan dat de schildklier niet voldoende functioneert. Afhankelijk van de vraag wat de oorzaak is van de hypothyreoïdie, kunnen we spreken van een:
- primaire hypothyreoïdie (de oorzaak is te vinden in de schildklier);
- secundaire hypothyreoïdie (de oorzaak ligt in de hypofyse = hersenaanhangselklier); of
- tertiaire hypothyreoïdie (de oorzaak is te vinden in de hogere hersenkernen die de hypofyse besturen = hypothalaam).
Secundaire en tertiaire hypothyreoïdie zijn zeer zeldzaam, evenals enkele andere oorzaken die niet goed in deze indeling zijn onder te brengen. Deze andere oorzaken zijn: farmacologisch (door medicamenten en dergelijke), jodiumtekort (komt in Nederland vrijwel niet voor dat het leidt tot hypothyreoïdie), overmaat jodide en perifere resistentie (ongevoeligheid) voor schildklierhormoon.
Oorzaken van hypothyreoïde
De belangrijkste oorzaken van hypothyreoïdie staan vermeld in tabel 5 en worden hierna besproken.

- De meest voorkomende oorzaak van hypothyreoïdie in Nederland is de ziekte van Hashimoto (thyreoïditis van Hashimoto), een auto-immuunaandoening waarbij het lichaam antistoffen maakt tegen de eigen lichaamscellen, in dit geval schildkliercellen. Deze antistoffen beschadigen de schildklier waardoor die op een bepaald moment niet meer in staat is om de normale hoeveelheid schildklierhormoon te maken. Zo ontstaat dan hypothyreoïdie. De antilichamen zijn in het bloed meetbaar (zie hoofdstuk 2) en ze zijn gericht tegen bestanddelen van de schildkliercel. De belangrijkste antilichamen zijn die tegen schildklierperoxidase (TPO) en thyreoglobuline (minder specifiek). Ook het CPK (creatinefosfokinase) kan verhoogd zijn als uiting van myopathie (spierzwakte). Al in hoofdstuk 2 is vermeld dat Hashimoto vaak voorkomt in combinatie met andere auto-immuunziekten.
- Het beloop van de ziekte is vaak (zeer) langzaam. In het begin kan er sprake zijn van een struma en soms kortdurend thyreotoxicose, dat wil zeggen hoge T4- en T3-waarden in het bloed. Deze hoge schildklierhormoonspiegels zijn voorbijgaand van aard. Zodra de schildkliercellen leeg zijn, zal de hypothyreoïdie zich ontwikkelen.
- Wereldwijd is jodiumtekort ook een oorzaak van hypothyreoïdie. Jodium is een belangrijk bestanddeel van de schildklierhormonen; thyroxine (T4) bevat vier en trijodothyronine (T3) drie jodiumatomen. Zonder jodium kan er geen T4 of T3 worden gemaakt in de schildklier of daarbuiten. In de westerse wereld, waar in het algemeen geen ernstig jodiumtekort meer bestaat, komt dit vrijwel niet meer voor.
- Een andere veel voorkomende oorzaak van hypothyreoïdie is de toestand na therapie voor de ziekte van Graves, wanneer patiënten worden behandeld met radioactief jodium of een operatie. Een te langzaam werkende schildklier kan direct na de behandeling voorkomen, maar ook pas na jaren sluipend ontstaan en dan dus meestal onverwacht.
- Oorzaken die minder frequent worden gezien, maar toch regelmatig voorkomen:
- (meestal tijdelijk) na een virale thyreoïditis (schildklierontsteking; zie hoofdstuk 6);
- als gevolg van jodiumhoudende medicamenten (hoestmiddelen, amiodarone, zeewierproducten) of röntgencontrastmiddelen, maar ook door lithium (gebruikt in de psychiatrie), bepaalde koolsoorten (Tasmanië) en zeewier (Japan) kan hypothyreoïdie optreden. Verder kan het ook voorkomen door een aangeboren afwijking in de fabricage van schildklierhormoon, zodat onvoldoende T4 en T3 worden gemaakt. Na een bevalling kan tijdelijk hypothyreoïdie optreden in het kader van een zogeheten postpartum thyreoïditis; soms kan de schildklierwerking verminderen als gevolg van een afwijking in de hypofyse (secundaire hypothyreoïdie). Het TSH-gehalte in het bloed is hierbij laag in verhouding tot het lage schildklierhormoon in het bloed en ook andere hypofysehormonen laten vaak een verlaagde bloedspiegel zien.
Klachten en verschijnselen bij hypothyreoïdie
De klachten die bij hypothyreoïdie voorkomen, zijn verschillend van aard en vaak zo algemeen dat ze niet altijd meteen worden herkend. Bij het stellen van de diagnose is dus niet zelden onduidelijk hoelang de aandoening al bestaat. En andersom, bij lichte vormen zijn er soms in het geheel geen klachten.
De klachten die het frequentst voorkomen, zijn toenemende vermoeidheid en kouwelijkheid. Ook geheugenverlies en spierzwakte komen vaak voor. Er kan kortademigheid optreden en pijn op de borst na inspanning of in de kou, wat kan wijzen op een vernauwing van de kransslagaderen (angina pectoris). Ook de bloedvaten in de benen kunnen vernauwd zijn, waardoor pijn ontstaat in de kuiten, die verdwijnt na stilstaan (claudicatio intermittens of ‘etalagebenen’).
De menstruatie kan heviger worden en langer duren, maar ook helemaal wegblijven. De vruchtbaarheid vermindert. Het gewicht kan toenemen, maar gewoonlijk niet meer dan enkele kilo’s. De huid wordt droog, koud en ruw.

Er kan zich vocht ophopen in het gezicht en rond de oogleden. Het uiterlijk wordt pafferig en de stem wordt hees en laag. Ook doofheid en een vertraagde stoelgang komen voor. Er kunnen krampen in de spieren of tintelingen van de handen optreden. Dit laatste komt door het carpaletunnelsyndroom. Bij dit syndroom zit er een zenuw klem in de pols. Die beklemming gaat gepaard met een stoornis van de gevoeligheid van de vingers die zich vooral uit in jeuk en kriebelingen (alsof er mieren lopen). Het komt ook voor bij andere aandoeningen en verdwijnt na behandeling. Bij lang bestaande, ernstige vormen kunnen ook psychische klachten voorkomen. Het vasthouden van vocht wordt veroorzaakt door ophoping van bepaalde eiwitten, de zogenaamde mucopolysacchariden (zie ook hierna).
Als de dokter je goed kent en je enige tijd niet heeft gezien, zal de diagnose snel duidelijk zijn. Meestal echter zijn de veranderingen zo langzaam gekomen dat ze niet zo erg opvallen.
De arts kan merken dat je er pafferig uitziet en dat je huid gelig is, wat wijst op myxoedeem. Deze aandoening is een indicatie van een ophoping van bepaalde stoffen in de huid en wordt gekenmerkt door een verlaagd basaal metabolisme en een wasachtige of deegachtige zwelling van de huid waarin geen putjes kunnen worden gedrukt (mucoïde infiltratie van de huid). De naam myxoedeem wordt ook gebruikt als synoniem van een (ernstige) hypothyreoïdie. De hartslag kan trager zijn, de bloeddruk wat hoger. De peesreflexen verlopen vertraagd. Vooral in het begin kan de schildklier opgezet zijn.
Diagnose stellen
Als gedacht wordt aan hypothyreoïdie, dan is de diagnose niet moeilijk te bevestigen of uit te sluiten via bloedonderzoek. Uit dat onderzoek zal dan blijken dat de TSH-concentratie is verhoogd (tenzij de oorzaak in hypofyse of hypothalamus is gelegen) en dat de FT4-spiegel laag is.
Indirecte tests, zoals cholesterol (aderverkalking!) en CPK (een spierenzym) kunnen verhoogde waarden laten zien. Ook het elektrocardiogram (de hartfilm) kan afwijkingen vertonen. De aanwezigheid van antistoffen tegen het schildklierperoxidase (TPO-antistoffen) past bij de ziekte van Hashimoto.
Behandeling
Op zich is de behandeling van hypothyreoïdie eenvoudig. De onvoldoende gevormde schildklierhormonen, waaronder in het bijzonder de thyroxine (T4), wordt vervangen door een tablet met synthetisch T4. Dit wordt levothyroxine genoemd, en is beschikbaar in verschillende merken (Eltroxin®, Euthyrox®, Levothyroxine®, Thyrax Duotab®, Thyrofix®, Tirosint®). Er zijn tabletten van verschillende sterkte van 0,025 tot 0,2 mg. Hiermee is de therapie gewoonlijk goed in te stellen.
Bij ouderen, mensen met angina pectoris en in het geval van zeer ernstige hypothyreoïdie wordt de dosering langzaam opgevoerd.
Zo wordt er bijvoorbeeld bij mensen op hoge leeftijd in het algemeen voorzichtig gestart met 0,025 tot 0,050 mg (= 25-50 µg) en wordt er opgehoogd per twee weken. Bij anderen, zeker als de hypothyreoïdie kort tevoren is ontstaan, kan meteen met een hogere dosis worden gestart, gewoonlijk met de volledige substitutiedosis.
De uiteindelijke dosis is meestal rond de 1,5- 1,7 µg /kg (dus bij iemand van rond de 50 kg meestal 75-87,5 µg) per dag, ’s morgens een halfuur voor het ontbijt in te nemen. Volgens recent onderzoek kan het ook vóór het slapen worden ingenomen. Waarschijnlijk is de opname dan zelfs beter. De behoefte aan schildklierhormoon kan met het stijgen van de leeftijd met 25 procent afnemen.
Men streeft bij deze behandeling in het algemeen naar een laag-normale TSH (0,5-1,0 mU/l), waarbij de FT4 vaak iets aan de hoge kant is. Hoewel dit in het algemeen de beste dosering is voor de meeste patiënten, geldt dit niet voor iedereen en voelen sommigen zich juist beter bij een hoger TSH en een lager FT4. Thyroxine werkt niet snel en het kan dus lang (soms zes tot negen maanden) duren voordat er merkbare veranderingen optreden.
Soms moet in het beloop (bijv. bij het ouder worden of bij veranderingen in gewicht) de dosering worden aangepast; daarom is het goed elk jaar of elke twee jaar het bloed te laten controleren.
Er is al jaren discussie over het al of niet bijgeven van trijodothyronine (T3) naast de thyroxine. Dit omdat de schildklier behalve T4 ook een kleine hoeveelheid T3 maakt. Het kan daarbij zo zijn dat bij bepaalde patiënten niet in alle organen de T4 even goed wordt omgezet in T3 en dat daardoor deze organen het effect van het waarschijnlijk belangrijkste werkzame schildklierhormoon (T3) moeten missen. Echter, alle studies die tot op heden gedaan zijn naar aanvullende therapie met T3 (cytomel) laten geen duidelijke verbetering zien ten opzichte van T4 alleen. Mogelijk komt dit doordat er nog geen T3-preparaten op de markt zijn met een vertraagde afgifte. T3-behandeling kan daardoor soms problemen opleveren door de perioden met verhoogd serum T3 en wordt dan ook niet standaard geadviseerd. Echter, in specifieke groepen patiënten met veel aanhoudende klachten ondanks een goede instelling kan een proefbehandeling met T3 worden overwogen. Indien dit geen duidelijke verbetering laat zien, moet dit weer gestaakt worden.
Na vele maanden (of jaren) kan verbetering van de klachten (met name de futloosheid en moeheid) optreden, zonder dat duidelijk is waarom. De beginbehandeling is gewoonlijk in handen van een huisarts of kinderarts. In specifieke gevallen kan een internist de behandeling tijdelijk overnemen van de huisarts tot de situatie stabiel is.
Bijzondere situaties
Als er sprake is van hypothyreoïdie, is het zaak de aandoening te onderscheiden van een aantal bijzondere situaties, zoals de subklinische hypothyreoïdie, het myxoedeem coma en de hypothyreoïdie bij kinderen en pasgeborenen.
Subklinische hypothyreoïdie
Als het TSH-gehalte licht verhoogd is en de vrije T4- en T3-spiegels normaal zijn, wordt gesproken over subklinische hypothyreoïdie. De toevoeging ‘subklinisch’ is eigenlijk onjuist, want patiënten met subklinische hypo- of hyperthyreoïdie kunnen wel degelijk klachten hebben. De prevalentie is 5-8 procent en neemt toe bij stijgende leeftijd, bij vrouwen ouder dan zestig jaar wordt in sommige studies zelfs gesproken van 20 procent. Hoewel in een aantal studies een verband wordt gevonden tussen subklinische hypothyreoïdie en hart- en vaatziekten, is het op dit moment onduidelijk of behandeling van subklinische hypothyreoïdie nuttig is, omdat er geen grote onderzoeken zijn gedaan naar de effecten van behandeling op hart- en vaatziekten en op de kans om te overlijden. Bij subklinische hypothyreoïdie kunnen al – meestal niet ernstige en aspecifieke – klachten bestaan, zoals moeheid en gewichtstoename. Ook het geheugen en de concentratie kunnen verminderen. Een recent klinisch onderzoek naar de behandeling van zeer milde subklinische hypothyreoïdie liet geen verbetering zien van de kwaliteit van leven.
Myxoedeem coma
Bij zeer ernstige hypothyreoïdie kunnen patiënten bewusteloos raken. Dit verschijnsel heet myxoedeem coma. Het is een ernstige aandoening die tot de dood kan leiden als niet vlot tot opname in het ziekenhuis wordt besloten. Behandeling zal dan meestal plaatsvinden op een intensive-careafdeling, vooral in verband met de slechte toestand van het hart.
Hypothyreoïdie bij kinderen en pasgeborenen
Bij jonge kinderen is de oorzaak van de hypothyreoïdie een gebrekkige ontwikkeling of afdaling van de schildklier, of van de ziekte van Hashimoto. Minder vaak is een aangeboren fout in de aanmaak van T4 en T3 (dyshormonogenese) de oorzaak van de aandoening. De opvallendste verschijnselen zijn een achterblijvende groei en een uitblijvende puberteit.
De diagnose wordt met hetzelfde bloedonderzoek gesteld als bij volwassenen, soms aangevuld met handfoto’s om de botleeftijd te bepalen (deze loopt achter) en een schildklierscan en/of -echo, die kunnen laten zien of de schildklier klein is of onvoldoende is afgedaald.
Bij pasgeborenen kan het niet-ontdekken van hypothyreoïdie ernstige gevolgen hebben. Onbehandeld kan dit namelijk leiden tot een permanente mentale retardatie. In verband daarmee wordt bij iedere pasgeborene via de hielprik gecontroleerd of er sprake is van een adequate schildlierfunctie. Indien vroeg behandeld, zal het kind een volledig normale ontwikkeling hebben.
Ernstige mentale retardatie kan ook voorkomen in die delen van de wereld waar er ernstig jodiumtekort is. In dat geval spreken we van cretinisme.
Ook bij baby’s wordt de hypothyreoïdie zonder bloedonderzoek niet altijd vlot herkend. De ontwikkeling blijft achter en vaak is er een bolle buik met een uitpuilende navel. Het uiterlijk is opgeblazen en er kunnen dezelfde verschijnselen zijn als bij volwassenen. Bij twijfel wordt behandeling met thyroxine geadviseerd, eventueel (tijdelijk) te staken op de leeftijd van één jaar. Vanwege het belang van schildklierhormoon voor de hersenontwikkeling, wil je niet het risico lopen dat je dit mist.
Hyperthyreoïdie
Hyperthyreoïdie houdt in dat de schildklier te hard werkt; daarbij zijn de concentraties van de schildklierhormonen T4 en T3 in het bloed verhoogd en daardoor is op zijn beurt het TSH verlaagd. Thyreotoxicose is een nog algemenere term die niet alleen hyperthyreoïdie, maar ook andere toestanden omvat, waarbij er een teveel aan schildklierhormoon circuleert. Daarbij hoeft de schildklier niet per se te hard te werken. In de praktijk worden deze twee termen door elkaar heen gebruikt, en wordt dit onderscheid dus lang niet altijd gemaakt. Bij een thyreoïditis (schildklierontsteking) gaan er schildkliercellen kapot, waardoor er tijdelijk te veel T4 en T3 uit deze cellen in het bloed lekt. De schildklier werkt daarbij dus zeker niet te hard en dat is ook zo als er te hoge T4- en/of T3-waarden zijn door de inname van te veel schildklierhormoon (al of niet bedoeld). Bij thyreotoxicose door inname van extra schildklierhormoon is het thyreoglobulinegehalte in het bloed onmeetbaar laag. Bij de meeste schildklieraandoeningen (inclusief hyperthyreoïdie) is het juist verhoogd.
Oorzaken van hyperthyreoïdie
De meest voorkomende oorzaken van hyperthyreoïdie zijn de ziekte van Graves en het toxisch (multi)nodulaire struma. Omdat deze zo belangrijk en ook verschillend zijn, worden ze hierna apart besproken. Hyperthyreoïdie kan verder veroorzaakt worden door toediening van jodium (als de schildklier vergroot is en de hormoonproductie aan de hoge kant is), een struma ovarii (abnormaal gelokaliseerd schildklierweefsel in een eierstok) of een mola-zwangerschap (een zwangerschap waarbij het embryo misvormd is) c.q. choriocarcinoom. Deze laatste twee oorzaken zijn zeer zeldzaam. Ook een overmaat van TSH, zoals bij een hypofyseproces, en een schildkliercarcinoom kunnen in zeer zeldzame gevallen tot hyperthyreoïdie leiden.
Wat vaker kan een thyreotoxicose optreden (dus geen hyperthyreoïdie, want de schildklier werkt niet te hard). Dit gebeurt onder meer in de eerste fase van een thyreoïditis (zie hoofdstuk 6) en door overmatige toediening van schildklierhormoon (door arts voorgeschreven of thyreotoxicosis factitia = door zelftoediening).
De oorzaken staan opgesomd in tabel 7.

Klachten en verschijnselen bij hyperthyreoïdie
De klachten en verschijnselen bij hyperthyreoïdie zijn in het algemeen veel duidelijker bij de ziekte van Graves dan bij een (multi)nodulaire struma.
De meest voorkomende klachten zijn: hartkloppingen, vermoeidheid, kortademigheid bij inspanning, last van de warmte, overmatig transpireren, nervositeit en gewichtsverlies.
Een struma komt vaak voor, de handen zijn warm en vochtig en er is een snelle, maar meestal regelmatige pols. Er kunnen tremoren zijn, oog- en, minder vaak, huidverschijnselen. Patiënten zijn soms zeer beweeglijk en kunnen diarree hebben. De huidverschijnselen komen vooral voor bij de ziekte van Graves en zijn te omschrijven als myxoedeem (meestal al of niet onregelmatige verdikking van de onderbenen = pretibiaal) en in zeldzamer gevallen als zwelling van vingers en tenen. De huid is vaak kwetsbaar en vochtig. Overigens moet het pretibiaal myxoedeem niet worden verward met het meer algemeen optreden van myxoedeem of huidverdikking die voorkomt bij ernstige hypothyreoïdie (zie tabel 8).
Hiernaast kan vitiligo optreden, die ook kan voorkomen bij andere auto-immuunaandoeningen. Vitiligo is een huidaandoening die gekenmerkt wordt door ronde, witte vlekken met daarop kleurloze haren, begrensd door een donkere rand.

Ziekte van Graves
Bij de ziekte van Graves is er sprake van een auto-immuunziekte, waarbij het lichaam (vooral stimulerende) antistoffen maakt tegen de TSH-receptor (TsAb/TSI). Daardoor raakt de schildklier diffuus vergroot en ontstaat er overactiviteit, waardoor te veel T4 en T3 in het bloed worden uitgescheiden. Het diffuse patroon van overactiviteit is goed zichtbaar als je een schildklierscintigram maakt.
Zoals bij de meeste schildklieraandoeningen wordt de ziekte van Graves meer bij vrouwen dan bij mannen gezien en is er een zekere familiaire aanleg. Soms begint de ziekte na een emotionele gebeurtenis. Bij rokers komt het vaker voor, en dit geldt nog sterker voor de oogverschijnselen.
De klachten die optreden bij hyperthyreoïdie zijn bij de ziekte van Graves in het algemeen redelijk uitgesproken aanwezig (figuur 7).
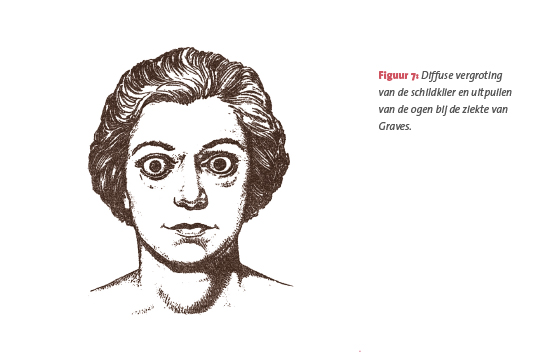
Oogverschijnselen bij ziekte van Graves
De oogverschijnselen die bij de ziekte van Graves optreden, worden waarschijnlijk veroorzaakt door een auto-immuunreactie die gericht is tegen de bindweefselcellen in de oogspieren en het oogvet achter de ogen. Hoewel de oogverschijnselen parallel lopen aan de klinische verschijnselen van de hyperthyreoïdie, is dit in lang niet alle gevallen zo. Er spelen daarom ook andere factoren een rol dan de antilichamen alleen.
Omdat de oogverschijnselen (figuur 7) soms tot grote problemen kunnen leiden, is een gezamenlijk spreekuur van internist-endocrinoloog en oogarts voor deze patiënten aan te bevelen. De opvallendste oogverschijnselen zijn de volgende.
- De ogen kunnen naar voren uitpuilen, waardoor de patiënt lijkt te staren. Dit wordt exophthalmus of proptosis genoemd. Je kunt de uitbolling simpel meten met een Hertel-meter.
- De oogleden kunnen opzwellen door verhoogde druk en verminderde vochtafvoer (‘wallen onder de ogen’).
- De ogen kunnen branderig zijn en gemakkelijker tranen, omdat ze minder beschermd zijn. De ogen kunnen extra vochtig zijn, rood doorlopen en soms sluiten ze slecht.
- Omdat de oogspieren ook zijn aangedaan, kan het zijn dat de oogbewegingen niet meer goed verlopen en kan er dubbelzien ontstaan. Bij het bewegen van de ogen is vaak goed zichtbaar dat één oog achterblijft.
- Door de verhoogde oogdruk kan de oogzenuw worden beschadigd waardoor uiteindelijk het gezichtsvermogen kan worden bedreigd.
Hyperthyreoot (multi)nodulair struma
Een hyperthyreoot (multi)nodulair struma wordt ook wel de ziekte van Plummer genoemd. Deze aandoening komt vooral bij oudere mensen voor die al jarenlang een knobbelig (nodulair) struma hebben (zie figuur 8). Het komt vaak in de familie voor, maar de klachten zijn gewoonlijk veel minder opvallend dan bij de ziekte van Graves; het ontstaan is dus meestal sluipend.
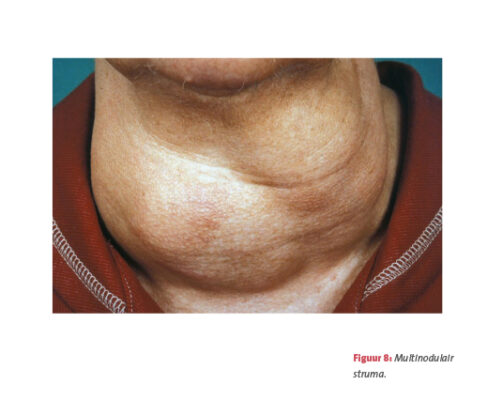
De meest voorkomende verschijnselen zijn een snelle polsfrequentie en struma. In de knobbels bevinden zich gebiedjes die zich aan de normale regulatie van de productie van schildklierhormoon (aangestuurd door de hersenaanhangselklier, hypofyse) onttrekken. Indien dit autonoom doorgaat, wordt uiteindelijk te veel schildklierhormoon gefabriceerd. De schildklierscan laat een vlekkerig beeld zien met afwisselend weinig en veel opname van het radio-isotoop (zie figuur 1). Als slechts één enkele (hyper)actieve knobbel wordt gezien, dan noemt men dit een toxische nodus (of toxisch adenoom).
Diagnose stellen
Om een hyperthyreoïdie vast te stellen, begint men met het bepalen van TSH in het bloed. Als deze laag is, wordt ook FT4 en zo nodig (als de FT4 normaal is) T3 bepaald. FT4 en T3 zijn gewoonlijk te hoog. Als alleen de T3-concentratie hoog is, spreekt men van een T3-toxicose. De klinische verschijnselen daarbij zijn niet anders dan bij een volledig ontwikkelde hyperthyreoïdie; het treedt op bij ongeveer 15 procent van de hyperthyreoïdiepatiënten.
Uiteraard zijn hierbij de symptomen en verschijnselen de leidraad en soms – zoals bij de ziekte van Graves – kunnen begeleidende fenomenen, zoals de kenmerkende oogverschijnselen, richting geven. Aanvullend bloedonderzoek in de zin van het bepalen van TSH-receptor stimulerende antilichamen kan wijzen op de ziekte van Graves. Deze kunnen echter ook voorkomen bij de ziekte van Hashimoto (zie hoofdstuk 2).
Bij twijfel kan een schildklierscintigram de ziekte van Graves bevestigen of een toxisch multinodulair struma of een toxisch adenoom aantonen. Bij zelftoediening van schildklierhormoon (thyreotoxicosis factitia) is er geen opname van radio-isotoop. Bovendien is daarbij het thyreoglobulinegehalte in het bloed onmeetbaar laag. De diagnostiek bij door jodium geïnduceerde thyreotoxicose is niet altijd gemakkelijk, meestal is de opname van radioactief jodium laag, maar zeker niet altijd (zoals na amiodaronetherapie).

Behandeling
De aanvangsbehandeling voor de meest voorkomende oorzaken van hyperthyreoïdie is dezelfde. Gewoonlijk wordt gestart met schildklierremmende medicijnen, meestal thiamazol c.q. methimazol (strumazol). Een alternatief is propylthiouracil (PTU), maar omdat dit gepaard kan gaan met ernstige leverproblemen is dit middel niet de eerste keuze. Zodra patiënten een normale schildklierfunctie hebben, afgemeten aan de verschijnselen en het bloedonderzoek, wordt schildklierhormoon toegevoegd aan de medicatie om de geremde schildklier te vervangen. Dit wordt ook wel ‘block & replace’-therapie genoemd.
Bij de ziekte van Graves wordt één à anderhalf jaar met deze combinatietherapie behandeld, waarna de ziekte bij minder dan de helft van de gevallen is genezen. Dit komt doordat bij een deel van de Graves-patiënten de ziekte mild verloopt en kortdurend is. In feite wordt deze periode met de medicamenteuze therapie overbrugd. Bij een toxisch (multi)nodulair struma is zo’n remissie niet te verwachten. Bij een terugkeer van de ziekte van Graves en bij een toxisch (multi)nodulair struma wordt combinatietherapie daarom meestal slechts gegeven om de schildklier tot rust te brengen, waarna definitieve therapie volgt. Dit kan zijn in de vorm van radioactief jodium (meestal) of operatie (in geselecteerde gevallen).
De medicijnen worden in het algemeen goed verdragen, maar soms kunnen de schildklierremmende middelen huidverschijnselen veroorzaken. Die gaan overigens weer over. Als iemand tijdens de behandeling keelpijn met koorts krijgt, is bloedonderzoek aangewezen omdat de witte bloedlichaampjes (maar ook de bloedplaatjes en de rode bloedlichaampjes) in hun aanmaak kunnen worden geremd. Dit is een mogelijk zeer gevaarlijke situatie, het komt gelukkig niet vaak voor.
Als er sprake is van oogverschijnselen bij de ziekte van Graves, dan is nog meer dan anders een stabiele instelling van de schildklier gewenst. Bij een slecht geregelde schildklierfunctie kunnen de oogverschijnselen in ernst toenemen.
Een door jodium veroorzaakte thyreotoxicose is in het geval van amiodarone vaak moeilijker te behandelen; hiervoor is specialistische expertise vereist. Een probleem is daarbij dat het eenmaal gegeven jodium in amiodarone lang in het lichaam blijft en het probleem niet snel is opgelost na het staken ervan. Röntgencontrastmiddelen bevatten tegenwoordig veel minder jodium dan vroeger. In deze gevallen is een thyreotoxicose vaak mild en voorbijgaand van aard.
Bij een al of niet opzettelijk ingenomen teveel aan schildklierhormoon kan dit uiteraard worden gestaakt, waarna na ongeveer zes tot acht weken een nieuw evenwicht ontstaat en de overmaat meestal is verdwenen.
De therapie van (zeer) zeldzame oorzaken van thyreotoxicose wordt hier verder niet besproken.
Radioactief jodium
Zoals eerder vermeld, is bij een terugkeer (recidief) van de ziekte van Graves en bij nodulair struma in het algemeen definitieve therapie noodzakelijk. Tegenwoordig wordt hiervoor voornamelijk radioactief jodium gebruikt, omdat het goed werkt, gemakkelijk beschikbaar is en niet al te duur is. Het wordt al heel lang toegepast en wordt in de vorm van een capsule of als vloeistof gegeven. Gedurende korte tijd (een à twee dagen) is isolatie nodig vanwege onder andere de afvoer van urine en ontlasting. In geval van een lage dosis is poliklinische behandeling, met inachtneming van enkele leefregels, mogelijk.
Voordat therapie met radioactief jodium kan plaatsvinden, moeten thyroxine (schildklierhormoon) vier weken en de schildklierremmende medicijnen vijf dagen onderbroken worden. De therapie helpt niet direct, er kunnen drie tot zes maanden voor nodig zijn. Daarom wordt de tablettherapie vijf dagen na de radio-actiefjodiumtherapie vaak gedurende die tijd hervat. Strumazol heeft hierbij de voorkeur boven PTU vanwege de eerdergenoemde, maar gelukkig zeldzame leverproblemen die gezien kunnen worden bij PTU.
Als er oogverschijnselen zijn bij de ziekte van Graves, kan het soms nodig zijn therapie met bijnierschorshormoon (prednison) toe te voegen om een verergering ervan te voorkomen. Tegenwoordig wordt vaak een kuur via het infuus toegediend (methylprednisolon). Dit gebeurt gedurende twaalf weken eenmaal per week. Dit werkt beter dan prednison in tabletvorm en heeft minder bijwerkingen.
Er zijn weinig complicaties als gevolg van radioactiefjodiumtherapie op de lange termijn. Wel is het zo dat patiënten een verhoogd risico hebben op het ontwikkelen van de oogsymptomen. Om die reden wordt patiënten met een verhoogd risico op de oogziekte soms een preventieve kuur met prednison voorgeschreven rondom de behandeling. In de meeste gevallen is dit echter niet nodig. Als er te weinig radioactief jodium is gegeven, kan een herhaalde dosis nodig zijn en kan op de lange duur een hypothyreoïdie ontstaan. Dit is echter min of meer inherent aan de (moeilijk met precisie te doseren) therapie.
Jaarlijkse controle van het bloed (TSH) is daarom wel aangewezen. Dit geldt echter evenzeer voor de andere vormen van therapie (operatie of medicamenten).
Operatieve behandeling als alternatief voor de therapie met radioactief jodium vindt soms plaats bij vrouwen met kinderwens en in geval van een groot struma. Complicaties van een operatie treden weinig frequent op en omvatten met name bijschildklierfalen ten gevolge van schade aan de kleine, dicht bij de schildklier gelegen bijschildklieren (er zijn er meestal vier) en heesheid. De heesheid wordt veroorzaakt door verlamming van een stemband, wat weer het gevolg is van een beschadigde zenuw, die ook vlak naast de schildklier loopt.
Rest nog te vermelden dat in geval van heftige klachten (vooral hartkloppingen) bètablokkerende middelen kunnen worden gegeven totdat de schildklierremmende medicijnen volledig werken. Deze geven vaak verlichting van de klachten. Voor de oogverschijnselen bij de ziekte van Graves is niet altijd een aparte behandeling nodig. Vaak zijn een zonnebril en methylcellulose (kunsttranen) al voldoende.
Soms is echter de eerder genoemde therapie met bijnierschorshormoon (prednison) nodig bij ernstige oogverschijnselen om de ontsteking tot rust te brengen. Bij blijvende problemen zijn soms aanvullende therapieën nodig (bijvoorbeeld bestraling) en kan het in een later stadium nodig zijn operatief in te grijpen. Deze operaties worden gewoonlijk door de oogarts verricht (vooral bij dubbelzien of ernstig uitpuilen).
Subklinische hyperthyreoïdie
Onder subklinische hyperthyreoïdie wordt verstaan die toestand waarbij het TSH-gehalte in het bloed onderdrukt is, maar de FT4- en T3-concentraties (nog) normaal zijn. Vroeger werd dit opgevat als een autonoom functionerende schildklier met een normale functie, waarbij alleen controle nodig was. Met het sterk verbeteren van laboratoriumbepalingen, gaan we er tegenwoordig vanuit dat de bij deze personen gevonden ‘normale’ FT4- en T3-waarden voor hen waarschijnlijk toch hoger zijn dan voor hen gebruikelijk is. Daarbij kunnen er al hyperthyreoïdieklachten bestaan, zoals een verhoogde polsfrequentie, boezemfibrilleren en botontkalking (dit laatste met name na de overgang).
Eerder dan voorheen zal daarom tegenwoordig worden overgegaan tot behandeling, zeker als er hartritmestoornissen bestaan of als er een groot risico is op botontkalking zoals bij vrouwen na de overgang.
Thyreotoxische crisis
Met een thyreotoxische crisis wordt een bijzonder ernstige en gelukkig zeer zeldzame toestand bedoeld, waarbij de verschijnselen van de hyperthyreoïdie zeer heftig zijn. Daarbij treden met name koorts, hartkloppingen (excessief), misselijkheid en braken, diarree, hartfalen en in ernstige gevallen geelzucht op. Patiënten kunnen in coma raken en behandeling op een IC-unit is nodig. De behandeling is moeilijker dan bij een ‘gewone’ hyperthyreoïdie en de sterfte is hoog.
Hyperthyreoïdie bij kinderen
Bij kinderen treedt hyperthyreoïdie gelukkig zelden op. Bij pasgeborenen kan het voorbijgaand optreden als er in het bloed van de moeder schildklierstimulerende antilichamen circuleren.
In het algemeen is therapie met schildklierremmende medicijnen aangewezen, die echter wel langer wordt voortgezet dan bij volwassenen, om de definitieve therapie met radioactief jodium of operatie nog uit te stellen. De definitieve behandeling kan dan zo nodig rond het achttiende jaar worden gegeven.
Struma
Als er over struma of krop wordt gesproken, wordt niets anders bedoeld dan een zichtbare of voelbare vergroting van de schildklier. Deze vergroting kan egaal (diffuus) of knobbelig (nodulair) zijn. Als er één knobbel wordt gevoeld, spreekt men van (uni)nodulair, zijn er meer knobbels dan noemen we dit multinodulair.
Een probleem daarbij kan zijn dat het voelen in de hals niet altijd gemakkelijk is en per onderzoeker kan verschillen. Daarom is afbeeldend onderzoek soms nodig.
Om een struma volledig te karakteriseren, is het nodig na te gaan wat de anatomie van de struma is, maar ook wat de functie en de oorzaak zijn. Euthyreoot noem je een struma waarvan de functie normaal is.
Daarnaast wordt over endemisch struma gesproken als het bij meer dan 10 procent van de bevolking voorkomt. Een en ander staat opgesomd in tabel 10.

Ongeveer 8 procent van de volwassenen heeft een voelbare knobbel in de schildklier en bij echografie van de schildklier blijkt zelfs 25-40 procent van de volwassenen een of meer knobbels in de schildklier te hebben. Verreweg het grootste deel van de schildkliernodi is goedaardig.
Het onderscheid tussen diffuus en multinodulair struma kan te maken hebben met de sterkte van de prikkel, die de oorzaak van de struma is. Een kortdurende sterke prikkel (bijvoorbeeld puberteit, zwangerschap in combinatie met jodiumgebrek, de ziekte van Graves) kan leiden tot het ontstaan van een euthyreoot diffuus struma. Een langdurige zwakke prikkel (bijvoorbeeld jodiumtekort, strumagene stoffen zoals thiocyanaat, schildklierremmende middelen en lithium) daarentegen leiden vaker tot een multinodulair struma. Een minder vaak voorkomende oorzaak is dyshormonogenese, oftewel een partieel enzymdefect. Hiermee wordt bedoeld dat er een stoornis is opgetreden in de fabricage van schildklierhormonen. Dit komt doordat het eiwit (enzym) dat de biochemische processen bevordert die nodig zijn voor deze fabricage, gedeeltelijk ontbreekt.
Een diffuus struma kan voorbijgaand zijn, maar kan op de lange duur ook overgaan in een nodulair struma en uiteindelijk hyperthyreoot worden.
De verschillen tussen Graves’ struma (diffuus) en nodulair struma staan vermeld in tabel 11.

In Nederland komt bij 18 procent van de gezonde mensen een knobbel zonder symptomen voor.
Informatie en onderzoek
Belangrijk is te weten hoelang de struma al bestaat, of deze groeit of pijnlijk is en of struma in de familie veel voorkomt. Gelet wordt op klachten die bij een hypo- of hyperthyreoïdie kunnen passen of bij een groot of laaggelegen (achter het borstbeen = retrosternaal) struma en of er klachten zijn van ademhalingsbelemmering.
Soms kan behalve van verdringing – wat vaak voorkomt – ook sprake zijn van vernauwing van de luchtpijp en daar heb je last van.
Bij het lichamelijk onderzoek wordt vooral aandacht geschonken aan de consistentie van de struma. Is die diffuus of nodulair, hard, vast of week, is de struma beweeglijk en is er pijn? Daarnaast wordt natuurlijk weer gelet op symptomen van hypo- of hyperthyreoïdie (zie de beide gelijknamige hoofdstukken).
Het onderscheid tussen een multinodulair (verscheidene knobbels) en een uninodulair (één voelbare knobbel) struma is kunstmatig. Beide vormen kunnen na elkaar voorkomen en soms blijkt een uninodulair struma bij verder onderzoek multinodulair te zijn. Beide vormen worden in feite tot hetzelfde ziektebeeld gerekend.
De oorzaak van een euthyreoot struma is vaak niet te achterhalen, simpeler is het om de functie vast te leggen. Dat kan via een bloedbepaling, de TSH-spiegel, zo nodig aangevuld met bepaling van het vrije T4 en T3.
Als bij het lichamelijke onderzoek niet duidelijk is of er een of meer knobbels (noduli) zijn, is een echografisch onderzoek het beste hulpmiddel om dit vast te stellen. De grootte van de knobbels is het best te meten met behulp van echografie. Ook kan echografie informatie geven over bepaalde ‘verdachte’ kenmerken die zouden kunnen wijzen op een maligniteit. Ook wordt echografie gebruikt bij een eventuele cytologische punctie. De functie van de schildklier en met name de functie van de daarin voelbare knobbels kan weer het beste worden nagegaan met scintigrafie (naast het bloedonderzoek). Indien er sprake is van een normaal bloedonderzoek, wordt scintigrafie in het algemeen achterwege gelaten.
Nadeel van de echografie is dat er vaak ook allerlei andere knobbeltjes worden gevonden (incidentalomen), die niet van belang zijn, maar die wel kunnen leiden tot extra aanvullende onderzoeken.
Oorzaken van struma
Wereldwijd is jodiumgebrek de belangrijkste oorzaak van struma en als dit zeer ernstig is, ontstaat ook hypothyreoïdie. Er zijn echter veel meer oorzaken, waaronder de strumagene (struma veroorzakende) stoffen, fabricagefoutjes in de schildklierhormoonsynthese (deze zijn zeer moeilijk aan te tonen), thyreoïditis, adenoom en carcinoom en het dysplastisch (abnormaal ontwikkeld) struma (tabel 12).


Dysplastisch struma wordt ook wel niet-toxisch of euthyreoot multinodulair struma genoemd. In de klassieke vorm ontstaat het langzaam over vele jaren, komt het in de familie voor en geeft het geen aanleiding tot klachten. De oorzaken ervan zijn waarschijnlijk divers en kunnen bijna alle genoemde problemen zijn, zoals vermeld in tabel 12.
Natuurlijk beloop
De sporadisch voorkomende, niet-toxische (euthyreote) struma wordt gekenmerkt door een geleidelijke toename van de grootte en de mogelijkheid van het ontwikkelen van een hyperthyreoïdie. In een diffuus struma kunnen op den duur noduli ontstaan die zich onttrekken aan de normale regulatie en dus autonoom worden. Deze autonome noduli kunnen op den duur te veel T3 en later ook T4 produceren, waardoor hyperthyreoïdie ontstaat. Dit gaat vaak sluipend en betrekkelijk ongemerkt. Een enkele keer kan ook bijvoorbeeld ten gevolge van een bloeding of door weefselversterf een teruggang van (hyper)functie plaatshebben.
Grote problemen zijn in het natuurlijke beloop dus meestal niet te verwachten.
Complicaties
Zoals eerder vermeld, kan hyperthyreoïdie ontstaan in een lang bestaand euthyreoot (meestal nodulair) struma. Dit is ook meteen de meest voorkomende complicatie. Mechanische complicaties (problemen door druk op de omgeving, met name de luchtpijp) en kanker (carcinoom) komen niet zo vaak voor. De sterfte van strumapatiënten is na twintig jaar niet anders dan die van personen zonder struma.
Behandeling
Meestal is behandeling niet nodig en kan worden volstaan met het vervolgen in de tijd. Jaarlijkse controle van de TSH-concentratie in het bloed is voldoende.
Redenen om te behandelen kunnen zijn: mechanische bezwaren, angst voor een kwaadaardige afwijking in de schildklier en minder vaak cosmetische klachten. Operatieve verwijdering van een struma is effectief, maar kan gepaard gaan met complicaties die gelukkig niet vaak voorkomen. Zo kunnen per ongeluk de bijschildklieren beschadigd raken tijdens de operatie, wat resulteert in een laag calciumgehalte in het bloed. Dit moet behandeld worden met tabletten (calcium en actief vitamine D). Ook kan een te groot deel van de schildklier weggenomen zijn, waardoor hypothyreoïdie optreedt. Een andere vervelende complicatie die niet vaak wordt gezien, is heesheid of een stemverandering ten gevolge van beschadiging van de zenuwen die de stembanden verzorgen en die vlak naast de schildklier lopen. Logopedische behandeling is dan aangewezen.
Behandeling met schildklierhormoon (thyroxine) wordt – in ieder geval in Nederland – zelden meer toegepast voor de behandeling van een struma omdat het weinig effectief is.
Behandeling van struma met radioactief jodium wordt ook vaak toegepast, omdat het eenvoudig is en in hoge dosis ook effectief. Verkleining van een struma treedt op tot 50 procent, maar het duurt wel een à twee jaar voor dit effect wordt bereikt. Ze wordt vooral toegepast bij ouderen met een groot struma; als er sprake is van een forse vernauwing van de luchtpijp, moet wel prednison gegeven worden om een tijdelijke extra zwelling door bestralingsontsteking te voorkomen. Hypothyreoïdie kan ook na jaren nog optreden als radioactief jodium is gegeven.
Als er sprake is van één enkele nodus die mechanische klachten geeft, kan een injectie met alcohol of behandeling met radiofrequente ablatie (RFA, waarbij de nodus als het ware wordt weggebrand) worden overwogen. Met beide therapieën zal de nodus in het algemeen verschrompelen.
Speciale problemen
Solitaire (enkele) nodus
Als er slechts één nodus is of als er een nodus duidelijk uitspringt in een meerknobbelig (multinodulair) struma is de verdenking op kwaadaardigheid iets groter. Specifieke kenmerken van echografie staan vermeld in hoofdstuk 2.
Bedacht moet worden dat ook dan verreweg de meeste knobbels goedaardig zijn. De mogelijke oorzaken staan vermeld in tabel 13.

Een cytologische punctie is echter wel aangewezen, en in geval van twijfel kan een operatie noodzakelijk zijn. Bij twijfel kunnen moleculaire merkers soms behulpzaam zijn. Zie verder ook hoofdstuk 7.
Jodiumaanbod/-besmetting
Patiënten met een struma kunnen een hyperthyreoïdie krijgen als ze grote hoeveelheden jodium krijgen zoals in röntgen-/contrastvloeistof of amiodaron. Vooral als er van tevoren sprake is van een jodiumgebrek, is dit risico groot. Met name deze oorzaak van hyperthyreoïdie bij amiodarongebruik is soms moeilijk te behandelen. Soms is het dan nodig de schildklier te verwijderen.
Luchtpijpvernauwing en retrosternaal struma
Vernauwing van de luchtpijp komt waarschijnlijk vaak voor, alhoewel er weinig onderzoek naar is gedaan. De luchtpijp is daarbij soms vernauwd en veel vaker nog wordt deze door de struma opzij geduwd. De ernst van de vernauwing kan gemeten worden via het longfunctieonderzoek, met name de inademing is dan belemmerd. Zo nodig kan dit met radioactief jodium worden behandeld. Retrosternaal (achter het borstbeen gelegen) struma komt ook voor en is operatief moeilijker te behandelen. Dit gebeurt daarom meestal met radioactief jodium, maar als dit niet goed mogelijk is of geen effect heeft ook wel via een operatie.
Speciale problemen
- De solitaire (enkele) nodus
- Als er slechts één nodus is of als er een nodus duidelijk uitspringt in een meerknobbelig (multinodulair struma) is de verdenking op kwaadaardigheid groter, zeker als de nodus geen jodium opneemt (koud is op de scan) en solide (met weefsel gevuld op de echo).
- Bedacht moet worden dat ook dan verreweg de meeste knobbels goedaardig zijn. De mogelijke oorzaken staan vermeld in onderstaande tabel.
- Een cytologische punctie en bij twijfel operatie is wel aangewezen. Zie verder ook Schildklierkanker .
- Jodium aanbod/besmetting

Patiënten met een struma kunnen een hyperthyreoïdie krijgen als ze grote hoeveelheden jodium krijgen zoals in röntgen/contrastvloeistof of amiodaron. Vooral als er van tevoren sprake is van een jodiumgebrek, is dit risico groot. Omdat deze vorm van hyperthyreoïdie moeilijk te behandelen is, is vaak profylactische therapie nodig. Het komt niet vaak voor.
Luchtpijpvernauwing en retrosternaal struma
Vernauwing van de luchtpijp komt waarschijnlijk vaak voor, alhoewel er weinig onderzoek naar is gedaan. De ernst ervan kan gemeten worden via het longfunctie-onderzoek, met name de inademing is dan belemmerd. Zonodig kan met radioactief jodium worden behandeld. Retrosternaal (achter het borstbeen gelegen) struma komt ook van tijd tot tijd voor en zal, omdat het moeilijker te controleren is, wat sneller worden behandeld. Dit gebeurt meestal met radioactief jodium, maar ook wel via een operatie. De luchtpijp is daarbij soms vernauwd en veel vaker nog wordt deze door de struma opzij geduwd.
Thyreoïditis
Een thyreoïditis is een schildklierontsteking. In de meeste gevallen is een virus daarvan de oorzaak. Wat voor klachten geeft dat de patiënt? En moet hij ervoor worden behandeld? In dit hoofdstuk wordt daar nader op ingegaan.
Er zijn verschillende vormen van thyreoïditis. De subacute of virale thyreoïditis is de meest voorkomende en is genoemd naar de Zwitserse chirurg De Quervain, die het ziektebeeld voor het eerst beschreef. Minder voorkomende vormen van thyreoïditis worden aan het eind van dit hoofdstuk kort beschreven.
Subacute virale thyreoïditis komt vrij vaak voor, soms in een dusdanig milde vorm dat het niet wordt herkend en voor griep wordt aangezien. Omdat het vrijwel altijd vanzelf geneest, is het niet erg als het niet wordt herkend.
De aandoening komt meer bij vrouwen dan bij mannen voor, vooral als er al een kleine struma bestaat. Waarschijnlijk zijn diverse virussen de veroorzaker, maar gewoonlijk wordt hier niet naar gezocht omdat dit geen consequenties heeft.
Klachten en verschijnselen
We hebben al eerder aangegeven dat het ziektebeeld bij een virale thyreoïditis sterk kan wisselen in ernst. Gewoonlijk begint het met een griepachtig beeld met moeheid, hoofdpijn, spierpijn en lichte temperatuurverhoging. Na enkele dagen wordt de schildklier groter, vaster en pijnlijk, in het bijzonder bij druk. Er ontstaan zowel slikklachten als stekende pijn die door kan trekken tot in de oren. Omdat bij een schildklierontsteking de cellen kapot gaan, lekt er schildklierhormoon in het bloed waardoor thyreotoxische klachten kunnen ontstaan (zoals bij hyperthyreoïdie).
Diagnose stellen
De klachten en symptomen zoals hiervoor beschreven, hoe aspecifiek ook, moeten – vooral als de schildklier pijnlijk vergroot is – doen denken aan een subacute thyreoïditis. Gedurende de eerste fase, als er sprake is van ontsteking, is de bloedbezinking verhoogd, evenals de schildklierhormoonconcentratie (T4 en T3). Het TSH-gehalte is juist onderdrukt. In deze fase laat de schildklierscan géén normale opname zien van radioactief jodium of technetium als uiting van de kapotte schildkliercellen, die niet tot opname in staat zijn. Gedurende een korte periode kunnen alle schildklierantistoffen verhoogd zijn, wat het onderscheiden van Hashimoto-thyreoïditis (zie verderop) moeilijk maakt.
Beloop en behandeling
De meeste patiënten genezen binnen drie tot zes weken; soms duurt het enkele maanden, slechts zelden langer. Na de fase van thyreotoxicose (verval van de cellen) is er een periode van hypothyreoïdie (de cellen zijn leeg) waarna in de meeste gevallen compleet herstel optreedt. Na een jaar heeft slechts een deel van de patiënten (met name degenen met een zeer ernstige thyreoiditis) een blijvende hypothyreoïdie. Omdat de ziekte meestal mild verloopt, is behandeling vaak niet nodig. Eventueel worden in verband met de pijn salicylaten (aspirine), paracetamol of een NSAID (zoals ibuprofen of diclofenac) geadviseerd. Als er heftige klachten zijn in de fase van thyreotoxicose kunnen bètablokkerende middelen uitkomst bieden. In ernstige gevallen kan kortdurende behandeling met prednison (bijnierschorshormoon) aangewezen zijn, eerst in een hoge dosis (30-40 mg per dag) en in drie tot zes weken uitlopend tot 0. Behandeling met schildklierremmers is nooit nodig.
Na herstel normaliseren bloedbezinking, schildklierfunctie en scintigram, hoewel dit laatste zelden of nooit wordt gecontroleerd.
Andere vormen van thyreoïditis
Hashimoto-thyreoïditis
Bij de Hashimoto-thyreoïditis kan het klinische beeld lijken op dat van De Quervain, zij het dat de schildklierantistoffen sterker zijn en hun aanwezigheid meer blijvend van aard is, dat de bloedbezinking vaak wat lager is en dat de schildklierscan hoogstens verminderde en soms zelfs normale opname van radioactief jodium laat zien.
Silent of painless thyreoïditis
Silent of painless thyreoïditis lijkt erg op de subacute thyreoïditis, maar dan zonder pijn. Het is in feite een variant van Hashimoto. Hierbij worden dan ook vaak antistoffen tegen de schildklier gezien (zoals bij Hashimoto), en ook een hoge bezinking. Het beloop lijkt eveneens op de subacute variant, alleen wordt vaker een blijvende hypothyreoïdie gezien. Eenzelfde beeld zien we ook wel in de eerste jaren na een zwangerschap. Dat noemen we dan een postpartum thyreoïditis (zie hoofdstuk 8).
Amiodarone geïnduceerde thyreoïditis
Op een onvoorspelbaar moment kan tijdens amiodarone therapie een hyperthyreoidie ontstaan. Er zijn twee types: type 1 treft patiënten die al een schildklieraandoening hebben, zoals de ziekte van Graves of multinodulair struma. Deze vorm is door de overmaat aan jodium geïnduceerd en gaat gepaard met een verhoogde schildklierhormoonsynthese. Ook kunnen antilichamen tegen de schildklier worden gevonden (TSAb, TPO). De behandeling is met thiamazol en kaliumperchloraat en is niet altijd eenvoudig. Na de behandeling treedt geen hypothyreoïdie op. In het algemeen wordt geprobeerd om de amiodarone therapie in deze groep te staken, maar dat is lang niet altijd mogelijk. In sommige gevallen zal door middel van een operatie de schildklier verwijderd worden. Type 2 is een destructieve thyreoïditis met een beeld en beloop die lijken op die van de subacute thyreoïditis en wordt veroorzaakt door het toxische effect van amiodarone op de schildkliercellen. In deze groep is er in het algemeen geen sprake van een voorafgaande schildklieraandoening, is er zelden een (kleine) struma en ontbreken antistoffen. De behandeling vindt plaats met prednison gedurende enkele maanden en de amiodarone hoeft niet te worden gestopt. Na de behandeling komt een hypothyreote fase vaak voor.
Riedelse thyreoïditis
Hiermee wordt een chronische thyreoïditis bedoeld, waarbij verbindweefseling (fibrose) optreedt. Door die fibrose ontstaat een zeer harde struma met hypothyreoïdie. De chronische fibreuze thyreoïditis van Riedel is zeer zeldzaam en er is verband met soortgelijke, ook zeldzame, problemen in de buik zoals retroperitoneale fibrose en scleroserende cholangitis.
Schildklierkanker
Schildklierkanker komt niet erg vaak voor (ongeveer 700 nieuwe gevallen per jaar in Nederland) en de sterfte eraan is gelukkig laag. Net als bij andere schildklieraandoeningen komt het vaker bij vrouwen dan bij mannen voor (als bij een man een nodus wordt gevonden is de verdenking op schildklierkanker echter groter omdat schildklierafwijkingen bij mannen niet zo vaak voorkomen). Het kan op alle leeftijden optreden, maar het meest vóór het twintigste en na het zeventigste levensjaar. Veel klachten zijn er vaak niet. In het algemeen ontstaat er verdenking bij het ontdekken van een solitaire (enkele) of prominente schildkliernodus. Daarbij moeten we ons realiseren dat verreweg de meeste knobbels uiteindelijk goedaardig blijken te zijn.
Risicofactoren
De kans dat een nodus maligne is ligt ergens tussen de 5 en 10 procent. Er bestaan factoren die de kans op een kwaadaardige aandoening in een nodus verhogen. Deze factoren staan vermeld in tabel 14.

De belangrijkste factoren die de verdenking op schildklierkanker groter kunnen maken, zijn:
- bestraling met röntgenstralen op de hals in de (vroege) jeugd (latentietijd 10-30 jaar);
- schildkliercarcinoom in de familie;
- een knobbel in een asymmetrische schildklier bij een man of een kind;
- heesheid; stridor (sterk hoorbare inademing);
- voelbaar grotere lymfklieren in de hals bij iemand met een struma of schildkliernodus;
- zeer harde schildklier of nodus; nodus groter dan 4 cm;
- niet beweeglijke nodus bij slikken, dus vastzittend aan huid of spieren;
- kernreactorongevallen (Tsjernobyl, Fukushima);
- een acuut ontstane al of niet pijnlijke knobbel in de hals.
Onderzoek
Nader onderzoek bij knobbels die verdacht zijn van kanker levert vaak weinig op. De functie is gewoonlijk normaal. Bij de echografie wordt meestal een echoarme solide nodus gevonden. De geoefende echografist kan bepaalde kenmerken opsporen, die de verdenking op een kwaadaardige tumor vergroten. Dit zijn: microcalcificaties (kleine verkalkingen), het ontbreken van een halo (een lichte rand om de nodus), onregelmatige begrenzingen, vermeerderde bloedstromen in de nodus en een echo-arm karakter van de nodus. Tegenwoordig is in specifieke gevallen, als het cytologisch onderzoek niet geheel conclusief is, ook onderzoek naar bepaalde moleculaire merkers mogelijk, die bij aanwezigheid de kans op een kwaadaardigheid vergroten. Dit onderzoek wordt echter nog niet algemeen toegepast.
De cytologische punctie is direct en betrouwbaar, mits uitgevoerd onder echocontrole door een ervaren dokter en beoordeeld door een ervaren patholoog. Alhoewel schildklierkanker zich in de meeste gevallen dus presenteert als een solitaire nodus wordt een aanzienlijk deel gevonden bij patiënten met multipele wisselend actieve noduli (dus ook bij een veranderende multinodulaire struma). Minder vaak is de eerste manifestatie het optreden van uitzaaiingen in (hals)lymfklieren of op afstand (bot, long).
De presentatie van schildkliercarcinoom kan divers zijn en staat vermeld in tabel 15.

Soorten schildklierkanker
De meest voorkomende vormen van schildklierkanker zijn de gedifferentieerde vormen; dat wil zeggen dat de kanker zich bij pathologisch onderzoek ordelijk gedraagt, waarbij de cellen lijken op gewone schildkliercellen. Hieronder vallen het papillaire en folliculaire schildkliercarcinoom. Er zijn echter ook kankervormen die zich minder ordelijk en zelfs agressief gedragen. Een dergelijke vorm heet ongedifferentieerd of anaplastisch carcinoom. Daarnaast zijn er zeldzamer vormen, zoals het medullair schildkliercarcinoom, het lymfoom en de metastasen (uitzaaiing van carcinomen elders in het lichaam).
De gedifferentieerde carcinomen komen het meest voor en zijn gelukkig ook het best te behandelen. De belangrijkste kenmerken van de diverse schildkliercarcinomen staan vermeld in tabel 16.

In de nu volgende paragrafen worden de verschillende vormen van schildklierkanker apart besproken.
Gedifferentieerde carcinomen
Bij de gedifferentieerde carcinomen gaat het dus om papillair en folliculair schildkliercarcinoom. Het papillaire carcinoom komt als vorm het meest voor en heeft de beste prognose. Beide vormen komen op alle leeftijden voor, zij het dat we bij kinderen vaker de papillaire vormen aantreffen. Behoudens de eerder genoemde risicofactoren is de oorzaak meestal onbekend.
Papillaire carcinomen zaaien vooral uit naar lymfklieren in de hals en komen nogal eens op meer plekken tegelijk in de schildklier voor; dit kunnen overigens ook lymfogeen veroorzaakte metastasen zijn in de schildklier. De folliculaire carcinomen zijn iets agressiever dan de papillaire, met name bij ouderen, en zaaien via het bloed uit (we noemen dat hematogeen metastaseren).
Via het bloed komen uitzaaiingen vooral voor in longen en skelet. Een variant van het folliculaire carcinoom is het ‘Hürthle-cel’carcinoom, waarbij de cellen er iets anders uitzien. Deze Hürthle-celvariant reageert in het algemeen minder goed op therapie met radioactief jodium.
De folliculaire carcinomen zijn meestal omkapseld en tonen ingroeiing in kapsel en bloedvaten. Dit is pas te zien als je de hele afwijking (dus meestal een schildklierkwab) wegneemt en nakijkt. Vandaar dat de cytologische punctie (alleen losse cellen) het onderscheid tussen goed- en kwaadaardig hier eigenlijk niet goed kan maken.
De behandeling is voor alle vormen van gedifferentieerd schildkliercarcinoom grofweg hetzelfde. De schildklier wordt in zijn geheel verwijderd (in geval van twijfel na de cytologische punctie gebeurt dit vaak in twee operaties). Aansluitend wordt therapie met radioactief jodium gegeven om eventueel nog aanwezig schildklierweefsel uit te schakelen en de follow-up te vergemakkelijken. Eventuele uitzaaiingen worden meestal met radioactief jodium meebehandeld. In sommige gevallen is er voor uitzaaiingen ook nog extra lokale behandeling nodig zoals een operatie of bestraling. Hierna krijgt de patiënt therapie met schildklierhormoon (thyroxine) enerzijds om de schildklier te vervangen en anderzijds om mogelijke hypofysestimulatie via TSH van achtergebleven schildkliercellen te voorkomen. Men streeft naar een TSH-gehalte in het bloed onder het normale niveau, in ieder geval gedurende de eerste periode.
Omdat met de verbeterde en veel vaker gebruikte diagnostische technieken tegenwoordig meer en vaak ook (heel) kleine (vooral papillaire) carcinomen (incidentalomen) worden gevonden, wordt in die gevallen volstaan met een kleinere ingreep, zonder aansluitende therapie met radioactief jodium. Behandeling met thyroxine is dan meestal ook niet nodig. De prognose van deze groep is uitstekend.
Als er geen schildklierweefsel meer is, is het thyreoglobulinegehalte in het bloed een goede maat om na te gaan of er recidieven optreden. Thyreoglobuline komt immers alleen in schildklierweefsel (normaal + kankercellen) voor. Als er antistoffen tegen thyreoglobuline bestaan, kan de bepaling foutief laag zijn en dus onbetrouwbaar. Ongeveer een jaar na de therapie wordt onder TSH-stimulatie een nieuwe thyreoglobulinemeting verricht. Dit wordt ook wel dynamische herstratificatie genoemd. Als bij een dergelijke dynamische herstratificatie het thyreoglobuline onmeetbaar laag is, is het risico dat de ziekte nog terugkomt <5 procent en wordt de patiënt geclassificeerd als laag risico. Hiermee kan dan in de verdere follow-up rekening gehouden worden.
TSH-stimulatie kan gebeuren door de thyroxinetherapie tijdelijk te onderbreken of door recombinant humaan TSH (Thyrogen®) te gebruiken. Dit laatste heeft als voordeel dat de klachten van onttrekking van schildklierhormoon kunnen worden vermeden. Patiënten worden gewoonlijk jarenlang gecontroleerd, maar uiteindelijk niet vaker dan eenmaal per jaar. Niet alle metastasen nemen radioactief jodium op, dan is operatie of bestraling zo mogelijk nodig. Tegenwoordig kunnen patiënten met snelgroeiende uitzaaiingen die geen radioactief jodium meer opnemen, behandeld worden met nieuwe klassen medicamenten.
Medullair schildkliercarcinoom
Het medullair schildkliercarcinoom is een zeldzame vorm van kanker die ontstaat uit de C-cellen in de schildklier. Dit carcinoom kan de stof calcitonine produceren, die in het bloed te meten is. Soms worden ook nog andere hormonen gevormd of CEA (carcinogenic embryonic antigen, een stofje dat eigenlijk een tumormerker is van dikkedarmkanker). Het kan via de andere hormonen diarree veroorzaken. Ook wordt het gezien in combinatie met bijniertumoren (feochromocytoom) en hyperparathyreoïdie (te hard werkende bijschildklieren). Men spreekt dan van een MEN2-syndroom (MEN staat voor multipele endocriene neoplasie). In ongeveer de helft van de patiënten met een medullair schildkliercarcinoom is er sprake van een MEN2-syndroom. Dit ontstaat door een afwijking in het DNA en komt in families voor. Familieleden van patiënten met een MEN2-syndroom wordt daarom aangeraden om zich te laten onderzoeken op de aan- of afwezigheid van het MEN2-syndroom.
Uitzaaiingen vinden zowel hematogeen als lymfogeen (via de lymfklieren) plaats. De behandeling is vaak lastiger dan bij de gedifferentieerde carcinomen. In eerste instantie wordt geopereerd (totale schildklierverwijdering, verwijdering van de centrale klieren in de hals en zo nodig ook verwijdering van de klieren aan de zijkant van de hals als er sprake is van metastasen) en vervolgens wordt thyroxine voorgeschreven. Radioactief jodium helpt niet omdat deze cellen geen radioactief jodium opnemen. De prognose is slechter dan bij de gedifferentieerde carcinomen. Bij recidieven wordt zoveel mogelijk gestreefd naar lokale therapie (door bijvoorbeeld heroperatie of bestraling). Patiënten met meerdere groeiende uitzaaiingen kunnen worden behandeld met nieuwe klassen medicamenten. De follow-up wordt gedaan via het eerder genoemde calcitoninegehalte en CEA in het bloed, en door echografie en CT-scanning.
Ongedifferentieerd of anaplastisch carcinoom
Deze agressieve tumor, die erg slecht te behandelen is, komt gelukkig weinig voor. De schildklier voelt hard aan en groeit snel, ook in de omliggende weefsels. Het komt vooral op hogere leeftijd voor (ouder dan vijftig jaar). De behandeling helpt slechts tijdelijk en bestaat uit uitwendige bestraling of chemotherapie. Zelden is operatie mogelijk en zinvol.
Lymfoom
Het maligne lymfoom is een tumor die afkomstig is van witte bloedlichaampjes en die slechts zelden in de schildklier voorkomt. Het groeit snel en wordt nogal eens verward met het anaplastische carcinoom. Het reageert soms goed op bestraling en/of chemotherapie.
Metastasen
Uitzaaiingen in de schildklier van tumoren in long, borst of nier komen een enkele keer voor. Meestal is de primaire tumor wel bekend en is behandeling afhankelijk van deze primaire tumor. De tumor is gewoonlijk al vergevorderd.
Schildklier en zwangerschap
Tijdens elke zwangerschap treden hormonale veranderingen op die ook de schildklier betreffen. In de normale zwangerschap treden symptomen op, zoals een snelle hartactie, warmtegevoelens, nervositeit, moeheid, een verhoogd basaal metabolisme en uitblijven van de menstruatie. Dit kan gemakkelijk worden verward met een hyperthyreoïdie, waarvan in het algemeen objectief gezien (bloedonderzoek) geen sprake is. Een milde hyperthyreoïdie is hierdoor echter moeilijk te herkennen.
Tijdens de zwangerschap is er een verhoogde behoefte aan schildklierhormoon. Dit komt onder andere door de behoefte van de foetus, die in het eerste trimester volledig afhankelijk is van het schildklierhormoon van de moeder voor zijn/haar ontwikkeling. Daarnaast stijgen de spiegels van het totaal T4 en T3, omdat het thyroxinebindend globuline (TBG) verhoogd is. Dit is dan weer het gevolg van een verhoogde oestrogeenproductie in de placenta (moederkoek). In deze toegenomen behoefte kan worden voorzien door het zwangerschapshormoon hCG, dat in hoge concentraties de schildklier kan stimuleren. De spiegels van het vrije T4 (dat wil zeggen niet aan eiwit = TBG-gebonden) zullen hierdoor ook stijgen, wat zal leiden tot een lichte daling in het TSH van de moeder tijdens de zwangerschap.
Auto-immuunziekten die al voor de zwangerschap bestonden, zoals de ziekte van Graves, verlopen tijdens de zwangerschap milder. Antilichaamgehalten dalen daarbij. Na de bevalling kan een verergering optreden.
In het eerste trimester is het ongeboren kind volledig afhankelijk van de moeder wat de schildklierhormoonvorming betreft. Daarna ontwikkelt de schildklier zich bij het kind, die pas rond week 20 van de zwangerschap echt volledig functioneel is.
De placenta is een natuurlijke barrière tussen moeder en kind. Een aantal stoffen is echter in staat de placenta te passeren en dat kan gevolgen hebben voor de therapie die men eventueel geeft. Antistoffen, zoals die voorkomen bij de ziekte van Graves, kunnen de foetale schildklier stimuleren of remmen. Geneesmiddelen, zoals thyreostatica (bijvoorbeeld methimazol = strumazol en propylthiouracil = PTU), bètablokkerende middelen (propranolol, bisopropol) en (radioactief) jodium, passeren de placenta. Omdat schildklierhormoon, met name later in de zwangerschap de placenta minder goed passeert, moet eventuele therapie voor hyperthyreoïdie worden aangepast (zie verderop).
Hyperthyreoïdie en zwangerschap
Hyperthyreote patiënten raken minder gemakkelijk zwanger. Dit verandert echter als de hyperthyreoïdie wordt behandeld.
Hyperthyreoïdie kan ook tijdens de zwangerschap ontstaan, al gebeurt dat niet zo vaak. Overmatig zwangerschapsbraken (hyperemesis gravidarum) kan gepaard gaan met hyperthyreoïdie omdat de hoge concentraties van het zwangerschapshormoon hCG een TSH-achtige werking hebben en zo de concentraties van (F)T4 en T3 verhogen.
Het herkennen ervan is niet altijd gemakkelijk. De meest voorkomende oorzaak tijdens de zwangerschap is de ziekte van Graves, of een subacute thyreoïditis. Deze laatste wordt vaak voorafgegaan door een virale infectie en wordt evenmin altijd herkend. Belangrijk bij de ziekte van Graves is dat er autoantilichamen circuleren in het bloed van de moeder, die ook kunnen overgaan naar het ongeboren kind.
Bij vrouwen die de ziekte van Graves hebben of in het verleden hebben gehad moeten deze antilichamen (TSAb = TSH-receptorstimulerende antilichamen oftewel TSI = thyroid stimulating immunoglobulins) worden bepaald omdat de aanwezigheid ervan consequenties kan hebben voor het kind. Als ze in het bloed van het kind komen, dan kan dit in de baarmoeder en in de eerste weken na de bevalling verschijnselen van hyperthyreoïdie geven, wat extra aandacht van eerst de gynaecoloog en later de kinderarts noodzakelijk maakt.
De diagnose hyperthyreoïdie bij de zwangere vrouw kan zoals gewoonlijk gesteld worden door het meten van hoge vrije T4-spiegels in combinatie met een laag TSH-gehalte in het bloed. De T3-spiegel is vaak al verhoogd door de zwangerschap omdat daarvan meestal niet de vrije fractie, maar het totaal wordt gemeten. Zoals hiervoor is uitgelegd, zal de totale T3-concentratie hoog zijn door de hoge eiwit-(TBG-)spiegels. Het is belangrijk dat een schildklierscan tijdens de zwangerschap niet kan worden gemaakt in verband met de stralenbelasting voor het kind, maar een echografie maken kan wel (dat is tenslotte een ‘geluidsonderzoek’). De behandeling van hyperthyroïdie in de zwangerschap is anders dan bij de niet-zwangere patiënt.
Omdat de schildklierremmende medicatie (thyreostatica) de placenta goed en schildklierhormoon de placenta in mindere mate passeert, wordt gezocht naar de laagst mogelijke dosering van het thyreostaticum zonder toevoeging van schildklierhormoon. Dit is anders dan buiten de zwangerschap wanneer vaak combinatietherapie gegeven wordt, waarbij met een hogere dosis thyreostaticum de schildklier wordt platgelegd, en daarnaast het T4 wordt aangevuld (de zogeheten block and replace-therapie). Omdat er de laatste jaren meer en meer bewijs is dat strumazol een verhoogd risico geeft op aangeboren afwijkingen bij het kind, wordt tijdens de zwangerschap vaak voor PTU gekozen. PTU geeft weliswaar een hoger risico op bepaalde aangeboren afwijkingen, maar deze zijn in het algemeen minder erg. In zeldzame gevallen kan PTU-gebruik echter wel leiden tot leverfalen. Wat dat betreft heeft het, als mogelijk, de voorkeur om reeds voor de zwangerschap een blijvende therapie voor de Graves te geven zodat beide medicijnen tijdens de zwangerschap vermeden kunnen worden. Gelukkig is vaak is tijdens de zwangerschap een zeer lage dosis of geen therapie al genoeg. Uiteraard kan radioactief jodiumtherapie niet worden gegeven. Soms is een operatie (thyroïdectomie) nodig. Dit wordt dan het beste in het tweede trimester uitgevoerd. Dit gaat meestal zonder problemen.
Van belang is nog om te vermelden dat het raadzaam is om – als iemand om welke reden dan ook therapie met radioactief jodium heeft gekregen – minstens een halfjaar te wachten met een zwangerschap. Dit geldt niet alleen voor vrouwen, maar ook voor mannen. Er is anders een risico op miskramen en aangeboren afwijkingen.
Hypothyreoïdie en zwangerschap
Vrouwen met een onbehandelde hypothyreoïdie worden niet gemakkelijk zwanger. Na goede behandeling is de zwangerschapskans normaal. De diagnose hypothyreoïdie tijdens de zwangerschap wordt op dezelfde manier gesteld als buiten de zwangerschap. Een verhoogde TSH- en een verlaagde FT4-spiegel zijn bewijzend voor de diagnose. Wel is het zo dat door de veranderingen die plaatsvinden tijdens de zwangerschap de referentiewaarden (normaalwaarden) in de zwangerschap anders zijn dan daarvoor of daarna.
Ook de behandeling is grotendeels hetzelfde: de thyroxinetherapie wordt opgehoogd tot de TSH-concentratie normaal is. Gezien het belang van schildklierhormoon voor het kind wordt ernaar gestreefd om zo snel mogelijk normale schildklierhormoonwaarden in het bloed te hebben.
Bij patiënten die al gesubstitueerd worden met schildklierhormoon voor ze zwanger werden, is het belangrijk om af te spreken dat de dosis met 25-30 procent moet worden opgehoogd bij een positieve zwangerschapstest. Dit vanwege de toegenomen behoefte aan schildlierhormoon en het belang van een goede hoeveelheid hormoon voor een optimale ontwikkeling van het kind. Men streeft naar hoog-normale waarden van de FT4 en adviseert tijdens het begin van de zwangerschap om de 4-6 weken TSH en FT4- waarden te meten. Later in de zwangerschap kan er meer tijd tussen de metingen zitten. Direct na de zwangerschap kan men teruggaan naar dezelfde dosering als voor de zwangerschap.
Met deze voorzorgsmaatregelen is een normale zwangerschap mogelijk en loopt het kind geen gevaar.
Struma en zwangerschap
Omdat de behoefte aan jodium tijdens de zwangerschap groter is dan normaal, is lang gedacht dat de schildklier groeit in de loop van de zwangerschap. Dit blijkt in landen waarin voldoende jodium beschikbaar is, zoals in Nederland, niet het geval te zijn. In die gebieden (en dat zijn er nogal wat in de wereld) waar wel jodiumgebrek is, groeit de schildklier wel en kan een struma voelbaar worden. De grootte valt meestal wel mee. In die zeer zeldzame gevallen dat een bestaande (meestal nodulaire) struma onaanvaardbaar groeit en ingrijpen nodig is, wordt de voorkeur gegeven aan een operatie in het tweede trimester.
Schildklierkanker en zwangerschap
Soms wordt tijdens de zwangerschap een nodus ontdekt. Omdat de prognose van schildklierkanker niet slechter is als pas na de bevalling een operatie wordt verricht, wordt een cytologische punctie van de nodus bij voorkeur uitgesteld tot na de bevalling. Wanneer er wel een punctie verricht wordt en het om schildklierkanker blijkt te gaan, wordt meestal gewacht met opereren tot na de bevalling. Als er wel geopereerd moet worden, kan dit het beste in het tweede trimester gebeuren.
Bij patiënten die schildklierkanker hebben, bestaat soms de wens om zwanger te worden. Wanneer patiënten behandelingen moeten ondergaan (met radioactief jodium of met moderne antikankermedicamenten) is zwangerschap gecontraïndiceerd. In andere gevallen, ook wanneer er uitzaaiingen bestaan die niet of zeer langzaam groeien, heeft zwangerschap waarschijnlijk geen negatieve gevolgen voor de prognose.
Problemen in de periode na de bevalling
In de eerste maanden na de bevalling kan de schildklierwerking enige tijd gestoord zijn, vooral als van tevoren al schildklierantilichamen aanwezig waren. Soms wordt dit opgevat als een postnatale depressie.
Er zijn enkele specifieke beelden die hieronder kort worden besproken.
Postpartum thyreoïditis
In het eerste jaar na een bevalling of miskraam kan thyreotoxicose optreden die op een postpartum thyreoïditis berust. Het ziektebeeld lijkt op dat van de stille thyreoïditis (zie hoofdstuk 6) en gaat vanzelf over. Waarschijnlijk is er ook enige verwantschap met de Hashimoto-thyreoïditis. Tijdens de hyperthyreote fase kan behandeling met een bètablokker nodig zijn, in de hypothyreote fase dient de patiënte behandeld te worden met T4. Bij patiënten met diabetes treedt de ziekte vaker op.
Na een volgende zwangerschap treedt het bij ongeveer de helft opnieuw op. Bij ongeveer een kwart treedt op den duur een permanente hypothyreoïdie op.
Syndroom van Sheehan
Als door overmatig bloedverlies tijdens de bevalling een infarct in de hypofyse optreedt, spreekt men van het syndroom van Sheehan. Door uitval van de hypofyse kan er een tekort ontstaan van diverse hormonen, waaronder het schildklierhormoon. Bij de acute situatie is behandeling met bijnierhormoon als eerste aangewezen. Als daarna de borstvoeding of de menstruatie niet op gang komt, kan dit wijzen op hypothyreoïdie. Gelukkig komt dit slechts zeer zelden voor.
Problemen bij pasgeborenen
Veel van de problemen die kunnen voorkomen, zijn al aan de orde geweest. Aangeboren hyperthyreoïdie is zeer zeldzaam en meestal van voorbijgaande aard. Het hangt samen met de schildklierstimulerende antilichamen in het bloed van de moeder (soms zelfs lang na een goed behandelde ziekte van Graves).
Ook aangeboren hypothyreoïdie komt weinig frequent voor. Dit kan door overbehandeling met thyreostatica van de moeder optreden, maar gebeurt vaker door een aangeboren afwijking in de fabricage van schildklierhormoon bij de baby zelf. Elders in de wereld, in gebieden met jodiumgebrek, komen hypothyreoïdie en cretinisme wel vaker voor. Omdat niet-behandelen van de hypothyreoïdie in deze periode grote consequenties heeft, vooral voor de hersenen, wordt bij iedere pasgeborene via de hielprik de schildklierfunctie gemeten. Zo kan vroeg met de eventueel noodzakelijke behandeling worden begonnen en kan het kind een normale ontwikkeling hebben.
Overige problemen met de schildklier
In dit laatste hoofdstuk komen verschillende problemen aan de orde die min of meer samenhangen met de werking van de schildklier, maar die niet direct afwijkingen van de schildklier zelf zijn.
Hypofyse-uitval
Uitval van de hypofyse kan optreden als gevolg van een (meestal goedaardige) hypofysetumor of na een heftige bloeding, bijvoorbeeld na een bevalling (syndroom van Sheehan, zie hoofdstuk 8). Hierbij kan de schildklier uitvallen. Belangrijk is dan te bedenken dat ook andere hormoonsystemen, in het bijzonder de bijnieren, de eierstokken en het groeihormoon kunnen uitvallen. Voordat eventuele schildklierhormoontherapie wordt voorgeschreven, is het noodzakelijk te weten te komen of de bijnieren normaal functioneren. Als dat niet zo is, dient eerst het tekort aan bijnierschorshormoon te worden behandeld met behulp van tablettherapie (hydrocortison). Zou eerst schildklierhormoon gegeven zijn, dan kan de patiënt ernstig in de problemen komen en zelfs in coma raken als de bijnieren het helemaal opgeven en de extra behoefte, ontstaan door het geven van schildklierhormoon, niet aankunnen.
MEN-syndromen
MEN betekent multipele (veelvoudige) endocriene neoplasie (nieuwvorming). De MEN-syndromen 1, 2A en 2B komen vaak in de familie voor en omvatten ieder een aantal endocriene aandoeningen (tabel 17). Bij de MEN 2-syndromen hoort het medullaire schildkliercarcinoom dat bij MEN 2A gecombineerd voorkomt met vooral primaire hyperparathyreoïdie en feochromocytoom en bij MEN 2B vooral met feochromocytoom, neuromen van de slijmvliezen en huid en een marfanoïde habitus (lang, mager en slungelig uiterlijk met dikke lippen en tong en overrekbare gewrichten).

Polyglandulaire auto-immuunsyndromen (PGA)
Hierbij worden aandoeningen bedoeld waarbij sprake is van antistoffen tegen eigen lichaamscellen (auto-immuunaandoeningen) en waarbij minstens twee endocriene klieren en andere niet-endocriene auto-immuunafwijkingen zijn betrokken. Er zijn drie typen en in elk ervan komen schildklierafwijkingen voor. Ze staan opgesomd in tabel 18.

Type 1 begint al op de kinderleeftijd. Type 2 wordt ook wel het syndroom van Schmidt genoemd. De polyglandulaire auto-immuunsyndromen zijn betrekkelijk zeldzaam.
‘Euthyroid sick syndrome’
Het euthyroid sick syndrome, vroeger ook wel ‘non-thyroidal illness’ genoemd, is geen echte ziekte. Het komt voor bij ernstige, meestal acute ziekten waarbij de gehalten van T3 en soms ook T4 in het bloed dalen. Het TSH-gehalte is daarbij vaak normaal. Men gaat er vanuit dat er waarschijnlijk sprake is van adaptatie en dat de patiënt in feite euthyreoot is. Bij herstel stijgen T3 en T4 tot normaal en wordt er soms korte tijd een geringe TSH-stijging gezien.
Als alleen het T3 verlaagd is, spreekt men ook wel over het low T3-syndrome. Hiervan zijn meer oorzaken bekend, die vermeld staan in tabel 4.
Psychiatrie
Omdat de klachten van zowel hypo- als hyperthyreoïdie niet altijd compleet en specifiek zijn, kunnen beide aandoeningen gemakkelijk ten onrechte worden aangezien voor psychiatrische ziekten. Speciale aandacht verdient daarbij het ziektebeeld apathische hyperthyreoïdie, omdat deze nog gemakkelijker kan worden gemist. Hierbij is er waarschijnlijk sprake van een verwaarloosde, niet vastgestelde, hyperthyreoïdie, die dus ook niet wordt behandeld. De patiënten zijn gewoonlijk ouder en ze zijn vaak inactief en depressief, volstrekt anders dan bij een gewone hyperthyreoïdie. Zelfs de polsfrequentie is vaak aan de lage kant. Behandeling is als de gewone hyperthyreoïdie, vaak is therapie met radioactief jodium nodig. Bij twijfel wordt geadviseerd bloedonderzoek te doen (TSH). Op die manier is in het algemeen simpel een afwijkende schildklierfunctie vast te stellen en hoeft de psychiater niet te worden ingeschakeld.
Pijn in de hals
Alhoewel door menigeen bij pijn in de hals (schildklier) in eerste instantie zal worden gedacht aan een carcinoom, wordt dit slechts zelden veroorzaakt door een carcinoom. Veel vaker is er sprake van een bloeding in een cyste of een subacute thyreoïditis, waarvan de verdere kenmerken staan vermeld in tabel 19.

Resistentie voor schildklierhormoon
Resistentie betekent ongevoeligheid. In bepaalde families komt, zowel bij mannen als bij vrouwen, resistentie voor schildklierhormoon voor. Dit gebeurt meestal door een defect in een van de receptoren voor schildklierhormoon. Bij de meest voorkomende vorm (door een defect in de bètareceptor die ook in de hypofyse zit) probeert het lichaam hiervoor te compenseren. Er wordt meer schildklierhormoon gevormd en daardoor zijn de spiegels van T4 en T3 in het bloed hoog. Opvallend daarbij is dat de TSH-waarde normaal of licht verhoogd is, terwijl hij normaal gesproken onderdrukt zou moeten zijn.
De reactie van de verschillende lichaamsweefsels op deze hoge schildklierhormoonwaarden is wisselend, zowel een normale als een verminderde respons is mogelijk. Onder deze omstandigheden kan ook een struma ontstaan. Behandeling in de zin van radioactief jodium of operatie is niet aangewezen en levert meestal geen verbetering op, T4 en T3 blijven hoog, steeds weer met een normaal TSH. Deze normale TSH-spiegel moet er dus op wijzen dat er een euthyreote toestand is en dat behandeling onnodig is.
Hypothyreote patiënten met ongevoeligheid voor schildklierhormoon hebben vaak (zeer) hoge doses thyroxine nodig om het TSH te normaliseren. Dit gaat dan gepaard met hoge FT4- en T3-spiegels, zoals te verwachten is.
Recentelijk is ook een vorm van resistentie ontdekt door een defect in de alfareceptor voor schildklierhormoon. Deze receptor zit niet in de hypofyse, en daardoor zijn over het algemeen het TSH en FT4 niet afwijkend. Deze patiënten hebben met name last van een verminderde werking van schildklierhormoon in de hersenen, het bot en de darmen en hebben in het algemeen baat van behandeling met extra schildklierhormoon.
